В промышленности эту реакцию ведут по Кучерову в присутствии сульфата ртути или гетерогенных катализаторов.
Из ацетилена получают уксусный альдегид и его гомологов – кетоны.
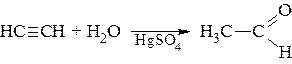
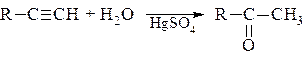
Присоединение идет по правилу Марковникова.
Спирты присоединяются к ацетиленам по правилу Марковникова в присутствии алкоголятов (RONa), комплексов фтористого бора. Получаются простые виниловые эфиры, которые используют как мономеры.
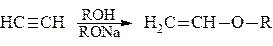
В реакциях с органическими кислотами получают сложные виниловые эфиры, которые тоже используются как мономеры (присоединение – по Марковникову).
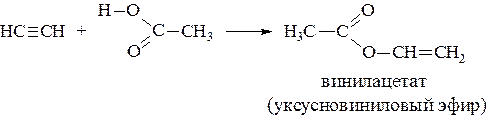
Ацетилен в присутствии медных солей присоединяет также синильную кислоту с образованием важного мономера – акрилонитрила.
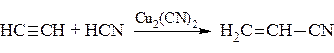
Полимеризация.
а) при нагревании с активированным углем образуется бензол.
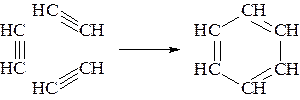
б) в присутствии CuCl и NH4Cl ацетилен димеризуется и тримеризуется линейно с образованием винилацетилена и дивинилацетилена.

Винилацетилен гидрохлорируют с образованием хлоропрена, который идет на получение хлоропренового каучука.
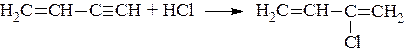
Реакции, обусловленные повышенной подвижностью водородных атомов при углеродах с тройной связью:
Атомы водорода могут быть замещены на металлы (Na, Ag, Cu и другие).
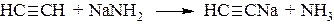
ацетиленид натрия
Ацетилениды исключительно взрывоопасны в сухом виде.
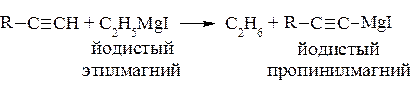
Эти соединения используются для получения кислот и спиртов с тройной связью.
Ацетилены с концевой тройной связью могут присоединяться с разрывом связи CH, сохраняя тройную связь (проявление кислотных свойств).
В промышленности на катализаторах проводят конденсацию ацетилена с муравьиным альдегидом (ацетилен после диссоциации по связи ≡С-Н присоединяется по месту разрыва p -связи С=О).
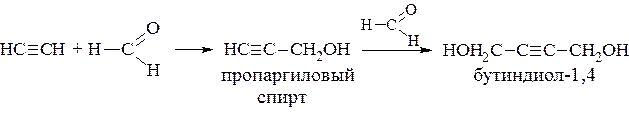
Из первого продукта получают глицерин, из второго – дивинил и адипиновую кислоту.
Ацетиленовые углеводороды способны изомеризоваться с перемещением тройной связи или с превращением в диеновые углеводороды. Как установил А.Е. Фаворский, промежуточными продуктами в этих реакциях являются алленовые углеводороды.
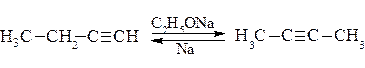
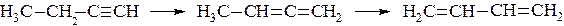
 2014-02-02
2014-02-02 773
773







