Связь и взаимные превращения углеводородов различных классов отражены на схеме:
циклизация дигалогенпроизводных

|





 гидрирование
гидрирование 
 | |||||||||
 |  |  | |||||||
 | |||||||||

| гидрирование | дегидрирование | гидрирование | Дегидроциклизация |




    гидрирование гидрирование
дегидрирование дегидрирование | диеновый синтез гидрирование | ||||||||||
     гидрирование гидрирование | тримеризация | дегидрирование | |||||||||
АЛКАНЫ
(насыщенные алифатические углеводороды, парафины)
Общая формула СnH2n+2.Гомологическая разность -СН2.В молекулах алканов атомы углерода соединены в прямые или разветвленные цепи одинарными связями.
| Гомологический ряд алканов | |||
| брутто-формула | название | брутто-формула | название |
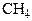 | метан | 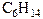 | гексан |
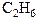 | этан | 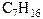 | гептан |
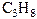 | пропан | 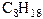 | октан |
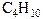 | бутан | 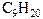 | нонан |
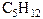 | пентан | 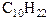 | декан |
Номенклатура, изомерия. Каждый гомолог метана имеет название с суффиксом –ан. Корни слов, обозначающие названия первых членов гомологического ряда – мет-, эт-, проп-, бут-. Названия следующих гомологов образованы от корней греческих и латинских названий числительных.
Для алканов характерна изомерия углеродного скелета. Соединения, имеющие характерное разветвление на конце углерод–углеродной цепи, называют, добавляя приставку изо-:
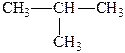
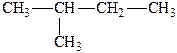
изобутан изопентан
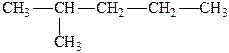
изогексан
Согласно правилам номенклатуры IUPAC (ИЮПАК), при составлении названия сложного разветвленного углеводорода выбирают наиболее длинную цепь углеродных атомов (главная цепь) и нумеруют ее с того конца, ближе к которому находится большинство боковых ответвлений (заместителей). Основу названия составляет название алкана, соответствующего количеству атомов углерода главной цепи, боковые ответвления называют как радикалы с указанием (цифрой) номера углерода главной цепи, к которому они относятся:

2,2,4-триметил-3-этилгептан
Одинаковые радикалы группируются вместе, их общее количество указывают с помощью соответствующих префиксов: если их два – ди, три –три, четыре – тетра, пять – пента и так далее с использованием греческих числительных.
| Структура радикала | Название радикала |
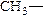 | метил |
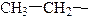 | этил |
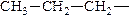 | пропил |
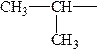 | изопропил |
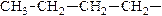 | бутил |
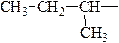 | вторичный бутил |
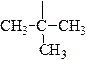 | третичный бутил |
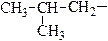 | изобутил |
Для алканов характерна структурная изомерия (пример – все изомеры пентана).
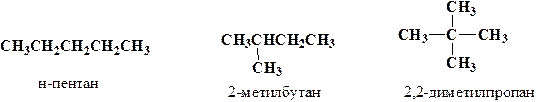
Изомеры – соединения, имеющие один и тот же брутто-состав, но разную структуру (разная последовательность соединения атомов в молекуле).
Тип связи. В молекулах алканов атом углерода находится в состоянии sp³- гибридизации.
Термин гибридизация обозначает смешение валентных (внешних) орбиталей и выравнивание их по форме и энергии. sp³- гибридизация – это концепция, призванная объяснить эквивалентность всех C—H–связей в метане.
1s 2s 2р
 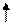  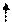   |

гибридизация
Рис. 1 Электронная структура и гибридизация атомных орбиталей углерода в алканах
sp³- Гибридные орбитали расположены под углом 109°28' друг к другу, поэтому углы между связями С-Н в метане, а также между связями С-С и С-Н в его гомологах такие же. Связи, образованные перекрыванием гибридных орбиталей называют σ-связями. Длина одинарной С-С связи равна 0,154 нм, энергия связи 83,6 Ккал.
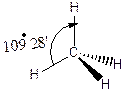
Рис.2 Тетраэдрическая модель молекулы метана.
Молекула метана имеет тедраэдрическую симметрию: если атом углерода расположить в центре правильного тетраэдра, то атомы водорода окажутся в его углах, и углы между связями С-Н составят 109°28'.
Физические свойства алканов: низшие С1-С4 – газы, С5-С16 – жидкости, С17 и далее – твердые соединения.
 2014-02-02
2014-02-02 1537
1537








