Таким образом, в системе из двух способных взаимодействовать с протоном веществ основанием всегда служит то, которое его прочнее связывает, т.е. характеризуется большим протонным сродством.
Таким образом, теория кислот и оснований Аррениуса-Оствальда полностью применима лишь к водным растворам веществ. Процессы, протекающие без участия растворителя, а также в неводных жидких средах, требуют существенного дополнения и обобщения данной теории.
Такой более общей теорией кислот и оснований явилась протолитическая теория, предложенная в 1923 г. независимо друг от друга датским ученым Бренстедом и английским ученым Лоури.

Йоханнес Николаус Бренстед (1879 – 1947) – датский физикохимик. Томас Мартин Лоури (1875 – 1936) – английский химик. Независимо друг от друга практически одновременно сформулировали основные положения протолитической теории кислот и оснований. Бренстед, основные работы которого посвящены термодинамике растворов и кислотно-основному катализу, разработал детали и количественное описание протолитической теории. Основной областью научных интересов Лоури были оптически активные органические соединения.
|
|
|
Согласно этой теории, кислотой называется всякая частица (молекула или ион), способная отдавать протон. Основанием является частица (молекула или ион), способная присоединять протон.
Причем отдача иона водорода кислотой всегда происходит в присутствии основания, которое его должно присоединить. При диссоциации кислоты в растворе в роли основания выступают молекулы растворителя:
| НА | + | Н2О | 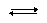 | А– | + | Н3О+ |
| кислота | основание | сопряженное основание | сопряженная кислота |
Образующаяся после отделения иона водорода частица А– называется сопряженным данной кислоте основанием, т.к. она способна снова присоединять к себе ион Н+.
Соответственно, частица, полученная после присоединения к основанию иона Н+, называется сопряженной данному основанию кислотой, т.к. способна отдавать его обратно:
| В | + | Н+ |  | ВН+ |
| основание | сопряженная кислота |
Кислота и основание в кислотно-основной паре взаимосвязаны друг с другом. Чем сильнее (слабее) кислота, тем слабее (сильнее) сопряженное с ней основание (табл. 13). Например, в водном растворе хлороводородная кислота HCl сильнее, чем уксусная кислота СН3СООН, поэтому ацетат ион СН3СОО– будет более сильным основанием, чем хлорид ион
Cl–.
Трактовка понятия «кислота» в протолитической теории Бренстеда-Лоури совпадает с теорией Аррениуса-Оствальда и лишь распространяет ее и на неводные растворы.
В случае же трактовки понятия «основание» подход совершенно другой. Например, гидроксид натрия NaOH считается основанием не потому, что он диссоциирует с отщеплением гидроксид-иона ОН–, а потому что этот ион может присоединять к себе ион Н+ с образованием молекулы воды. И именно его следует считать основанием в данном случае. Причем основные свойства ион ОН– проявляет в присутствии кислоты, способной отдать ему Н+. При растворении основания в роли такой кислоты опять же выступают молекулы растворителя:
|
|
|
| NН3 | + | HOH |  | NH4+ | + | ОH– |
| основание | кислота | сопряженная кислота | сопряженное основание |
Согласно протолитической теории, кислоты и основания могут быть трех типов: нейтральные, анионные и катионные.
В роли первых выступают нейтральные молекулы, способные отдавать или присоединять ион Н+, например: HCl, H2SO4, HNO3 (кислоты); NH3, CH3–O–CH3 (основания).
Анионные основания и кислоты представляют собой отрицательно заряженные ионы, например: HSO4–, HPO42–, HS– (кислоты); OH–, Cl–, NO3– (основания).
В роли катионных оснований и кислот выступают положительно заряженные ионы, например: NH4+, H3O+ (кислоты); H2N–NH3+, H2N–(CH2)2–NH3+ (основания).
Многие частицы (как молекулы, так и ионы) обладают амфотерными свойствами, т.е. в зависимости от условий могут выступать как в роли кислоты, так и в роли основания, например: H2O, NH3, HSO4–, H2N–NH3+ и т.д. Данные соединения называются амфипротными или амфолитами.
В некоторых случаях провести резкую грань между их кислотными и основными свойствами и определить, какие из этих свойств выражены сильнее, бывает затруднительно.
Кислотные свойства соединения в растворе определяют по отношению к растворителю как к основанию. Количественно они оцениваются константой равновесия (К) реакции, заключающейся в переносе протона от кислоты к основанию (протолитическая реакция). Покажем это на примере диссоциации муравьиной кислоты в водном растворе:
| НСООН | + | Н2О |  | НСОО– | + | Н3О+ |
| муравьиная кислота | основание (избыток) | формиат-ион (сопряженное основание) | ион гидроксония (сопряженная кислота) |
Константа равновесия данного процесса равна

Эта константа отличается от обычного выражения константы диссоциации кислоты (Kдисс.), приводимого ранее, множителем 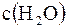 . При рассмотрении диссоциации разных кислот в одном и том же растворителе данный множитель остается одинаковым, поэтому его обычно включают в константу равновесия в виде произведения
. При рассмотрении диссоциации разных кислот в одном и том же растворителе данный множитель остается одинаковым, поэтому его обычно включают в константу равновесия в виде произведения 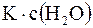 и обозначают Ka (константа кислотности):
и обозначают Ka (константа кислотности):

Чем больше величина Ka, тем сильнее кислота, т.е. тем она легче отдает ионы Н+ основанию (молекулам растворителя). Для оценки силы слабых кислот чаще используют не величину Ka, а ее десятичный логарифм, взятый с обратным знаком:
–lg Ka = pKa
Чем больше значение рKa, тем слабее кислота.
Для количественной характеристики основности соединения в водном растворе служит константа равновесия K реакции:
| :B | + | H2O |  | ВН+ | + | ОН– |
| основание | кислота | сопряженная кислота | сопряженное основание |
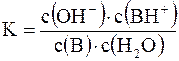
С учетом того, что 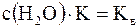 (константа основности), можно записать:
(константа основности), можно записать:
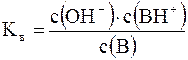
Для оценки силы слабых оснований, как и в случае слабых кислот, также удобнее применять не значение Kв, а ее отрицательный десятичный логарифм:
pKв = –lg Kв
На практике для оценки основных свойств соединения часто вместо Kв (pKв) используют величину Ka (pKa) сопряженной данному основанию кислоты ВН+:
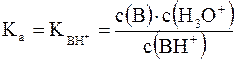
Например, мерой основности NH3 служит величина Ka иона аммония NH4+ (сопряженной аммиаку кислоты):
NH4+ + H2O  NH3 + H3O+
NH3 + H3O+

Чем меньше значение  , тем более сильным является основание.
, тем более сильным является основание.
Для кислоты и сопряженного ей основания в разбавленном водном растворе справедливо равенство:
Kw = Ka · Kв
где Kw – ионное произведение воды.
Кислотные свойства вещества в растворе зависят не только от его способности отдавать ион Н+, но и от способности молекул растворителя его принять. Так, хлороводород при растворении в воде практически полностью распадается на ионы, а его растворы в бензоле, наоборот, не содержат ионов и не проводят электрический ток.
|
|
|
Чем больше у растворителя сродство к протону, тем легче диссоциирует в нем кислота. Растворители с ярко выраженным сродством к ионам Н+ называются протофильными.
В таких растворителях (жидкий NH3, гидразин) даже очень слабые в водных растворах кислоты – HCN, H2S – являются сильными.
Растворители, обладающие гораздо большей способностью к отдаче протона, чем к его присоединению, называются протогенными. К ним относятся: ледяная уксусная кислота, концентрированная (100%) H2SO4 и др. В их среде затрудняется диссоциация кислот, но облегчается ионизация оснований.
Растворители, обладающие сравнимой способностью к присоединению или отдаче ионов Н+, называются амфипротными. К ним относятся Н2О, насыщенные одноатомные спирты (СН3ОН, С2Н5ОН) и т.д.).
Существуют также апротонные или инертные растворители: бензол, толуол, CCl4, дихлорэтан и др. Способность присоединять или отщеплять от себя ион Н+ у них выражена крайне слабо. В их среде кислоты и основания практически не диссоциируют.
Таким образом, в теории кислот и оснований Бренстеда-Лоури понятия кислоты и основания относятся лишь к функции, которую выполняет рассматриваемое соединение в том или ином процессе. Одно и то же вещество может в одних условиях проявлять себя как кислота, а в других – как основание. Например, в водных растворах СН3СООН ведет себя как кислота:
СН3СООН + Н2О  СН3СОО– + Н3О+
СН3СОО– + Н3О+
а в 100% H2SO4 – как основание
СН3СООН + H2SO4  HSO4– + СН3СООН2+
HSO4– + СН3СООН2+
Все реакции кислотно-основного взаимодействия (ионизации, нейтрализации, гидролиза), согласно теории Бренстеда-Лоури, состоят в обратимом переносе протона от кислоты к основанию, вследствие чего их часто называют протолитическими. В результате такого взаимодействия образуется пара новых частиц, одна из которых опять способна отдавать протон (сопряженная кислота), а другая – его присоединять (сопряженное основание). Таким образом кислота оказывается в равновесии с сопряженным основанием, а основание – с сопряженной кислотой:
|
|
|
| НА | + | В |  | ВН+ | + | А– |
| кислота | основание | сопряженная кислота | сопряженное основание |
Данный процесс называется кислотно-основным равновесием. До наступления равновесия он преимущественно протекает в сторону образования более слабой кислоты и основания.
Рассмотрим примеры некоторых протолитических реакций.
1. Реакция ионизации:
| СН3СООН | + | Н2О |  | СН3СОО– | + | Н3О+ |
| кислота | основание | сопряженное основание | сопряженная кислота |
Реакция, протекающая в прямом направлении, является реакцией ионизации уксусной кислоты, а в обратном направлении – реакцией нейтрализации основания (ацетат-иона) кислотой.
Равновесие данного обратимого процесса в значительной степени смещено влево, т.к. СН3СООН и Н2О являются более слабыми кислотой и основанием, чем Н3О+ и СН3СОО– (табл. 13).
2. Реакция гидролиза:
| СН3СОО– | + | Н2О |  | СН3СООН | + | ОH– |
| основание | кислота | сопряженная кислота | сопряженное основание |
Данная прямая реакция является реакцией гидролиза ацетат-иона, а обратная – реакцией нейтрализации уксусной кислоты сильным основанием ОН–.
Более слабыми кислотой и основанием являются Н2О и СН3СОО– (табл. 13) и поэтому в данном обратимом процессе обратная реакция превалирует над прямой.
Таблица 13. Значения рKa и pKв сопряженных кислот и оснований в разбавленных водных растворах
| Кислота | рKa | Сопряженное основание | pKв |
| H3O+ | –1,74 | H2O | 15,74 |
| HNO3 | –1,32 | NO3– | 15,32 |
| H2C2O4 | 1,26 | HC2O4– | 12,74 |
| H2SO3 | 1,92 | HSO3– | 12,08 |
| H3PO4 | 2,12 | H2PO4– | 11,88 |
| HF | 3,14 | F– | 10,86 |
| CH3COOH | 4,76 | CH3COO– | 9,24 |
| H2S | 7,05 | HS– | 6,95 |
| NH4+ | 9,25 | NH3 | 4,75 |
| HCN | 9,22 | CN– | 4,78 |
| H2O | 15,74 | OH– | –1,74 |
Теория Бренстеда-Лоури хоть и является более совершенной, чем теория Аррениуса, однако тоже имеет определенные недостатки, и не является всеобъемлющей. Так, она не применима ко многим веществам, проявляющим функцию кислоты, но не содержащим в своем составе ионов Н+, например: BCl3, AlCl3, BF3, FeCl3 и др.
В 1923 г. Г.Н. Льюисом была выдвинута электронная теория кислот и оснований, в которой кислотные свойства соединения вообще не связываются с наличием в нем ионов водорода.

Гильберт Нильтон Льюис (1875 – 1946). Американский физикохимик. Его работы связаны с химической термодинамикой и теорией строения вещества. Ввел в термодинамике понятие активности, разработал теорию обобщенных электронных пар в моделях ковалентной связи (структуры Льюиса). В 1926 г. практически одновременно с Бренстедом и Лоури предложил новую концепцию кислот и оснований, в которой основой является передача электронной пары: кислоты Льюиса – акцепторы, а основания Льюиса – доноры электронной пары. В 1930-х гг. Льюис разработал метод получения тяжелой воды.
Кислотой по Льюису является частица (молекула или ион), способная присоединять электронную пару (акцептор электронной пары). Она должна содержать в своем составе атом с незаполненной до октета внешней электронной оболочкой: BF3, AlCl3, BeCl2, H+, Cu2+ и т.д.
Основанием является частица (молекула или ион), способная предоставлять для образования связи электронную пару (донор электронной пары). Основание по Льюису должно содержать в своем составе атом с неподеленной электронной парой на внешнем слое::NH3,:NH2 – NH2,:OH–,:Cl–.
Согласно теории Льюиса, кислота и основание взаимодействуют друг с другом с образованием ковалентной связи по донорно-акцепторному механизму:
 А А | + | :В | → |  А: В А: В |
| кислота | основание | кислотно-основной комплекс |
 BF3 BF3 | + | :NH3 | → |  F3B: NH3 F3B: NH3 |
| кислота | основание |
 H+ H+ | + | Н2О: | → | Н3О+ |
| кислота | основание |
Теория Льюиса не противоречит теории Бренстеда-Лоури. Понятие основания в обеих этих теориях практически совпадает, однако понятие кислоты в концепции Льюиса значительно шире и охватывает, кроме иона Н+, многие другие электронноакцепторные частицы, в том числе и катионы металлов Men+. Соответственно, значительно увеличивается и число реакций, которые по своему характеру относятся к кислотно-основному взаимодействию. Так, например, согласно теории Льюиса, кислотно-основными являются многочисленные реакции комплексообразования:
| Cu2+ | + | 4NН3 | → | [Cu(NН3)4]2+ |
| кислота | основание |
Теория Льюиса широко используется для объяснения реакционной способности органических соединений и очень удобна при описании механизма химических реакций, протекающих с их участием.
Определение буферных систем и их классификация
Многие реакции в растворе протекают в нужном направлении только при определенной концентрации ионов Н+. Изменение её в ту или иную сторону от соответствующего оптимального значения приводит к появлению новых, часто нежелательных продуктов. В связи с этим, поддержание постоянного значения рН на протяжении всего времени осуществления реакции часто является важным условием ее успешного завершения.
Особенно актуально это для биохимических процессов, протекающих в живых организмах. Большинство из них катализируется различными ферментами или гормонами, проявляющими свою биологическую активность только в строго определенном и достаточно узком интервале значений рН.
Растворы, способные сохранять постоянной концентрацию ионов Н+ при добавлении к ним небольших количеств сильной кислоты или щелочи, а также при разбавлении, называются буферными растворами или буферными системами.
Свойство данных растворов сохранять неизменным присущее им значение рН при вышеперечисленных обстоятельствах называется иначе буферным действием.
Буферные растворы в зависимости от своего состава делятся на 2 основных типа: кислотные и основные.
Кислотные буферные системы обычно образованы слабой неорганической или органической кислотой и солью этой же кислоты с сильным основанием. Например:
| 1) | СН3СООН | + | СН3СООNa | – | ацетатный буфер |
| слабая кислота | соль кислоты |
| 2) | Н2СО3(Н2О + СО2) | + | NaНСО3 | – | гидрокарбонатный или бикарбонатный буфер |
| слабая кислота | соль кислоты |
С точки зрения теории Бренстеда-Лоури, кислотной буферной системой является равновесная смесь слабой кислоты и сопряженного ей основания. Причем роль сопряженного основания играют образующиеся при диссоциации солей анионы слабых кислот. В связи с этим состав буферных растворов можно записать иначе:
| 1) | СН3СООН | / | СН3СОО– | – | ацетатный буфер |
| слабая кислота | сопряженное основание |
| 2) | Н2СО3(Н2О + СО2) | / | НСО3– | – | гидрокарбонатный буфер |
| слабая кислота | сопряженное основание |
Кислотная буферная система может быть образована и смесью двух солей многоосновной кислоты, соответствующих различным стадиям нейтрализации этой кислоты. В таком случае кислотный остаток одной из солей (менее замещенный) играет роль слабой кислоты, а кислотный остаток второй соли (более замещенный) – сопряженного ей основания.
Примером таких систем могут служить:
1) карбонатная буферная система, представляющая собой смесь кислой (NaHCO3) и средней (Na2CO3) солей угольной кислоты
| HCO3– | / | СО32– |
| слабая кислота | сопряженное основание |
2) фосфатные буферные растворы
| NaH2PO4 + Na2HPO4 | (H2PO4– | / | HPO42– |
| слабая кислота | сопряженное основание |
| Na2HPO4 + Na3PO4 | (HPO42– | / | PO43– |
| слабая кислота | сопряженное основание |
Следует отметить, что не только смеси, но и растворы некоторых индивидуальных солей (например: тетрабората натрия (Na2B4O7), карбоната аммония ((NH4)2CO3) и др.) тоже обладают буферными свойствами, которые объясняются сильным гидролизом этих солей и образованием вследствие этого компонентов, необходимых для буферного действия:
(NH4)2CO3 + HOH  NH4HCO3 + NH3 × H2О
NH4HCO3 + NH3 × H2О
Оснóвные буферные системы образованы слабым неорганическим или органическим основанием и солью этого основания с сильной кислотой. Например:
| 1) | NH3 · H2O | + | NH4Cl | – аммиачный буфер |
| слабое основание | соль |
| 2) | C2H5–NH2 × H2О | + | C2H5NH3Cl | – этиламиновый буфер |
| слабое основание | соль |
С точки зрения теории Бренстеда-Лоури, оснóвная буферная система также представляет собой равновесную смесь слабой кислоты и сопряженного ей основания, только роль кислоты в данном случае выполняет образующийся при диссоциации соли катион:
| 1) | NH4+ | / | NH3 × H2О | – аммиачный буфер |
| слабая кислота | сопряженное основание |
| 2) | C2H5–NH3+ | / | C2H5–NH2 × H2О | – этиламиновый буфер |
| слабая кислота | сопряженное основание |
Определенным буферным действием обладают также и растворы многих органических веществ, молекулы которых одновременно содержат в своем составе функциональные группы, проявляющие как слабые кислотные (СООН-группы), так и оснóвные (NH2-группы) свойства. По своей природе данные соединения являются амфолитами. К ним относятся аминокислоты, белки, пептиды.
 2014-02-02
2014-02-02 4182
4182








