Пептиды-продукты взаим-ия АМК. Образуются либо при гидролизе белков, либо много пептидов, облад-их биол.активностью. N-концевая АМК амидная связь.







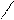
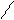 O H O O H O
O H O O H O







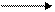

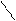
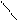
 H2N-CH-C + H-N-CH-C H2N-CH-C-N-CH-CH-C
H2N-CH-C + H-N-CH-C H2N-CH-C-N-CH-CH-C
 CH3 OH CH2OH OH -H2O CH3 CH3OH OH С-кольц.АМК
CH3 OH CH2OH OH -H2O CH3 CH3OH OH С-кольц.АМК
Аланин сирин аланилсерин
N-концевая (не участв.в об-ие пептид.связи)
COOH-не уч-ет в об-ие пептид.связи.
 Строение пептидной группы
Строение пептидной группы

 R2 H
R2 H

 Cl N
Cl N





 C C2
C C2
O R2 H пептидная связь яв-ся плоской копланарной
Неопределенная пара е-атома N нах-ся в сопряжении с П-связью карбонильной группы в р-те чего связь с-N укорачивается и имеет характер двойной связи, вокруг α-ой нет свободного вращения.
П,р-сопряж.





 O O O-
O O O-






 -C-N- -C=N- C=N+-
-C-N- -C=N- C=N+-
H H H Благодаря наличию электронного резонанса возможно об-ие водор.связей, и возможно сущ-ие цис и транс изомеров. В природных пептидах и белках встречается транс расп-ие радикалов.
Химический метод синтеза пептидов(классич)
При обычном смещении 2-х АМК возможны след.затруднения:
1. Из-за диполярной структуры проведение реак.требует высоких температур, что приводит к побочным продуктам(дикетопиперацин)
2. АМК необходимо соед-ть в строгой опред-ой последовательности
 Классич.метод всключает несколько стадий:
Классич.метод всключает несколько стадий:
1. Защита аминогруппы N-канцевой АМК чаще используют реак.ацилирования след.реагентами:
O O
С6H5CH2O-C бензоксикарбонихлорид;(CH3)3COC
Cl N3


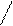
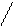 Третбутоксикарбоксазид O O
Третбутоксикарбоксазид O O

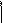
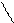
 H2N-CH-COOH+C6H5CH2O-C C6H5CH2OC-NH-CH-COOH
H2N-CH-COOH+C6H5CH2O-C C6H5CH2OC-NH-CH-COOH
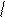
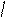 CH3 Cl -HCl CH3 O
CH3 Cl -HCl CH3 O
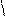 2. Активация карбоксильной группы, N-защищенной АМК. Для актив.исп-ют либо PCl5, либо SOCl2, C2H5O-C
2. Активация карбоксильной группы, N-защищенной АМК. Для актив.исп-ют либо PCl5, либо SOCl2, C2H5O-C
ЭтилхлорформиатCl
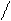
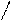



 O O O
O O O
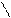
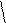 C6H5CH2OC–NH–CH–COOH+SOCl2®C6H5CH2OC–NH–CH–C + SO2 +HCl
C6H5CH2OC–NH–CH–COOH+SOCl2®C6H5CH2OC–NH–CH–C + SO2 +HCl
CH3 CH3
3. Защита карб-ой гр, С-канцевой АМК.
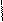
 H2N-CH-COOH + C2H5OH F H2N-CH-COOC2H5+H2O
H2N-CH-COOH + C2H5OH F H2N-CH-COOC2H5+H2O
CH2OH CH2OH


 4.Синтез
4.Синтез









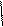 O O O CH3 O H
O O O CH3 O H

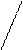
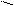
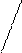
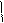
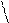
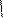 C6H5CH2OC–NH–CH–C + HNH–CH–COOC2H5®C6H5CH2OC–NH–CH–C–N–CH–COOC2H5
C6H5CH2OC–NH–CH–C + HNH–CH–COOC2H5®C6H5CH2OC–NH–CH–C–N–CH–COOC2H5
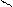 CH3 Cl CH2OH
CH3 Cl CH2OH
5-6. Снятие защиты с N и С концов.



 O O O
O O O
 С6H5-CH2O-C-NH-CH-C-N-CH-C
С6H5-CH2O-C-NH-CH-C-N-CH-C
CH3 CH2OH OC2H5

 H2 P H2O,OH-
H2 P H2O,OH-
C6H5CH3 -C2H5OH


 O H
O H

 H2N-CH-C-N-CH-COOH
H2N-CH-C-N-CH-COOH
CH3 CH2OH
Твердофазный синтез пептидов (ТФСП)
Полипептидная цепь наращивается на тв.основе без выделения промеж.продуктов.

 O
O


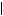



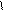
 смола –СH2Cl + HOOCCH-NH2 ® смола CH2OC-CH-NH2
смола –СH2Cl + HOOCCH-NH2 ® смола CH2OC-CH-NH2

 R -HCl R
R -HCl R
На конце свободная аминогруппа ацилир-ся след.АМК, у α-ой защищена аминогр.(бок-группы) в присутствии активатора карбоксильной группы N-N’, где карбоксил N-N- дициклогексилкарбодисемид.

 O
O


 -СH2OCCH-NH2+HOOC-CH-NHБОК + C6H5N=C=N-C6H11
-СH2OCCH-NH2+HOOC-CH-NHБОК + C6H5N=C=N-C6H11
R R (ДЦГК)



 O O
O O




 ® CH2OCCH-NH-C-CHNHБОК+C6H11NH—C-NHC6H11
® CH2OCCH-NH-C-CHNHБОК+C6H11NH—C-NHC6H11
R R’ O дициклогексилмочевина
Далее удаляют защиту действ.3-фторуксус.к-ты, пролив-ют от избыт.реагентов и побочных продуктов. Таким образом конденсируются и след.АМК.
После присоед. послед. Кисл. остатка и снятия защиты обрабатывают бромоводор.к-ой ® в р-те полипептид отдел. От полимера.
Все стадии автоматизированы.
 2014-02-02
2014-02-02 947
947








