РОЛЬ ЛЕЙКОЦИТОВ В ГЕМОСТАЗЕ
Ретракция сгустка крови
Процесс агрегации заключается в присоединении активированных тромбоцитов, находящихся в токе крови, друг к другу и ранее фиксированным в области повреждения. Основным рецептором агрегации является GPIIb-IIIa (интег-рин αIIbβ3). После активации тромбоцита GPIIb-IIIa значительно повышает свою аффинность по отношению к фибрину и меняет антигенную структуру (что свидетельствует о значительных кон-
формационных изменениях). После этого происходит соединение тромбоцитов, опосредованное фибрином и фактором Виллебранда (рис. 24).
Вследствие распространения активирующего сигнала на агрегированные тромбоциты, удаленные от места повреждения, образуется толстый слой тромбоцитов, армированный фибрином. Этот процесс лежит в основе образования тром-боцитарного тромба. По мере удаления от зоны
Тромбоциты
повреждения концентрация агонистов активации и агрегации тромбоцитов снижается и соответственно уменьшается активация тромбоцитов. Дистально расположенные частично активированные тромбоциты отрываются от сгустка и возвращаются в кровоток. Таким образом, периферическая дезагрегация тромбоцитов предотвращает неограниченный рост сгустка.
Ретракцией сгустка крови называют уплотнение сгустка с выделением из него избытка сыворотки. Ретракция способствует улучшению механических характеристик сгустка и снижению ак-
тивности фибринолиза внутри него. Ретракция сгустка связана с контрактильными свойствами тромбоцитов. Фибриллы миозина, расположенные в цитоплазме тромбоцитов, фиксированы к мембранному гликопротеину GPIIb-IIIa. В активированных тромбоцитах за счет миозина происходит процесс постепенного «сжимания» цитоплазмы, что приводит к уплотнению всего сгустка крови.
При врожденной недостаточности GPIIb-IIIa -тромбастении Гланцмана - грубо нарушается ретракция сгустка крови. Следствием этого является не только грубый дефект тромбоцитарного гемостаза, но и качественный дефект образовавшегося сгустка крови.
Роль лейкоцитов в гемостазе
Лейкоциты (нейтрофилы и моноциты) в зоне повреждения сосуда участвуют в гемостатических реакциях.
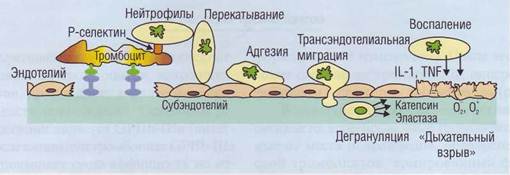
Агрегация тромбоцитов сопровождается освобождением из α-гранул активаторного рецептора Р-селектина (CD62), который остается ассоциированным с плазматической мембраной тромбоцитов. Экспрессия на мембране лейкоцитов Р-селек-тин-связывающего гликопротеина-1 (PSGL-1) позволяет нейтрофилам присоединять тромбоциты (рис. 29). Связь нейтрофилов с тромбоцитами обеспечивает репаративные и воспалительные реакции, возникающие в ответ на повреждение.
Нейтрофилы после связывания на мембранах способны секретировать адгезивные молекулы и интерлейкины. Некоторые из интерлей-кинов, в частности интерлейкин-1 (ИЛ-1) и фактор некроза опухоли-ос (ФНО-а), активируют эндотелиальные клетки. Первичный контакт гранулоцитов приводит к перемещению их вдоль сосудистой стенки с последующей транс-эндотелиальной миграцией в субэндотелий. При действии повреждающих факторов, таких, как иммунные комплексы, эндотоксин, гранулоци-
ты могут дегранулироваться и освобождать ИЛ-1, ФНО-α, протеолитические ферменты, такие, как эластаза и катепсин, активные формы кислорода (О2-, О2+), что в свою очередь ведет к повреждению сосудистой стенки. Этот процесс доминирует при воспалительных реакциях. Протеолитические ферменты, которые освобождаются из лейкоцитов, в участках воспаления вызывают нарушения структуры и функции эндотелия, это является условием развития петехий.
Роль нейтрофилов в модуляции реакций гемостаза требует уточнения. С одной стороны, экспрессия тканевого фактора на мембране нейтрофилов происходит либо при длительной стимуляции различными провоспалительными цитокинами, либо после длительного взаимодействия с Р-селектином активированных тромбоцитов. К этому времени на активированных тромбоцитах уже образуется сгусток крови. С другой стороны, экспериментально доказано моду-
 2014-02-17
2014-02-17 991
991








