Суспензии для инъекций. Суспензии для инъекций должны иметь не только химическую, но и физическую стабильность. Физическая стабильность определяется способностью гетерогенных систем оставаться в высокодисперсном состоянии на протяжении установленного срока хранения. Поэтому в их состав, при необходимости, вводят стабилизаторы. Сложной технологической задачей при приготовлении суспензий для инъекций является выбор метода стерилизации, так как при высокой температуре в суспензиях может происходить укрупнение размера частиц дисперсной фазы. В связи с этим суспензии для парентерального применения, как правило, приготавливают из стерильных порошков (если они выдерживают стерилизацию) непосредственно перед введением (в асептических условиях). В промышленных условиях используют также методы стерилизации, которые обеспечивают физическую стабильность лекарственной формы. В настоящее время в виде суспензий для инъекций производятся кортизона ацетат 2,5 % во флаконах по 10 мл, гидрокортизона ацетат 2,5 % в ампулах по 2 мл и др.
|
|
|
Примером экстемпоральной прописи суспензий для парентерального применения может являться следующая:
Rp.: Streptocidi 6,0
Olei Persicorum 30,0 pro injectionibus
Misce. Da. Signa. Для внутримышечных инъекций
При нагревании взвесей происходит укрупнение дисперсной фазы. В связи с этим их готовят с использованием простерилизованных ингредиентов в асептических условиях.
В сухой стерильный флакон фильтруют 30,0 г масла персикового и стерилизуют в сушильном шкафу при 180—200 °С в течение 15— 30 минут. В стерильной ступке тщательно растирают 6,0 г стрептоцида (предварительно простерилизованного) с 30 каплями спирта этилового (трудноизмельчаемое вещество) до максимальной мелкости и в асептических условиях смешивают с 3,0 г (половинное количество от стрептоцида) масла стерильного до получения однородной взвеси. Далее смесь разбавляют оставшимся количеством масла и переносят в стерильный флакон с притертой пробкой.
Эмульсии для парентерального питания > Эмульсии для парентерального питания — это высокодисперсные гетерогенные системы, содержащие нейтральные жиры в водной среде.
Эмульсии для парентерального питания играют важную роль в организме: они включаются в обменные процессы, являясь при этом богатым источником энергии. По сравнению с другими препаратами они имеют более высокую калорийность при уменьшенном объеме жидкости, осмотическую неактивность, высокое содержание полиненасыщенных жирных кислот, малую степень выведения субстрата с мочой и калом.
Лекарственные препараты в форме жировых эмульсий не должны проявлять гемолитическую активность, токсичность и пироген-ность.
|
|
|
В медицинской практике наиболее часто используются такие жировые эмульсии: «Интралипид» (Швейцария), «Венолипид» (Япония) и др. Широкое применение находят эмульсии антигемолитического действия, содержащие фосфатидил-этаноламин; эмульсии на основе фторуглеродных соединений, используемые для переноса кислорода.
Отечественная фармацевтическая промышленность (Львовский НИИ гематологии и переливания крови) выпускает препарат «Ли-пидин», представляющий собой 20 % эмульсию подсолнечного масла, стабилизированную 1 % растительным фосфатидилхолином.
Оптимальный размер частиц в эмульсиях для парентерального питания должен быть не более 0,8—1 мкм. Получение эмульсий с заданной величиной частиц осуществляется с помощью методов механического и ультразвукового диспергирования.
В технологии эмульсий для парентерального питания важное значение имеет подбор количества эмульгаторов, порядок смешивания компонентов, рН системы и ее температура, выбор метода стерилизации.
Для приготовления жировых эмульсий используют жиры животного и растительного происхождения. Предпочтительнее использовать растительные масла (соевое, хлопковое, подсолнечное, кунжутное). В качестве эмульгаторов часто используют фосфолипиды, выделенные из яичного желтка и мозга крупного рогатого скота (фос-фатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, сфин-гомиелин). Эмульгаторы подбираются с учетом состава эмульсии и концентрации нейтральных жиров.
Термический метод стерилизации отрицательно сказывается на стабильности и сохранности препаратов. Более приемлемым является метод стерилизации ультрафильтрацией через мембранные фильтры.
Технологические стадии приготовления эмульсий для парентерального питания более подробно рассматриваются в курсе промышленной технологии лекарств.
ХРАНЕНИЕ И ОТПУСК ИНЪЕКЦИОННЫХ ЛЕКАРСТВЕННЫХ ФОРМ
Хранить приготовленные лекарственные препараты для инъекционного введения необходимо при условиях, которые исключают возможность их загрязнения. Места хранения должны быть отдалены от лифтов, санузлов, мест приема и распаковки товаров, использованной тары и оборудованные столами или стеллажами.
Отпуск лекарственных препаратов из аптек лечебно-профилактическим учреждениям необходимо проводить только при соблюдении режимов, исключающих их загрязнение в процессе транспортировки, то есть в чистую маркированную тару (ящики, легко поддающиеся дезобработке).
Приготовленные в аптеках растворы для инъекций, укупоренные «под обкатку» в соответствии с приказом № 96 МЗ СССР от 3.04.91 г (приложение 2), имеют срок годности от 7 до 30 суток, все остальные — не более 2 суток.
Структурно-логическая схема технологии и контроля качества растворов для инъекций приведена на схеме 17.
СОВЕРШЕНСТВОВАНИЕ ТЕХНОЛОГИИ
ИНЪЕКЦИОННЫХ ЛЕКАРСТВЕННЫХ ФОРМ
Проводимые исследования в области совершенствования технологии инъекционных лекарственных форм направлены на повышение эффективности и качества продукции, что требует решения основных проблем, — это стабилизация, обеспечение отсутствия механических примесей в препаратах, оптимизация процесса получения и его аппаратурного оснащения.
В настоящее время широкое распространение получил химический метод стабилизации, предусматривающий прибавление различных вспомогательных веществ-стабилизаторов к лекарственным препаратам, что не является оптимальным способом получения стабильных лекарств с биологической точки зрения. Заслуживает внимания физический, вернее технологический способ стабилизации, позволяющий получить стойкие препараты без прибавления каких-либо вспомогательных веществ-стабилизаторов. С биологической точки зрения физический способ стабилизации наиболее рациональный и требует значительного расширения исследований в этом направлении.
|
|
|
Так, в США широко развивается производство замороженных ин-фузионных растворов (цефалоспориновых антибиотиков и антибиотиков других групп). Эти растворы готовят в 0,9 %-ном растворе натрия хлорида или 5 %-ном растворе глюкозы и выпускают в специальных полимерных контейнерах вместимостью 50 или 100 мл.
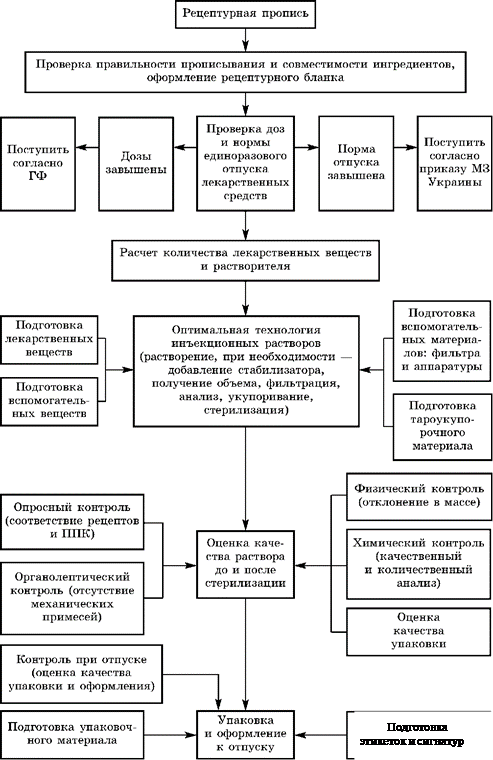
СТРУКТУРНО-ЛОГИЧЕСКАЯ СХЕМА ТЕХНОЛОГИИ И КОНТРОЛЯ КАЧЕСТВА РАСТВОРОВ ДЛЯ ИНЪЕКЦИЙ
Срок годности таких растворов 6 месяцев при хранении при температуре не выше минус 20 °С.
Одним из направлений совершенствования технологии инфузи-онных препаратов в отношении обеспечения стабильности является разработка методов создания водных растворов из труднорастворимых субстанций. Особое внимание привлекают комбинированные, инфузионные и полиионные препараты, требующие изучения вопросов совместимости и стабильности. Перспективным является производство концентрированных растворов (концентратов), порошков и лиофилизированных лекарственных форм для инъекций.
Концентраты для внутривенных инъекций представляют собой стерильные растворы, предназначенные для применения после разведения до указанного объема соответствующей жидкостью. Порошки и лиофилизированные лекарственные формы при встряхивании с указанным объемом соответствующей стерильной жидкости образуют прозрачный, свободный от механических частиц раствор.
Эти лекарственные формы должны соответствовать всем требованиям, предъявляемым к инъекционным препаратам.
В настоящее время развивается направление применения аминокислотных инфузионных растворов в сочетании с растворами глюкозы, жировыми эмульсиями.
Важной проблемой является оптимизация технологического процесса получения инъекционных лекарственных форм и совершенствования оборудования. Процесс получения, фильтрования, разлива во флаконы, укупорки инъекционных препаратов необходимо проводить в условиях «чистых комнат». Решение проблемы обеспечения отсутствия механических примесей в инъекционных препаратах осуществляется созданием эффективных фильтров, а также совершенствованием методов контроля качества фильтрата. Контроль фильтрата и раствора во флаконах в основном осуществляется визуально. За рубежом используются системы автоматического контроля чистоты растворов (Япония). В нашей стране разработана установка для контроля чистоты фильтрата по частичкам величиной 2—5 мкм и более.
|
|
|
Комплексное решение основных проблем с учетом других факторов, влияющих на стабильность препаратов, позволит получить стабильные инъекционные лекарственные формы высокого качества.
Глава 26
ГЛАЗНЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ
ХАРАКТЕРИСТИКА ГЛАЗНЫХ
ЛЕКАРСТВЕННЫХ ФОРМ
В практической офтальмологии для лечения глазных заболеваний применяют инстилляцию растворов, закладывание в конъюнк-тивальный мешок мазей, глазных пленок, таблеток, ламелей, инъекционное введение лекарственных веществ, а также с помощью контактных линз и электрофореза. Перечисленным путям введения офтальмологических лекарственных препаратов соответствует и многообразие лекарственных форм: твердых, жидких, мягких и газообразных.
К твердым глазным лекарственным формам относятся: таблетки, ламели, карандаши, присыпки, глазные лекарственные пленки; к газообразным — аэрозоли (глазные спреи); к мягким — мази гомогенные и гетерогенные; к жидким — истинные водные и масляные растворы, растворы ВМС, коллоидные растворы, эмульсии и суспензии. Они применяются в виде глазных капель, примочек, промываний, растворов для инъекций и электрофореза.
Вид лекарственной формы в офтальмологической фармакотерапии определяется целым рядом взаимосвязанных факторов: состоянием патологического процесса, общими показателями состояния организма больного, наличием соответствующих травматических повреждений органа зрения, степенью проницаемости гематоофталь-мологического барьера, физико-химическими свойствами лекарственных веществ, особенностями фармакологического действия лекарственных и вспомогательных веществ и др. Значительная роль в процессах активизации или ингибирования действия лекарственных веществ принадлежит и таким факторам, как величина рН, осмотическое давление раствора, молекулярная масса веществ-носителей и т. п. Для приготовления глазных лекарственных форм высокого качества необходимо учитывать указанные факторы.
В экстемпоральной рецептуре аптек наиболее часто приготовляются глазные капли, примочки и мази.
ГЛАЗНЫЕ КАПЛИ (GUTTAE OPHTALMICAE)
Ш Глазные капли — это жидкие лекарственные формы, представляющие собой водные или масляные растворы, а также тончайшие суспензии лекарственных веществ, предназначенные для инстилляции в глаз.
Наносят их на слизистую оболочку глаза с помощью стерильной глазной пипетки. Глазные капли прописывают в небольших количествах (5—10 мл) с расчетом их использования в течение непродолжительного времени.
В виде глазных капель применяют растворы различных лекарственных веществ. Многие из них нестойки и изменяются или разрушаются под влиянием высокой температуры, солнечного света, микрофлоры и других факторов.
Особенно часто назначают глазные капли с витаминами (кислотой аскорбиновой, тиамина бромидом, рибофлавином), солями алкалоидов (атропина сульфатом, пилокарпина гидрохлоридом и др.), антибиотиками (бензилпенициллином, левомицетином, неомицином и др.), цинка сульфатом, кислотой борной, натрия-сульфацилом. В настоящее время насчитывается около 80 лекарственных веществ, применяемых в глазной практике, и значительное количество разнообразных их сочетаний.
Требования, предъявляемые к глазным каплям. Низкое качество глазных капель и, в первую очередь, загрязнение их микроорганизмами может вызвать тяжелые последствия вплоть до потери зрения.
В связи с этим требования, предъявляемые к глазным каплям, должны быть аналогичны тем, которые предусмотрены для инъекционных растворов: стерильность, отсутствие механических примесей, стабильность, комфортность, (изотоничность, оптимальное значение рН), пролонгированность действия.
Стерильность. Глазные капли, а также концентрированные растворы, применяемые для их приготовления, должны приготовляться в асептических условиях с последующей стерилизацией.
Способ стерилизации глазных капель зависит от устойчивости лекарственных веществ в растворах к температурному воздействию. По этому признаку лекарственные вещества можно разделить на три группы:
1.Лекарственные вещества, растворы которых могут подвергаться тепловой стерилизации без добавления стабилизаторов (кислота борная, кислота никотиновая, натрия хлорид, фурацилин и др.).
2. Лекарственные вещества, растворы которых могут подвергаться тепловой стерилизации после добавления стабилизаторов (суль-фацил-натрия, этилморфина гидрохлорид, физостигмина салицилат, ПАС-натрий, салюзид растворимый и др.).
З.Лекарственные вещества, растворы которых не выдерживают тепловой стерилизации (протаргол, колларгол, лидаза, химопсин, трипсин, пенициллин и др.) и приготавливаются асептически без последующей стерилизации.
В асептических условиях также готовятся растворы лекарственных веществ, режимы стерилизации которых не разработаны.
Глазные капли могут содержать консерванты, буферные растворы, пролонгаторы. Консервирование глазных капель предусматривает предупреждение развития микроорганизмов в лекарственной форме в процессе ее хранения и использования.
Механизм действия консервантов сводится к нарушению клеточной мембраны, коагуляции белка, блокированию свободных сульфгидрильных групп, химическому антагонизму. Характеристика консервантов и требования, предъявляемые к ним, приведены на с. 481—484.
В офтальмологических лекарственных формах используется ограниченный их ассортимент. Так, из неорганических консервантов чаще используется кислота борная в концентрации 1,9—2 % с рН около 5,0 (оптимальный рН офтальмологических растворов 4,5—9,0). Кроме того, кислота борная обладает буферными свойствами, предупреждает изменение рН раствора при добавлении в него лекарственного вещества, особенно из группы алкалоидов, дающих в растворах кислую среду (рН ниже 4,0).
Из органических консервантов практическое значение имеют спирт Р-фенилэтиловый — 0,3—0,5%, спирт бензиловый — 0,9%, сложные эфиры кислоты п-гидроксибензойной: нипагин — 0,05— 0,23 %, нипазол — 0,03—0,08 % или их смесь (нипагина — 0,18 %, нипазола — 0,02 %), левомицетин 0,15 %, соли четвертичных аммониевых оснований (бензалкония хлорид, цетилпиридиния хлорид, додецилдиметилбензиламмония хлорид) в концентрации 1:10000.
Из кислот нашла применение сорбиновая кислота, которая не оказывает раздражающего и аллергического действия на кожу и слизистые оболочки. Наиболее эффективна при рН = 3,0—4,0; обладает очень сильным фунгицидным свойством, применяется в концентрации 0,05—0,2 %.
Из металлорганических консервантов представляет интерес эта-нолмеркурия хлорид 0,01 % и мертиолат 0,005 %.
Консерванты добавляются в лекарственную форму перед стерилизацией раствора. Вследствие малой растворимости нипагин и ни-пазол растворяют в горячей воде при температуре 30—90 °С и энергичном взбалтывании.
Цетилпиридиния хлорид при взбалтывании в воде дает обильную пену, поэтому растворять его необходимо в части воды и осторожно (желательно при температуре воды около 50 °С).
Стабильность. В глазных каплях должна быть обеспечена устойчивость лекарственных веществ. Тепловая стерилизация и длительное хранение глазных растворов в стеклянной таре ведут к разрушению многих лекарственных веществ (алкалоидов, анестетиков и др.) вследствие гидролиза, окисления и т. д. Поэтому при приготовлении глазных капель и особенно при их стерилизации большое внимание должно быть уделено химической устойчивости стекла, так как щелочное стекло (наличие силиката натрия) придает воде щелочную реакцию, при стерилизации рН может достигать 10,0. Скорость разрушения препаратов зависит не только от температуры стерилизации, но и в значительной степени от рН среды.
Для сохранения стабильности большинство растворов требуют низкого значения рН (около 5,0). Исходя из этого, возникает необходимость приготовления глазных капель на буферных растворителях. При использовании буферных растворов достигается повышение химической стабильности, терапевтической активности, а также уменьшение раздражающего действия глазных растворов. Рекомендуется в качестве растворителей для приготовлении глазных капель применять стерильные изотонические растворы, обладающие консервирующими и буферными свойствами. Но эти растворы можно применять только по указанию врача.
Выбор буферного растворителя зависит от физико-химических свойств лекарственного вещества. По этому признаку их можно разделить на две группы: к первой группе относятся препараты, в растворах которых должно поддерживаться рН около 5,0. В этом случае рекомендуется использовать изотонический раствор кислоты борной (концентрация 1,9%), рН которого ниже 5,0. Раствор при этом обладает малой кислотностью, хорошо нейтрализует щелочь, которая извлекается из стекла. В то же время кислота борная нейтрализуется и поэтому не вызывает чувства боли. Такой буферный растворитель рекомендуется при приготовлении растворов: пилокарпина гидрохлорида, дикаина, совкаина, мезатона и солей цинка. Глазные капли, приготовленные на 1,9 %-ном растворе кислоты борной, могут автоклавироваться при 100 °С в течение 15 минут.
Ко второй группе относятся лекарственные вещества, в растворах которых должно поддерживаться рН около 6,8. В этом случае рекомендуется фосфатный буфер с рН = 6,8, изотонированный хлоридом натрия. Состав буфера:
Раствора однозамещенного фосфата натрия 0,8 % — 30 мл
Раствора двузамещенного фосфата натрия 0,94 % — 70 мл
Натрия хлорида — 0,43 г
На таком фосфатном буфере можно готовить растворы солей атропина, пилокарпина и скополамина. Для этих же препаратов применяют и боратный буфер следующего состава:
Кислоты борной — 1,84 г
Натрия тетрабората — 0,14 г
Воды очищенной (рН = 6,8) — 100 мл
Однако его можно использовать только при приготовлении глазных капель ex tempore, так как стабильность медикаментов в нем сохраняется в течение 5—10 суток.
Существует также боратно-ацетатный (1,9 %-ный раствор кислоты борной и 1,5 % раствор натрия ацетата) и боратно-пропионатный (1,9 %-ный раствор кислоты борной и 2 % раствор натрия пропиона-та) буферные растворы. Приготовление глазных капель с использованием буферных растворителей проводится путем выбора такого буферного раствора, состав и рН которого обеспечивал бы стабильность лекарственного препарата.
Стабилизация легкоокисляющихся солей физостигмина салици-лата и адреналина гидрохлорида в глазных каплях осуществляется добавлением антиоксидантов (натрия сульфита, натрия метабисуль-фита и др.). Для повышения стабильности 10, 20 и З0 %-ных растворов сульфацила натрия рекомендуется добавлять соответственно 1,0; 3,0; 5,0 г натрия метабисульфита и 5, 17 и 18 мл 0,1М раствора натрия гидроксида на 1 л раствора соответственно.
Раствор стерилизуют при 100 °С 30 минут. Упаковывают во флаконы под обкатку. В герметической упаковке раствор сохраняет стабильность в течение 18 месяцев.
Растворы сульфацил-натрия 10, 20 и 30 %, предназначенные для инстилляции взрослым, а также новорожденным детям для профилактики гонобленореи, могут быть приготовлены по следующей прописи:
Сульфацила-натрия 100,0; 200,0; 300,0 г
Натрия тиосульфата 1,5 г
Раствора кислоты
хлористоводородной 1М 3,5 мл
Воды очищенной до 1 л
Флаконы укупоривают под обкатку, стерилизуют при 120 °С 8 минут. Значение рН раствора 7,5—8,5. Препарат стабилен в течение 1 месяца.
При приготовлении глазных капель в стерильной полимерной упаковке (тюбиках-капельницах) в качестве стабилизатора добавляют 0,15 г натрия тиосульфата и 3,5 мл 1М раствора кислоты хлористоводородной на 1 л раствора.
Раствор кислоты аскорбиновой 2 %-ный стабилизируют добавлением натрия метабисульфита (0,1 %) или натрия сульфита безводного (0,2 %). В случае приготовления внутриаптечных заготовок вода насыщается углекислым газом. Очень часто рН растворов кислоты аскорбиновой имеет низкое значение рН (2,9—3,2), что вызывает у больного неприятные ощущения. Для их устранения излишняя кислотность нейтрализуется добавлением натрия гидрокарбоната до рН раствора 6,6—7,1.
Глазные капли — 0,02 %-ный раствор рибофлавина в комбинации с 2 % калия йодида и 2 % глюкозы стабилизируют трилоном Б в концентрации 0,03 %. Срок годности этих капель — 3 года.
При добавлении комплексного стабилизатора — смеси 0,1 % натрия метабисульфита и 0,03 % трилона Б — срок годности глазных капель, содержащих 0,02 % рибофлавина, 0,2 % кислоты аскорбиновой и 2 % глюкозы, увеличивается до 3 месяцев при хранении в условиях комнатной температуры и до 6 месяцев при температуре 4 °С.
Для стабилизации глазных капель могут быть использованы и другие методы, а именно: добавление высокополимеров, комплексо-нов, приготовление растворов в атмосфере инертных газов и т. д. Эти способы могут рассматриваться как потенциальные возможности значительного увеличения сроков годности глазных капель. Нестойкие глазные капли выпускаются в виде навесок сухого (лиофи-лизированного) вещества во флаконах и растворяются в стерильном растворителе непосредственно перед применением. Это относится к интермедину, ацетилхолину и другим препаратам.
Пролонгирование терапевтического действия г л а з н ы х к а п е л ь. Недостатком многих препаратов, применяемых в виде водных растворов, является короткий период их терапевтического действия.
Например, гипотензивное действие водного раствора пилокарпина гидрохлорида у больного глаукомой сохраняется только в течение 2 часов, что влечет за собой 6-кратную инстилляцию глазных капель в сутки.
В данном случае наблюдаются колебания внутриглазного давления. Частые инстилляции водного раствора смывают слезную жидкость, содержащую лизоцим, и тем самым создают условия для возникновения инфекционного процесса.
Это вызвало необходимость поиска веществ, способствующих пролонгированию (удлинению) терапевтического действия глазных капель. Рекомендуемая вязкость глазных капель 15—30 сантипуаз при температуре, соответствующей температуре тела.
С целью продления действия глазных капель делались попытки заменить воду другими растворителями, обладающими вязкостью, которые замедляют быстрое вымывание лекарственных веществ из конъюнктивального мешка. В качестве таких компонентов ранее использовали масла (рафинированное подсолнечное, персиковое или абрикосовое), трагакант и другие вещества. Но по различным причинам они широкого распространения не получили. Высокий показатель преломления, химическая неустойчивость ограничили их применение.
Более эффективные пролонгаторы для глазных капель — синтетические гидрофильные высокомолекулярные соединения. Для пролонгирования действия лекарственных веществ, применяемых в глазных каплях, в состав растворителя могут быть включены производные целлюлозы, такие, как метилцеллюлоза (0,5—2 %), натриевая соль карбоксиметилцеллюлозы (0,5—2 %), поливинол (1,5 %), микробный полисахарид аубазидан (0,1—0,3 %), полиглюкин и др. Эти вещества не раздражают слизистую оболочку глаза, в ряде случаев ускоряют эпителизацию эрозированной роговицы, а также совместимы со многими лекарственными веществами и консервантами.
Несмотря на то, что указанные пролонгирующие компоненты включены в ГФУ, они могут добавляться к глазным каплям только по указанию врача.
Удлинение действия глазных капель при использовании ВМС объясняется увеличением вязкости раствора и его контакта со слизистой оболочкой глаза. Так, метилцеллюлоза в концентрации (0,2— 2 %) обладает высокой вязкостью и коэффициентом преломления, равным 1,336 (коэффициент преломления воды = 1,333), что обеспечивает нормальное зрение. Она используется для приготовления глазных капель с пилокарпина гидрохлоридом, гоматропина гидробромидом, этилморфина гидрохлоридом, цинка сульфатом и др.
Однако, в последнее время наметилась тенденция к сокращению производства глазных капель на основе метилцеллюлозы. Это связано с тем, что она тормозит процессы регенерации эпителия роговицы, а при субконъюнктивальном введении приводит к разрастанию ткани. Поэтому в качестве пролонгатора в глазных каплях используют натрий-карбоксиметилцеллюлозу, которая хорошо растворима в воде и легко смешивается со слезной жидкостью. Например, количество инстилляций 2 %-ных растворов пилокарпина гидрохлорида, приготовленных с 2 % натрий-карбоксиметилцеллюлозы, у ряда больных глаукомой было сокращено до 3 раз в сутки вместо 6 инстилляций водного раствора.
Значительные преимущества по сравнению с производными ме-тилцеллюлозы имеет поливиниловый спирт (ПВС). Он не раздражает слизистую оболочку глаза, не нарушает целостности эпителия роговицы и в отличие от раствора метилцеллюлозы ускоряет эпите-лизацию эрозированной роговицы.
Растворы ПВС совместимы с большим количеством лекарственных веществ, применяемых в офтальмологии (антибиотиками, сульфаниламидами, солями алкалоидов, цинка сульфатом и др.). В то же время некоторые вещества (резорцин, кислота борная, натрия тетраборат) могут вызывать гелеобразование ПВС и делают невозможным его применение.
В качестве пролонгатора был предложен также полиакриламид, рН 1 %-ного раствора которого равен 5,0—7,0. Растворы выдерживают стерилизацию, совместимы со многими лекарственными веществами, не обладают раздражающими свойствами. 1 %-ный раствор полиакриламида может быть использован как растворитель для глазных капель пилокарпина гидрохлорида, атропина сульфата, дикаи-на, сульфапиридазин-натрия, скополамина гидробромида. Полиак-риламид обладает интерферогенной активностью, то есть способствует продукции интерферона (эффективное средство противовирусной терапии) при отсутствии токсического действия на макроорганизм.
Хорошим растворителем для получения глазных капель пролонгированного действия является 25 %-ный раствор полиэтиленок-сида-400. Он не только продлевает период терапевтического эффекта, но и увеличивает биологическую доступность лекарственных веществ (дикаина, новокаина и др.).
Принципиально новые возможности применения лекарственных веществ дало использование в фармации новых полимерных материалов, в том числе биорастворимых.
Так, сотрудниками Московского НИИ глазных болезней им. Гельм-гольца были предложены глазные полимерные пленки, приготовленные из 10 %-ного раствора поливинилового спирта (ПВС) и импрегнированные антибиотиками, пилокарпином и кортикостеро-идами. Однако эти пленки, хотя и пролонгировали действие лекарственных веществ и выдерживали хранение в течение 2 месяцев, имели существенный недостаток — они не растворялись в конъюнк-тивальной полости, а только набухали, увеличиваясь в размерах. Для устранения этого недостатка предложены пленки из биорастворимого полимера, например, глазные пленки с фенольным гидрофильным препаратом прополиса (разработаны академиком А. И. Тихоновым).
Благодаря пролонгирующему действию для получения терапевтического эффекта глазные лекарственные пленки можно применять 1 раз в сутки.
Преимущества глазных пленок — это высокая стабильность лекарственных веществ, удобство применения, гигиеничность, портативность и эффективность действия лекарственных препаратов.
В некоторых странах при приготовлении глазных лекарств используют различные полимерные растворы, которые обеспечивают пролонгирование терапевтического действия лекарственных веществ. Например, в Германии применяют раствор-носитель «Изанто», жидкую основу «Ликвифильм», которые способны покрывать поверхность глаза невидимой тоненькой пленкой, более чем в 3 раза удлиняющей терапевтическое действие растворенных лекарственных веществ.
Изотоничность. Многие глазные капли вызывают при ин-стилляции неприятные ощущения (жжение или боль). В большинстве случаев дискомфортные явления обусловлены несоответствием осмотического давления и значения рН глазных капель с осмотическим давлением и значением рН слезной жидкости. Глазные капли должны быть изотоничны слезной жидкости человека и соответствовать осмотическому давлению растворов натрия хлорида концентрации 0,9±0,2 % (0,7—1,1%), которое составляет приблизительно 286 мосмоль/кг. В отдельных случаях допускается применение гипертонических или гипотонических растворов, о чем должно быть указано в частных статьях.
В зависимости от величины осмотического давления глазные капли можно разделить на три группы:
1. Глазные капли, осмотическое давление которых ниже 0,7 % эквивалентной концентрации натрия хлорида — гипотонические растворы, обязательно изотонируются рассчитанным количеством натрия хлорида. Особенно важно, чтобы изотоничными были промывания для глаз.
2. Глазные капли, осмотическое давление которых выше 1,1 % эквивалентной концентрации натрия хлорида, не изотонируются, так как являются гипертоническими.
 2014-02-17
2014-02-17 1043
1043








