ПЛАН ЛЕКЦИИ
Лекция 12
Оксидами алюминия, кремния и титана
Оксидами щелочных и щелочноземельных металлов, а также
Катализаторм синтеза аммиака является железо, промотированное
И азот, получаемый из воздуха криогенным способом
Исходным сырьем является водород, получаемый из синтез-газа,
На процессы при низком, среднем и высоком давлениях
Промышленные технологии ситнтеза аммиака подразделяются
ВЫВОДЫ
Сырьем для азотной кислоты, как и для других азотосодержащих продуктов, служит аммиак.
Синтез азотной кислоты в соответствии с типом химико-технологической системы является сложным, односторонним, гетерогенно-каталитическим процессом с выделением тепла, т.е. с отрицательной
энтальпией и с диффузионным торможением
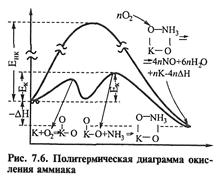
Химическая схема синтеза:
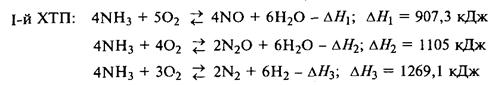 |
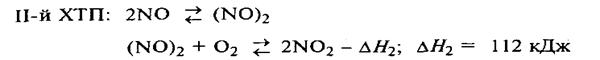
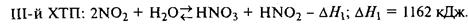
В условиях абсорбции диоксида азота водой возможно самовосстановление (самоокисление) оксидов азота:
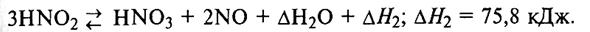 |
Суммарная реакция
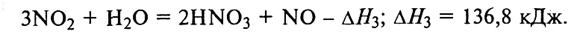 |
Известны три ХТС получения азотной кислоты:
• под атмосферным давлением,
• под повышенным давлением
• комбинированные, в которых окисление аммиака проводят под атмосферным давлением, окисление оксида азота до диоксида и хемосорбцию диоксида водой под повышенным давлением.
Современные производства азотной кислоты работают под повышенным давлением, так как, несмотря на меньшие расходы платины, установки под атмосферным давлением требуют больших капиталовложений вследствие малой их производительности и применения дорогостоящей и не слишком эффективной утилизации отходящих газов, содержащих N0, т.е. при существенных потерях аммиака. Установки, работающие при повышенном давлении, и комбинированные работают по принципу энерготехнологических систем, в них энергию отходящих газов и теплоту реакции окисления аммиака используют для сжатия синтез-газа, а также для получения технологического пара.
На рис. представлена технологическая схема получения разбавленной азотной кислоты под давлением 7,3 МПа.
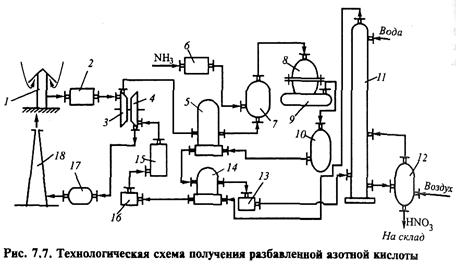
Атмосферный воздух после очистки поступает в компрессор 3, приводимый в движение газовой турбиной 4, где он сжимается до давления 0,73 МПа и нагревается до 135 °С.
Далее он поступает в подогреватель воздуха 5, где его температура поднимается до 250 °С за счет теплоты выходящих из окислителя нитрозных газов 10.
В смесителе 7 воздух смешивается с газообразным аммиаком, поступающим из испарителя аммиака 6.
Аммиачно-воздушную смесь направляют в контактный аппарат 8, где при температуре 900 °С на катализаторе, представляющем собой сплав платины (93%), палладия (4%) и родия (3%), происходит окисление аммиака.
Катализатор выполнен в виде сеток из проволоки диаметром 0,06-0,09 мм, имеющих 1024 отверстия в 1 см2. Для создания определенной продолжительности контактирования сетки скрепляют в виде пакета, который устанавливают в контактном аппарате.
Нитрозные газы поступают в котел-утилизатор 9, где охлаждаются до необходимой температуры и где образуется пар.
Далее газы поступают в окислитель 10, в котором монооксид окисляется в диоксид оставшимся в смеси кислородом.
Охлажденные в подогревателе воздуха 5, подогревателе хвостовых газов 13 и холодильнике-конденсаторе 12 до температуры около 45 °С нитрозные газы поступают в абсорбционную колонну 11, орошаемую противоточной водой.
Полученная азотная кислота (концентрацией 60-62%) самотеком поступает в отдувочную колонну 12, где с помощью горячего воздуха из петролеума (HNO3NO2) происходит отделение N02, которые направляются в абсорбционную колонну.
Хвостовые газы, пройдя систему каталитической очистки от оксидов азота восстановлением их аммиаком до элементного азота, выбрасываются в атмосферу
Катализатор выполнен в виде сеток из платиновой проволоки диаметром 0,06-0,09 мм, имеющих 1024 отверстия в 1 см2.
Для создания определенной продолжительности контактирования сетки скрепляют в виде пакета, который устанавливают в контактном аппарате.
При окислении аммиака под давлением увеличиваются потери платинового катализатора. Поэтому окисление аммиака производят при давлении около 0,4 МПа, а окисление оксида азота - при 1,2 МПа.
Для производства взрывчатых веществ, некоторых пластических масс, красителей необходима 98%-я азотная кислота. Ее можно получить концентрированием или прямым синтезом.
В качестве водоотнимающего средства применяют 94%-ю серную кислоту или нитрат магния
•Получение 98%-й азотной кислоты проводят прямым синтезом с применением обогащения газовой фазы диоксидом азота и свободного кислорода.
•Суммарная реакция
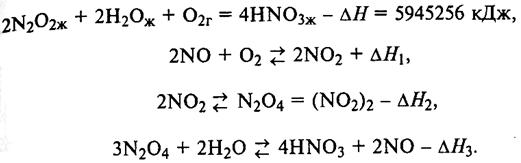
Для проведения синтеза нужно поднять давление до 50 ат, ввести некоторый избыток диоксида азота по отношению к воде, повысить температуру до 70 -80 °С.
Технологическая схема прямого синтеза азотной кислоты
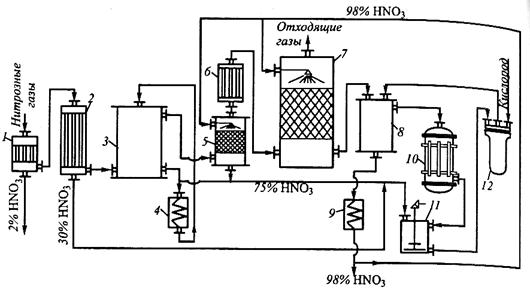 |
Для проведения указанных химических превращений требуется поднять давление до 50 ат, ввести некоторый избыток диоксида азота по отношению к воде, повысить температуру до 70 -80 °С.
При существовании NО2 в системе, где присутствует вода или азотная кислота, она резко меняет свои первоначальные термодинамические параметры. При взаимодействии N0 с NОз монооксид азота окисляется азотной кислотой до диоксида и образуется вода:
N0 + 2НN03 Û 2 N02 + 2Н20
Диоксид азота может быть выделен из нитрозных газов конденсацией или растворением. Легче его выделить из газов, получаемых окислением аммиачно -кислородных смесей, содержащих оксиды азота, кислород, немного азота и водяной пар.
На установках, работающих под повышенным давлением, можно получить жидкий диоксид азота, направив нитрозные газы в холодильник, и получить систему, состоящую из 30 -35% НКО3. Далее смесь из жидкого диоксида азота и воды направляют в автоклав, куда подают элементный кислород. Технологическая схема прямого синтеза азотной кислоты представлена на рис. 7.10.
Нитрозные газы, поступающие из контактного аппарата, направляются в два водяных холодильника 1, 2. Первый - скоростной (прямоточный), из него конденсат подают для дальнейшего использования (содержит 2-3% НМО3) в производстве азотной кислоты. Конденсат из второго холодильника направляют в смеситель 11, а нитрозные газы - в окислительную башню 3, где они окисляются содержащимся в газе кислородом до "93%, а затем в доокислительную башню 5, где окисление происходит концентрированной азотной кислотой,
Образовавшаяся 75%-я азотная кислота поступает в смеситель Ц. Из полученных в башне 5 нитрозных газов в виде ЫО2 Диоксид азота извлекают концентрированной азотной кислотой 1 башне 7. Для увеличения степени извлечения газ предварительно охлаждают в холодильнике 6 до ~10°С. До такой же температуры охлаждают поступающую азотную кислоту.
Нитрозные газы, поступающие из контактного аппарата, направляются в два водяных холодильника 1, 2. Первый - скоростной (прямоточный), из него конденсат подают для дальнейшего использования (содержит 2-3% НМО3) в производстве азотной кислоты. Конденсат из второго холодильника направляют в смеситель 11, а нитрозные газы - в окислительную башню 3, где они окисляются содержащимся в газе кислородом до "93%, а затем в доокислительную башню 5, где окисление происходит концентрированной азотной кислотой.
Образовавшаяся 75%-я азотная кислота поступает в смеситель 11. Из полученных в башне 5 нитрозных газов в виде NО2Диоксид азота извлекают концентрированной азотной кислотой 1 башне 7. Для увеличения степени извлечения газ предварительно охлаждают в холодильнике 6 до ~10°С. До такой же температуры охлаждают поступающую азотную кислоту.
 2014-02-09
2014-02-09 1462
1462