Кислород в кремнии
Кислород относится к числу примесей, быстро диффундирующих в кремнии. Его предельная растворимость несколько превышает 1017 см-3 при температуре, близкой к температуре плавления кремния и быстро уменьшается при понижении температуры. Например, при 900оС (температуре “загонки”) растворимость кислорода падает приблизительно до 1015 см-3. В растворенном состоянии кислород электрически не активен.
Связь O2–Si представляет собой ковалентную связь.
В оксиде кремния кислород занимает положение мостика между двумя атомами кремния, которые приблизительно сохраняют свою тетраэдрическую координацию по отношению друг к другу. Эти тетраэдры относительно легко деформируются, благодаря чему у SiO2 при разных температурах стабильными являются несколько кристаллографических форм. Фазовые переходы между этими формами идут достаточно медленно, так что вполне устойчивой является и аморфная модификация – плавленый кварц, структуре которого и соответствуют получаемые на кремнии пленки термически выращенного оксида.
При температуре 500…600оС кислород химически связывается с кремнием, причем вначале образуется комплекс, обладающий донорными свойствами. При дальнейшем повышении температуры каждый атом кислорода как бы встраивается между двумя атомами кремния, образуется Si–O–Si связь. В таком состоянии О2 также электрически не активен.
Оксид кремния относится к числу наиболее высококачественных диэлектриков. Он имеет диэлектрическую проницаемость 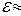 3.9,
3.9, 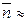 1.46,
1.46, 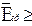 2 .107 В/см (в слоях
2 .107 В/см (в слоях 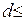 200 нм). У более толстых слоев
200 нм). У более толстых слоев 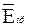 уменьшается пропрорционально
уменьшается пропрорционально 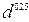 .
.
Роль, которую выполняет пленка SiO2 определяет возможность использования того или иного метода ее получения.
Для использования в качестве межуровневой изоляции или защитного слоя, наносимого поверх металлизации можно использовать химическое осаждение из газовой фазы. Защитные слои часто наносятся также пиролизом ТЭОС.
Слои, используемые в качестве масок при локальном легировании, обычно получают термическим окислением. На практике нередко используется комбинированный режим окисления, когда начальный этап окисления ведется в атмосфере сухого O2, затем в атмосфере паров воды, после чего опять следует окисление в сухом O2. Длительности этих трех процессов выбираются приблизительно равными. Первый этап окисления задает структуру границы раздела Si–SiO2. Во время второго этапа формируется основная толща пленки. Третий этап является термообработкой, в процессе которой понижается концентрация растворенной в пленке воды, толщина пленки при этом увеличивается незначительно. Такая методика позволяет сравнительно быстро получать слои SiO2, по свойствам приближающиеся к получаемым в атмосфере сухого O2. Для получения маскирующих слоев используют также методы химического осаждения из газовой фазы.
Наиболее высококачественные слои SiO2 для МДП структур получают только термическим окислением в атмосфере сухого O2. Для МДП структур на основе иных полупроводниковых соединений используют методы химического осаждения из газовой фазы или анодирования.
| Параметр | Значение параметра |
| Плотность, г/см3 | 2.2 |
| Показатель преломления | 1.46 |
| Диэлектрическая постоянная | 3.82 |
| Ширина запрещенной зоны, эВ | 8.9 |
| Удельное сопротивление постоянному току при T = 25 ºС, Ом*см | 1014-1016 |
| Скорость травления в буферном растворе HF, нм/мин | |
| Линия ИК поглощения, мкм | 9.3 |
| Коэффициент теплового расширения, С-1 | 5*10-7 |
| Механические напряжения в окисле, дин/см2 | 3*109 |
 2014-02-09
2014-02-09 5255
5255
