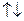Для двухатомной молекулы полярность молекулы совпадает с полярностью связи. В многоатомных молекулах общий дипольный момент молекулы равен векторной сумме моментов всех её связей. Вектор диполя направлен от + к –
Пример 3. Используя метод валентных связей, определите полярность молекул хлорида олова (II) и хлорида олова (IV).
50Sn относится к р – элементам.
Валентные электроны 5s25p2. Распределение электронов по квантовым ячейкам в нормальном состоянии:
5 - валентность 2
s p
и в возбуждённом состоянии: 5 - валентность 4
s p
17Cl – относится к р – элементам. Валентные электроны 3s
23p
5. Распределение электронов по квантовым ячейкам в нормальном состоянии: 3 - валентность 1.
s p
Химические формулы хлорида олова (IV) -SnCl4, хлорида олова (II) – SnCl2
Для построения геометрической формы молекул изобразим орбитали неспаренных валентных электронов с учётом их максимального перекрывания
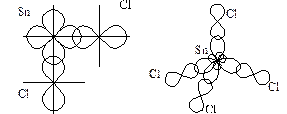
Рис. 4. Геометрическая форма молекул SnCl2 и SnCl4
Электроотрицательность Sn – 1,8. Cl – 3,0. Связь Sn – Cl, полярная, ковалентная. Изобразим вектора дипольных моментов полярных связей.
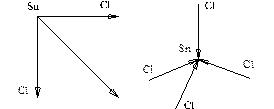
Рис. 5. Направление векторов дипольных моментов
в молекулах SnCl2 и SnCl4
SnCl2 – полярная молекула
SnCl4 – неполярная молекула.
Вещества в зависимости от температуры и давления могут существовать в газообразном, жидком и твёрдом агрегатном состоянии.
В газообразном состоянии вещества находятся в виде индивидуальных молекул.
В жидком состоянии в виде агрегатов, где молекулы связаны межмолекулярными силами Ван–дер–Ваальса или водородной связью. Причём, чем полярнее молекулы, тем прочнее связь и, как следствие, выше температура кипения жидкости.
В твёрдых телах структурные частицы связаны как внутримолекулярными, так и межмолекулярными связями. Классифицируют: ионные, металлические, атомные (ковалентные), молекулярные кристаллы и кристаллы со смешанными связями.
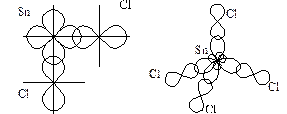
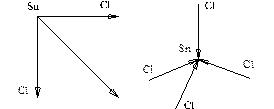
 2015-01-30
2015-01-30 4338
4338