Ресурсо- и энергосберегающие технологии в производстве экстракционной фосфорной кислоты.
H3PO4 – сильная кислота
2 метода:
термический метод
экстракционный метод
Термический метод основан на термическом сжигании фосфора в среде кислорода.
1 стадия. P + O2 → P2O5 (2.1)
реакция сжигания, сильно экзотермическая
2 стадия. P2O5 + 3H2O → 2H3PO4 (2.2)
Продукционная ортофосфорная кислота имеет концентрацию 85-86% масс. по P2O5 , практически без примесей.
Экстракционный метод основан на сернокислотном разложении апатитового концентрата.
Са5F(PO4)3 + 5H2SO4 + 10H2O → 3H3PO4 + 5CaSO4∙2H2O + HF (1.1)
Продукционная ЭФК с концентрацией 40% масс. по P2O5 (наличие примесей).
В зависимости от чистоты продукта различается область применения:
Чистая ортофосфорная кислота используется при фосфотировании Ме поверхностей (предварительная стадия перед окраской Ме поверхности), т. к. фосфорная кислота с добавками Zn или Mn образует на поверхности Ме защитную пленку.
В последнее время ортофосфорная кислота используется в парфюмерном пр-ве.
|
|
|
Область применения ЭФК:
Пр-во фосфорных и сложных концентрированных удобрений, а также получение фосфатов (кормовых), моющих и водоумягчающих средств.
Используется при крашении текстильных тканей, в реакциях органического синтеза (как катализатор).
По объему промышленного пр-ва в ассортиментной линейке занимает 3 место после серной и азотной кислот.
Некоторые характеристики водных растворов H3PO4 :
Таблица 2.1. Характеристики водных р-ров H3PO4 .
Давление атмосферное.
| Конц. P2O5, % масс. | t затверд., °С | t кип., °С | Cp, кДж/(кг∙К) | ή (25°С), Па·с |
| 0,8 | 100,10 | 4,0737 | 0,0010 | |
| -21,9 | 103,9 | 3,0271 | 0,0035 | |
| -76,9 | 114,9 | 2,4995 | 0,0092 |
Как видно из табл. 2.1 с ростом концентрации изменяется t кип, t затверд,
Ср, ή.
Это объясняется строением водных растворов H3PO4 .
Согласно основным законам, установленная связь между C, t, P объясняется повышением (понижением) T фаз. превр. (кип., замерз.) за счет внутреннего строения р-ра и сил взаимодействия между растворенным в-вом и р-лем.
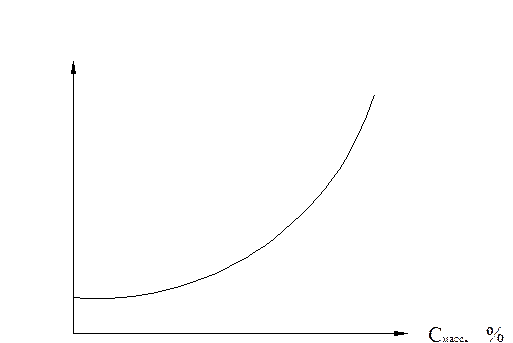
∆T = Tкип. р-ра - Tкип. чист. р-ля - температурная депрессия
Рис. 2.1. Зависимость температурной депрессии от концентрации.
|

|
С точки зрения технико-экономических показателей, большое преимущество имеет экстракционный способ (по сравнению с термическим).
Сравнение по минимуму приведенных затрат:
Зприв = Сб + Ен∙Куд (2.3)
Сб - себестоимость продукции, руб/т
Ен - нормативный коэффициент
Куд – уд. Капитальные затраты, руб/т
Ен = 1/Ток (2.4)
Ток – срок окупаемости
Сб = ∑Зi /ПR (2.5)
Куд = стоим. оборуд./ ПR (2.6)
∑Зi – текущие затраты
∑Зi = Зсырье + Зматер. + Зэнерг. + Зз.п. + Зремонт
|
|
|
ПRЭФК > ПRортофосф. к-ты (2.7)
При прочих равных условиях СбЭФК < Сбортофосф. к-ты
ЦЭФК < Цортф. к-ты
Условие (2.7) обусловлено народнохозяйственным спросом на рынке.
Сернокислотное разложение фосфатного сырья.
В основе лежит реакция (1.1).
Сырье- апатитовый концентрат
Источник- Карелия
Суть метода: извлечение (экстрагирование) H2O5 в виде H3PO4.
По этому методу природные фосфаты обрабатывают серной кислотой с последующим фильтрованием экстракционной пульпой с получением технической H3PO4 и осадка – ФГ.
Часть выделенного основного фильтрата, смешанного с промывочным раствором называют раствором разбавления, который возвращается в экстрактор для уменьшения вязкости реакционной пульпы в экстракторе.
Химическая схема процесса.
Классификация р-ции (1.1):
Гетерогенная (участники процесса находятся в разных фазах, а сам процесс протекает на границе раздела фаз).
Лимитирующей стадией является кристаллизация ФГ.
CaSO4∙2H2Oе ↔ Сае2+ + SO42- + 2H2O (2.8) ∆H< 0;
Обоснование технологического режима ТР.
ТР – такая совокупность технологических параметров (T,P,C), которая обеспечивает оптимальные условия эксплуатации оборудования.
Выбор и обоснование ТР будем проводить на основании данных о химическом равновесии и химической кинетике процесса.
 2015-02-27
2015-02-27 474
474








