Обоснование ТР производства ЭФК.
Выбор ТР на основании данных о хим. равновесии
CaSO4е ↔ Сае2+ + SO42- е; ∆H< 0 (3.1)
Анализ данных по химическому равновесию позволяет ответить на вопрос о возможности осуществления процесса.Позволяет определить равновесный состав реакционной смеси во время химического равновесия, а также позволяет управлять составом реакционной смеси в момент равновесия.
Для оценки влияния технологических параметров на состояние химического равновесия используют качественную и количественную оценки.
Изменять значение равновесной концентрации вещества в растворе- значит управлять величиной предела растворимости.
Нас интересует состояние реакционной системы, когда образуется осадок (ФГ).
Растворимое соединение выпадает в осадок при условии:
СМеn+,e∙CАm-,e > ПР/(γМеn+∙γАm-) (3.2), где
γ- соответствующие значения коэффициентов активности ионов.
Учитывают реальные силы взаимодействия ионов по сравнению с идеальными растворами.
Таблица 3.1. Некоторые значения ПР.
| соединения | СаСО3 | ZnS | PbCO3 | CdS | CaF2 | FeS |
| ПР | 3.1∙10-9 | 1.6∙10-24 | 1.5∙10-13 | 1∙10-29 | 4·10-11 | 4·10-19 |
Пути управления процессом (р-ция 3.1) за счет смещения химического равновесия.
1 прием.
Добавление H2SO4 в реакционную смесь в экстракторе.
Хим. равновесие смещается влево (Сае2+ ↓), движущая сила процесса увеличивается:
(∆ДСС)ДС = Сраб. – Сравн.
Рис. 3.1.а) Характер зависимости ССа2+,е от Т.
|

|
1- без дополнительных примесей;
2- с избытком H2SO4;
∆H< 0, ↑Т приводит к смещению химического равновесия влево, т. е. растворимость в-ва ↓.
Рис. 3.1. б).
ССа2+,е

3- ход кривой растворимости при добавке H3PO4.
С увеличением концентрации H3PO4 в реакционной смеси, растворимость ФГ↑.
ДС = Сраб. – Се ↓.
Выбор ТР на основании данных о химической кинетике.
Химическая реакция (3.1) – гетерогенная, многостадийная.
Для описания кинетики используется модель с фронтальным перемещением зоны реакции и непрореагировавшим ядром (МФПЗРиНЯ).
Основные допущения:
Рассматривается единичная шарообразная частица ФГ в потоке жидкой реакционной смеси.
рис.3.2. Распределение концентраций веществ вблизи шарообразной частицы:
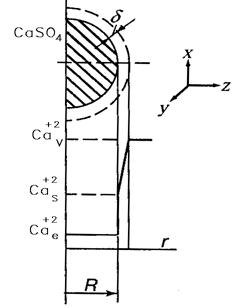
Реакционная смесь – сложная 3-х фазная система, динамическая, где тв. фаза- частицы образующегося ФГ;неразложившиеся частицы апатита;
жидкая фаза- фосфорная, серная кислоты;
газовая фаза- гидриды.
Лимитирующая стадия всего процесса – кристаллизация фосфогипса.
Условные обозначения к рис. 3.2:
ССа2+,ν, ССа2+,s, ССа2+,e – концентрация ионов Са2+ в объеме реакционной смеси, на поверхности твердой частицы ФГ и равновесная.
R- наружний радиус тв. ч-цы ФГ
δ – толщина пограничного слоя- это диффузионный слой, в котором сосредоточено основное сопротивление массопереносу.
Rсоп = 1/β или R= 1/βг (β- коэффициент массоотдачи)
Согласно МФПЗРиНЯ можно выделить основные стадии:
1. Внешняя диффузия ионов кальция из объема РС к наружней поверхности тв. ч-цы ФГ (кривая 1-2)
Wг = - 1/S·dWj/dτ (3.3)
S- поверхность раздела фаз
Уравнение (3.3) для 1 стадии:
Wг = β(ССа2+,ν – ССа2+,s) (3.4)
β≈D/δ
Пути управления скоростью на 1 стадии:
Измельчение δ↓→β↑
При этом средний размер частиц ФГ уменьшается, соотвктственно фильтрующие свойства осадка фосфогипса ухудшаются (увеличивается проскок твердых частиц через слой фильтрующего материала).
 2015-02-27
2015-02-27 302
302








