Для коллоидных растворов удобнее в уравнении (2.6) заменить соотношение C1/C2 на n1/n2, где n1и n2– концентрация, выраженная числом частиц в единице объема. В результате уравнение (2.6) принимает вид:
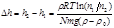 .
.
Уравнения (2.6) и (2.7) позволяют вычислить, на какой высоте концентрация частиц изменится в заданное количество раз. Например, для воздуха высота h2, на которой концентрация кислорода уменьшится вдвое, составляет 5 км. На высоте 100 км концентрация уменьшится в 106раз.
Для количественной оценки кинетической неустойчивости дисперсных систем используется критерий: 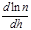 , где n – число частиц в единице объема.
, где n – число частиц в единице объема.
Этот критерий показывает, как быстро происходит относительное изменение концентрации частиц по высоте, т.е. характеризует кинетическую неустойчивость системы.
После несложных преобразований из (2.7) можно получить:
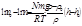 , где no– число частиц в единицах объема на фиксированной высоте ho. После дифференцирования получим:
, где no– число частиц в единицах объема на фиксированной высоте ho. После дифференцирования получим:
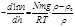 . При увеличении радиуса частиц в 100 раз величина d ln n / dh увеличивается в 1 000 000 раз. Таким образом, устойчивость одной и той же системы в пределах коллоидной степени дисперсности (1‑100 нм) может различаться в миллион раз.Из (2.9) следует: чем меньше разность плотностей дисперсной фазы и дисперсионной среды ( – о), тем больше кинетическая устойчивость системы. Если плотности равны = о, то d ln n / dh обращается в нуль, т.е. концентрация дисперсной фазы не изменяется по высоте. В этом случае система абсолютно кинетически устойчива. Если плотности дисперсной фазы меньше плотности дисперсионной среды о, то – о 0 и соответственно d ln n / dh 0, это означает, что частицы будут всплывать, т.е. концентрация увеличивается по высоте, например, концентрация частичек жира в молоке. Уравнения (2.7)-(2.9) характеризуют стационарное состояние дисперсной системы, которое получило название седиментационное равновесие. Для того, чтобы система пришла к этому состоянию, необходимо некоторое время, зависящее от скорости оседания (или всплывания) частиц. По формуле Стокса скорость U оседания частиц равна:
. При увеличении радиуса частиц в 100 раз величина d ln n / dh увеличивается в 1 000 000 раз. Таким образом, устойчивость одной и той же системы в пределах коллоидной степени дисперсности (1‑100 нм) может различаться в миллион раз.Из (2.9) следует: чем меньше разность плотностей дисперсной фазы и дисперсионной среды ( – о), тем больше кинетическая устойчивость системы. Если плотности равны = о, то d ln n / dh обращается в нуль, т.е. концентрация дисперсной фазы не изменяется по высоте. В этом случае система абсолютно кинетически устойчива. Если плотности дисперсной фазы меньше плотности дисперсионной среды о, то – о 0 и соответственно d ln n / dh 0, это означает, что частицы будут всплывать, т.е. концентрация увеличивается по высоте, например, концентрация частичек жира в молоке. Уравнения (2.7)-(2.9) характеризуют стационарное состояние дисперсной системы, которое получило название седиментационное равновесие. Для того, чтобы система пришла к этому состоянию, необходимо некоторое время, зависящее от скорости оседания (или всплывания) частиц. По формуле Стокса скорость U оседания частиц равна:
|
|
|
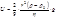 . Расчеты по уравнению Стокса показывают, что для частиц с плотностью 10 г/см3и плотностью дисперсионной среды = 1 г/см3при вязкости среды = 0,0015 Па ´ сек частицы с радиусом 100 нм проходят путь в 1 см – за 5,86 сек, с радиусом 10 нм – за 16 часов, а с радиусом 1 нм – за 19 лет. Установление равновесия требует сохранения состояния покоя и постоянства температуры, чтобы избежать появления конвективных потоков.
. Расчеты по уравнению Стокса показывают, что для частиц с плотностью 10 г/см3и плотностью дисперсионной среды = 1 г/см3при вязкости среды = 0,0015 Па ´ сек частицы с радиусом 100 нм проходят путь в 1 см – за 5,86 сек, с радиусом 10 нм – за 16 часов, а с радиусом 1 нм – за 19 лет. Установление равновесия требует сохранения состояния покоя и постоянства температуры, чтобы избежать появления конвективных потоков.
Для того, чтобы ускорить оседание частиц, используются ультрацентрифуги, которые позволяют заменить силы земного притяжения центробежной силой. Эта сила может превышать силу земного притяжения в 1 000 000 и более раз. Наряду с ускорением процесса использование ультрацентрифугирования позволяет определить средний размер коллоидных частиц, распределение их по размерам и даже качественно оценить отклонение частиц от сферической формы.
|
|
|
78. Строение коллоидных частиц.
Рассмотрим строение коллоидных частиц на примере коллоидного раствора иодида серебра, приготовленного из растворов AgNO3и KI при избытке AgNO3.Твердая частица – ядро коллоидной частицы – кристаллы иодида серебра (AgJ)n. Поверхность ядра адсорбирует преимущественно ионы Ag+, входящие в состав кристалла ядра, приобретая положительный заряд. Обозначим количество ионов Ag+, адсорбированное ядром, через n. Это количество входит в состав ядра. К заряженному ядру притягиваются противоионы NO3-, формируя двойной электрический слой. Часть противоионов n-x находится в адсорбционном слое, которые вместе с ядром составляют частицу, или гранулу. Остальная часть противоионов (х) находится в свободном объеме раствора. Пунктиром изображена линия, замыкающая весь объем
электролита, в котором находятся противоионы. Ядро вместе с адсорбционным слоем и слоем свободной жидкости, в которой находятся противоионы, называется мицеллой.
В коллоидной химии принята такая форма записи строения мицеллы:

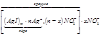
Эта формула соответствует схеме коллоидной частицы, изображенной на рис. 2.2.
Свойства коллоидных систем:
1) концентрация ионов в растворе: чем больше концентрация ионов, тем большее количество противоионов накапливается в твердом слое и тем меньше их будет в диффузной области;
2) заряд противоионов: чем больше заряд противоионов, тем сильнее они притягиваются к заряженной поверхности твердого тела, тем тоньше диффузный слой и соответственно меньше величина дзета-потенциала;
3) полярность противоионов: чем больше поляризуемость противоионов, тем больше дополнительные силы притяжения и тем тоньше становится слой Гельмгольца;
4) лиофильность: оболочка из молекул растворителя снижает силу взаимодействия между поверхностью твердого тела и противоионами. чем прочнее сольватная оболочка, тем толще диффузный слой и тем больше электрокинетический потенциал.
 2015-02-04
2015-02-04 1811
1811








