Состояние атома, при котором его электроны находятся на таких энергетических уровнях, что их суммарная энергия является минимальной, называется основным или невозбужденным. Состояния с более высокими значениями энергии называются возбужденными.
При сообщении атому дополнительной энергии электроны могут переходить на обладающие большей энергией орбитали. Эти переходы с подуровня на подуровень возможны только в пределах одного внешнего энергетического уровня. Происходящее при этом распаривание электронов приводит к возрастанию у атома числа неспа-ренных электронов, т.е. к появлению новых валентных возможностей.
Например, при возбуждении у атома бериллия один электрон с внешнего подуровня 2 s переходит на обладающий большей энергией и ранее свободный (вакантный) подуровень 2 р. При этом валентность атома бериллия становится равной 2.
Электронная формула атома бериллия в возбужденном состоянии будет иметь вид:
4 Bе٭ 1s2 2s1 2р1.
Электронно-графическая формула атома бериллия в возбужденном состоянии:
|
|
|
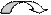 | |||
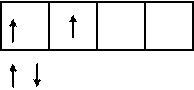 |
 2 Валентность II
2 Валентность II
1 p
s
Электронная формула атома бора в нормальном состоянии:
5B 1 s 22 s 22 p 1.
Электронно-графическая формулаатома бора имеет вид:

 2015-03-27
2015-03-27 14287
14287
