Вещества, растворение которых приводит к снижению поверхностного натяжения растворителя, носят название поверхностно-активных веществ (ПАВ), а их свойство понижать s называют поверхностной активностью. ПАВ - это обычно органические соединения, молекулы которых имеют несимметричное, дифильное строение, т.е. состоят из двух частей или групп - полярной и неполярной. Примером полярных групп могут служить: ¾OH, ¾COOH, ¾NO2, ¾CN, ¾NH2 и т.д. Неполярной частью молекулы обычно являются углеводородные радикалы. Примером наиболее распространенного ПАВ является обычное мыло (натриевые соли жирных карбоновых кислот), к ПАВ относят также карбоновые кислоты, спирты, амины, сульфокислоты и другие вещества.
Условно принято обозначать молекулу ПАВ символом ¾O, где кружек соответствует полярной группе, а палочка - неполярной части.
Из рисунка 13(А) видно, что для ПАВ (ds/dC) < 0 и, согласно уравнению Гиббса, Г > 0, т.е. молекулы ПАВ адсорбируются на поверхности раздела фаз, снижая тем самым поверхностное натяжение растворителя. Адсорбция ПАВ происходит по следующей причине. Взаимодействие между диполями воды значительно сильнее, чем между диполями и неполярными частями ПАВ. Поэтому энергетически выгоден переход молекул ПАВ из фазы на поверхность или в другую фазу, при этом восстанавливаются сильные диполь - дипольные и водородные связи молекул воды. Чем длиннее углеводородный радикал, тем больше молекул воды он разобщает и тем больше тенденция выхода молекул ПАВ на поверхность, т.е. тем больше их адсорбция.
Эффект снижения поверхностного натяжения водных растворов ПАВ может быть очень велик. Так, обычное мыло понижает поверхностное натяжение воды на 42,8×10-3 Дж/м2 при концентрации 10-3 моль/л. Для сравнения: повышение s для инактивного вещества обычно меньше 0,8×10-3 Дж/м2 даже при концентрации 1 моль/л.
С ростом концентрации ПАВ в растворе s сначала падает резко, а затем - постепенно (рис.13А). Подобный ход кривой объясняется тем, что при малых концентрациях поверхность жидкости свободна и практически все растворенные молекулы ПАВ адсорбируются на поверхности воды, сильно снижая s. При больших С на поверхности образуется насыщенный мономолекулярный слой молекул ПАВ, дальнейшая адсорбция становится невозможной и с ростом концентрации s изменяется незначительно. Поверхностное натяжение растворов при этих концентрациях приближается к значению s самих ПАВ на границе с воздухом (18 - 22 ×10-3 Дж/м2).
В 1908г Шишковский провел исследования зависимости s растворов низкомолекулярных карбоновых кислот (от C3 до C6) в воде от их концентрации. Результаты его опытов представлены на рис.13(Б).
Установлено, что полученные зависимости могут быть описаны эмпирическим уравнением Шишковского:
s - s0 = Ds = A ln(1 + B C)
Здесь so - поверхностное натяжение чистой воды, A и B - константы уравнения. Оказалось, что константа A остается постоянной для всех членов гомологического ряда, а константа B увеличивается в 3 - 3,5 раза при удлинении углеводородной цепи на одно звено -CH2-.
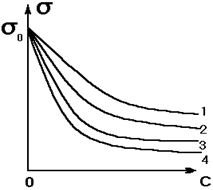 |
Рис.13(Б). Изотермы поверхностного натяжения кислот в воде: 1 - пропионовая; 2 - масляная; 3 - валериановая; 4 -капроновая (по данным Шишковского).
Графически дифференцируя кривые, полученные Шишковским, а также используя свои данные, Ленгмюр по уравнению Гиббса рассчитал изотермы адсорбции исследованных ПАВ. Изотермы приведены на рисунке 13(В).
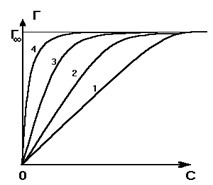 Рис.13(В). Изотермы адсорбции кислот в воде: 1 - пропионовой; 2 - масляной; 3 - валериановой; 4 - капроновой.
Рис.13(В). Изотермы адсорбции кислот в воде: 1 - пропионовой; 2 - масляной; 3 - валериановой; 4 - капроновой.
При одинаковой C адсорбция возрастает с удлинением цепи, но для всех членов ряда кривые стремятся к одному и тому же пределу Г¥, называемому предельной адсорбцией или ёмкостью монослоя. Факт постоянства Г¥ для всех членов ряда, на первый взгляд, удивителен, т.к. означает, что на единице поверхности помещается одно и то же число адсорбированных молекул, независимо от их размера. Этот факт, установленный экспериментально, позволил Ленгмюру выдвинуть представления об ориентации адсорбированных молекул в поверхностном слое и распространить уравнение изотермы, выведенное им для адсорбции на твердых адсорбентах, и на поверхность жидкость - газ. Действительно, кривые на рис.13(В) могут быть описаны изотермой Ленгмюра:
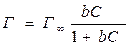
где b - адсорбционный коэффициент, Г¥ - емкость монослоя. Для объяснения постоянства Г¥ для всех членов гомологического ряда Ленгмюр предположил, что углеводородная цепь ПАВ не занимает места в поверхностном слое - неполярные части "торчат" в воздух, образуя "молекулярный частокол", как это изображено на рис.13(Г). В таком случае Г¥ определяется лишь размерами полярной группы S0, а она у всех гомологов одна и та же. Например, площадь поперечного сечения карбоксильной группы жирных кислот равна 21,3×10-20 м2. S0 можно рассчитать из адсорбционных измерений по уравнению:
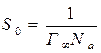
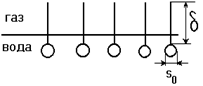 Рис.13(Г). Ориентация молекул ПАВ на поверхности вода - воздух.
Рис.13(Г). Ориентация молекул ПАВ на поверхности вода - воздух.
Зная Г¥, можно вычислить длину углеводородного радикала ПАВ, равную толщине насыщенного адсорбционного монослоя d, т.е. высоту "молекулярного частокола":
d = M Г¥ /r
Здесь r - плотность адсорбата, М – его молярная масса.
Совмещение уравнений Гиббса и Ленгмюра дает уравнение:
s = s0 - s = Г¥RT ln(1 + b C)
Оно аналогично уравнению Шишковского, при этом константа A = RTГ¥, т.е. она не должна зависеть от длины углеводородного радикала ПАВ, что и наблюдается в экспериментах. Величина B равна адсорбционному коэффициенту b в уравнении Ленгмюра, он индивидуален для каждого вещества и определяется способностью ПАВ к адсорбции, т.е. коэффициент B должен увеличиваться с ростом длины углеводородного радикала ПАВ, что также подтверждается опытом.
Исследуя поверхностное натяжение водных растворов органических веществ, Траубе (1891) установил правило, что в одном гомологическом ряду при малых концентрациях удлинение углеводородной цепи на СН2 – группу увеличивает поверхностную активность в 3-3,5 раза.
 2015-04-01
2015-04-01 4098
4098
