Гальванические элементы – это химические источники тока. Они состоят из двух электродов первого рода (металлов, опущенных в растворы собственных солей), соединенных во внешней и внутренней цепях. Рассмотрим элемент, состоящий из металлического цинка, погруженного в 0,1 М раствор нитрата цинка, и металлического свинца, погруженного в 0,02 М раствор нитрата свинца. Схема рассматриваемого гальванического элемента:
 (–) Zn|Zn(NO3)2(0,1M)||Pb(NO3)2(0,02M)|Pb (+)
(–) Zn|Zn(NO3)2(0,1M)||Pb(NO3)2(0,02M)|Pb (+)
анод катод
Поскольку цинк стоит левее в ряду напряжений и является более активным металлом, он окисляется
Zn – 2e = Zn2+, т.е. этот электрод он является анодом.
На свинцовом электроде (j Pb > j Zn) происходит восстановление ионов Pb2+ + 2e = Pb, т.е. он служит катодом. За счет протекания окислительно-восстановительной реакции возникает электрический ток. Если во внешнюю цепь включить вольтметр, то он покажет определенную разность потенциалов.
ЭДС гальванического элемента рассчитывается как разность электродных потенциалов катода и анода:
Εг.э. = j катода – j анода
Чтобы определить ЭДС гальванического элемента, необходимо вычислить электродные потенциалы катода и анода. Для этого в табл. П3.7 находим значения стандартных электродных потенциалов систем: φ0Zn2+/Zn = – 0,76 B и φ0Pb2+/Pb = –0,13 В, затем рассчитываем значения j по уравнению Нернста:


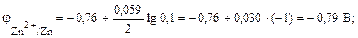
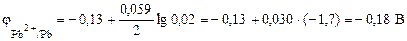
Находим ЭДС элемента:
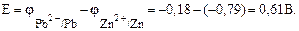
Выполнение опыта. Собрать гальванический элемент в соответствии со схемой
Zn | ZnSO4 || CuSO4 | Cu
Для этого налить в два стаканчика (рис.) 1М растворы солей: в один сульфата цинка, в другой – сульфата меди, опустить пластинки Zn в ZnSO4 и Cu в CuSO4.
Растворы соединить электролитическим мостиком, наполненным раствором NaCl в агар-агаре. Обе пластины соединить тонким проводником с гальванометром. Наблюдать отклонение стрелки гальванометра.
Записать схемы протекающих процессов, данные гальванометра и нарисовать гальванический элемент. Что произойдет, если убрать электролитический мостик? Объяснить происходящие явления.
Рассчитать ЭДС гальванических элементов:
1) Zn | 1M ZnSO4 || 0,01M АgNO3 | Ag;
2) Zn | 0,1M ZnSO4 || 1M CuSO4 | Cu;
3) Zn | 1M ZnSO4 || 0,01M ZnSO4 | Zn.
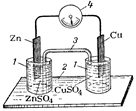
Рис 8. Гальванический элемент:
1 – стаканчики с растворами ZnSO4 и CuSO4;
2 – подставка под прибор;
3 – гальванический (электролитический) мостик;
4 – гальванометр.
 2015-04-01
2015-04-01 3110
3110
