147. Дайте определение понятию окислительно-восстановительные реакции. Какие из приведенных ниже реакций являются окислительно-восстановительными:
а) 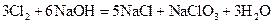 .
.
б) 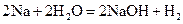 ;
;
в) 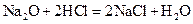 ;
;
148. Какие частицы называют восстановителями. Руководствуясь строением атомов, решите, могут ли фигурировать в качестве восстановителей следующие ионы: Sn2+, Cl–, Zn2+.
149. Дайте определение понятию степень окисления. Определите степень окисления центрального атома в следующих ионах: SO42–, SO32–, S2O32–.
150. Какие частицы называют окислителями. Укажите, какие из перечисленных ионов могут быть окислителями: Fe3+, Br–, Cr3+
151. Какие из перечисленных частиц обладают двойственной окислительно-восстановительной природой, почему?
а) N–3, N20, N+3;
б) H–1, H20, H+1;
в) Fe2+, Fe3+, Fe+6;
г) C+2, Cu+1, F–1.
152. Укажите, какие из перечисленных частиц являются только окислителями:
а) Cl+7, O20, F20;
б) N+5, S+6, Cl+3;
в) H+, Br+7, C+4;
г) Cr+6, Mn+7, Mn+4.
153. Укажите, какие из перечисленных частиц являются только восстановителями:
а) Ca0, N–3, O–1;
б) H–, I–, Na+;
в) O–2, Cu+1, C+4.
154. Окислительно-восстановительные реакции выражаются приведенными схемами:
а) P + HIO3 + H2O® H3PO4 + HI;
б) 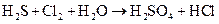 ;
;
в) KMnO4 + N2H4 + H2SO4 ® N2 + MnSO4 + K2SO4 + H2O;
г) HgS + HCl + HNO3 ® S + HgCl2 + NO + H2O;
д) FeSO4 + HNO3 ® Fe(NO3)3 + NO + H2SO4 + H2O;
е) Mg + HNO3 ® NH4NO3 + Mg(NO3)2 + H2O;
ж) 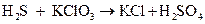 ;
;
з) 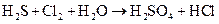 ;
;
и) 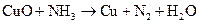 ;
;
к) 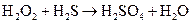 ;
;
л) 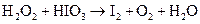
м) 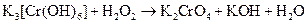 ;
;
н) 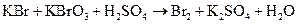 ;
;
о) 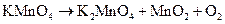 ;
;
п) 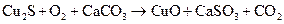 ;
;
Подберите коэффициенты в предложенных реакциях методом электронного баланса. Укажите, какое вещество в каждом взаимодействии является окислителем, какое – восстановителем.
155. Окислительно-восстановительные реакции выражаются ионными уравнениями:
а) 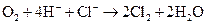 ;
;
б) 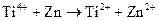 ;
;
в) 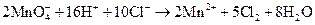 ;
;
г) 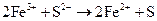 ;
;
д) 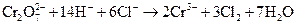 ;
;
е) 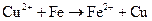
Составьте электронные и молекулярные уравнения. Для каждой реакции укажите, какой ион является восстановителем, какой – окислителем.
 2015-04-01
2015-04-01 659
659








