Движущая сила массообменных процессов. Различные вещества могут находиться в различных фазовых состояниях.
Движущая сила массообменных процессов — разность концентраций.
Основное уравнение массопередачи. Коэффициент массопередачи. Процесс переноса сахара из стружки в воду в соответствии с основным кинетическим уравнением можно описать следующим образом:
dM/(F*dτ)=k*Δ
где M — масса вещества, перешедшего из одной фазы в другую, кг; k — кинетический коэффициент, учитывающий сопротивление в процессе переноса; Δ — движущая сила; F— площадь межфазовой поверхности, через которую осуществляется перенос вещества, м2; τ — продолжительность процесса, с. Это уравнение называют основным уравнением массопередачи.
Коэффициент к получил название коэффициента массопередачи. Размерность его зависит от размерности, принятой для концентрации.
Физический смысл коэффициента массопередачи следует из его определения:
коэффициент массопередачи показывает, какое количество вещества переносится через 1 м2 поверхности фазового раздела за 1 с при разности концентраций, равной единице.
Коэффициент массопередачи не зависит от площади поверхности, времени и разности концентраций. Он зависит от свойств участвующих в процессе веществ и характера взаимодействия фаз.
Основными законами массопередачи являются закон молекулярной диффузии (первый закон Фика), закон массоотдачи (закон Ньютона — Щукарева) и закон массопроводности.
Закон молекулярной диффузии (первый закон Фика), основанный на том, что диффузия в газах и растворах жидкостей происходит в результате хаотического движения молекул, приводящего к переносу молекул распределяемого вещества из зоны высоких концентраций в зону низких концентраций,
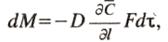
где dM — количество вещества, перенесенного путем диффузии; D — коэффициент пропорциональности, или коэффициент диффузии; С/1 — градиент концентрации в направлении диффузии; F — элементарная площадка, через которую происходит диффузия; dx — продолжительность диффузии.
Коэффициент диффузии показывает, какое количество вещества диффундирует через поверхность в 1 м2 в течение 1 ч при разности концентраций на расстоянии 1 м, равной единице.
Знак «минус» в правой части уравнения показывает, что при молекулярной диффузии концентрация убывает.
Коэффициенты диффузии зависят от агрегатного состояния систем. Для газов коэффициенты диффузии имеют значения (0,1...1,0)10~4 м2/с. Они примерно на четыре порядка выше, чем для жидкостей. С увеличением температуры коэффициенты диффузии.возрастают, а с повышением давления уменьшаются
 2015-05-05
2015-05-05 1731
1731
