При выполнении как конструкторского, так и поверочного расчета парогенератора, а также при обработке результатов балансовых испытаний для определения тепловосприятия в отдельных газоходах необходимо вычислить энтальпию продуктов сгорания, определяемую на 1 кг твердого и жидкого топлива или на 1 м3 газового топлива по формуле:
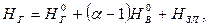
в которой энтальпия теоретического количества продуктов сгорания 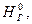 МДж/кг или МДж/м3 (a=1), при температуре J, °С,
МДж/кг или МДж/м3 (a=1), при температуре J, °С,
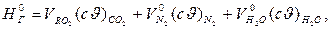
энтальпия теоретически необходимого количества воздуха 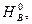 МДж/кг или МДж/м3,
МДж/кг или МДж/м3,
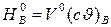
Здесь 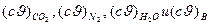 - энтальпия 1 м3 углекислоты, азота, водяного пара и влажного воздуха.
- энтальпия 1 м3 углекислоты, азота, водяного пара и влажного воздуха.
Средние теплоемкости воздуха и газов от 0 до 2500°С, кДж/(м3 К)
| T,.°С | 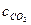
| 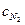
| 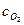
| 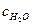
| 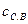
| 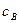
|
| 1,5998 | 1,2946 | 1,3059 | 1,4943 | 1,2971 | 1,3188 | |
| 1,9887 | 1,3276 | 1,3980 | 1,5897 | 1,3427 | 1,3683 | |
| 2,2035 | 1,3917 | 1,4775 | 1,7229 | 1,4097 | 1,4373 | |
| 2,3354 | 1,4440 | 1,5294 | 1,8527 | 1,4620 | 1,4926 | |
| 2,4221 | 1,4826 | 1,5692 | 1,9628 | 1,5010 | 1,5328 | |
| 2,4811 | 1,5114 | 1,6027 | 2,0528 | 1,5303 | 1,5638 |
Энтальпия золы 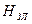 , МДж/кг,
, МДж/кг,
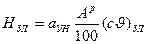
учитывается, если приведенная величина уноса золы из топки
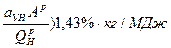
В формуле:
|
|
|
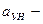 доля золы топлива, уносимая газами;
доля золы топлива, уносимая газами;
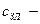 теплоемкость золы твердых топлив, включая при высоких температурах теплоту превращения из твердого в жидкое состояние, значения которой приведены в таблице “Теплоемкость золы твердых топлив”.
теплоемкость золы твердых топлив, включая при высоких температурах теплоту превращения из твердого в жидкое состояние, значения которой приведены в таблице “Теплоемкость золы твердых топлив”.
Теплоемкость золы твердых топлив
| T, °C | |||||||
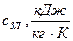
| 0,7955 | 0,8374 | 0,8667 | 0,8918 | 0,9211 | 0,9420 | 0,9504 |
| T, °C | |||||||
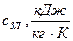
| 0,9630 | 0,9797 | 1,0048 | 1,0258 | 1,0519 | 1,0969 | 1,1304 |
| T, °C | |||||||
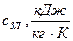
| 1,1849 | 1,2228 | 1,2979 | 1,3398 | 1,3816 | 1,4235 |
Все формулы для подсчета объемов и энтальпии относятся к случаю полного сгорания, но они с достаточной для расчетов точностью применимы также при наличии химической неполноты горения.
Расчеты теплообменников удобно выполнять с помощью Н, t – диаграммы, представляющей собой ряд линий, дающих зависимость энтальпии продуктов сгорания Нг от их температуры при различных значениях aв. Для примера на рисунке 1 построена Н, t – диаграмма для продуктов сгорания природного газа (газопровод Бухара – Урал).
 Прежде всего, по Н, t – диаграмме можно определить температуру, которую имели бы продукты сгорания при условии, что вся теплота горения затрачивается только на их нагрев, а теплопотери отсутствуют. Эта температура называется адиабатной, поскольку горение осуществляется в адиабатном процессе – изолированной системе, без теплопотерь. Если продуктов неполного сгорания нет, теплота из зоны горения не отводится и сжигание организованно в потоке (практически при р=const), то количество выделяющейся при сгорании теплоты равно энтальпии продуктов сгорания:
Прежде всего, по Н, t – диаграмме можно определить температуру, которую имели бы продукты сгорания при условии, что вся теплота горения затрачивается только на их нагрев, а теплопотери отсутствуют. Эта температура называется адиабатной, поскольку горение осуществляется в адиабатном процессе – изолированной системе, без теплопотерь. Если продуктов неполного сгорания нет, теплота из зоны горения не отводится и сжигание организованно в потоке (практически при р=const), то количество выделяющейся при сгорании теплоты равно энтальпии продуктов сгорания:
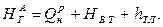
Если температура воздуха tв.т и топлива (tтл) на входе в топку равны нулю, то их энтальпии Нвт= hтл=0 и 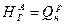 .
.
|
|
|
Откладывая на Н, t – диаграмме значение 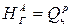 , найдем на пересечении с кривой, построенной для выбранного значения aв, соответствующую адиабатную температуру. Например, значения aв=1,25 и
, найдем на пересечении с кривой, построенной для выбранного значения aв, соответствующую адиабатную температуру. Например, значения aв=1,25 и 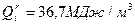 соответствует точка А на рис. 1, т.е. ta=1700°С. Естественно, адиабатная температура будет максимальной для стехиометрической смеси, т.е. для aв=1. Она называется теоретической tт. В примере на рис. 1 tт=2000°С. С увеличением aв в продуктах сгорания появляется «лишний» воздух, на нагрев которого также затрачивается теплота, поэтому адиабатная температура уменьшается. Теоретическая температура горения некоторых газообразных топлив в холодном воздухе, рассчитанная без учета диссоциации, составляет:
соответствует точка А на рис. 1, т.е. ta=1700°С. Естественно, адиабатная температура будет максимальной для стехиометрической смеси, т.е. для aв=1. Она называется теоретической tт. В примере на рис. 1 tт=2000°С. С увеличением aв в продуктах сгорания появляется «лишний» воздух, на нагрев которого также затрачивается теплота, поэтому адиабатная температура уменьшается. Теоретическая температура горения некоторых газообразных топлив в холодном воздухе, рассчитанная без учета диссоциации, составляет:
| Газ | СО | Н2 | СН4 |
| tт, °С | |||
| Газ | Коксовый | Природный | Доменный |
| tт, °С |
Действительная температура оказывается тем ниже адиабатной, чем больше теплопотери (в основном излучением) из зоны горения на холодные стены топки и в окружающую среду, и обычно отличается от нее на 20-25%. При нагреве воздуха или обогащении его кислородом адиабатная температура увеличивается.
В процессе сгорания топлива в топочных камере теплота может передаваться конвекцией и излучением нагреваемому материалу в печах или охлаждающим поверхностям в котлах. В результате газы охлаждаются, их энтальпия снижается. Этот процесс на рисунке 1 изображается линией aв= const. Например, при охлаждении в топке продуктов сгорания до 1100°С и неизменном коэффициенте избытка воздуха aв=1,25 (линия АВ) их энтальпия снижается до 22,5 МДж/м3. Теплота, отдаваемая продуктами сгорания в процессе их охлаждения (в расчете на единицу количества сгоревшего топлива), равна уменьшению их энтальпии, т.е.
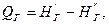 (*)
(*)
где 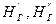 - энтальпии газов соответственно до и после теплообменника.
- энтальпии газов соответственно до и после теплообменника.
Уравнение теплового баланса (*) служит основой для расчета всех теплообменных поверхностей.
Очень часто для удаления продуктов сгорания из агрегата их отсасывают, т.е. они движутся в агрегате под разрежением. Через неплотности к ним может подсасываться атмосферный воздух. Пусть коэффициент избытка воздуха увеличится при этом от 1,25 до 1,5 (Daв=0,25). Энтальпия газов при этом практически не изменится, поскольку энтальпия подсасываемого холодного воздуха близка к нулю. Следовательно, подмешивание (присос) холодного воздуха к продуктам сгорания изобразится в Н, t – диаграмме горизонтальной линией Нг=const. В нашем примере газы охладятся за счет присоса (с 1100 до 930°С, линия ВС). Чем больше присосы, тем меньше окажется разность энтальпий при той же разности температур, поэтому из-за присосов через неплотности в газоходах, когда газ движется под разрежением, экономичности теплообменника снижается так же, как и из-за утечек части горячего газа через те же неплотности, когда газ по газоходу движется под давлением.
 | |||
 | |||
 Нг, МДж/м3
Нг, МДж/м3



















 А
А




 Д
Д
30 


 Н
Н










 С В
С В

 | |||||
 |  |
9. Вопросы для самопроверки.
1. Основные требования, предъявляемые к органическим топливам.
2. Определение энергетического топлива
3. Классификация топлив то способу получения.
4. Классификация твердых топлив то размеру кусков.
5. Бурые угли.
6. Каменные угли.
7. Классификация каменных углей.
8. Торф.
9. Сланцы.
10. Мазут.
11. Природный газ.
12. Минеральные примеси топлива.
13. Балласт топлива.
14. Зола топлива.
15. Влага топлива.
16. Выход летучих и свойства кокса.
17. Понятие условного топлива.
18. Высшая и низшая теплота сгорания топлива.
19. Закон Гесса.
20. Способы определения теплоты сгорания топлив.
21. Теоретически необходимое количество воздуха.
|
|
|
22. Коэффициент избытка воздуха.
23. Состав продуктов сгорания топлива.
24. Энтальпия продуктов сгорания.
25. Построение Н, t – диаграммы.
26. Определение адиабатной и теоретической температуры горения с помощью Н, t – диаграммы.
27. В чем отличие теоретической температуры горения от адиабатной.
10. Контрольные задачи, вынесенные на самостоятельную проработку.
Дано: Состав газообразного топлива, коэффициент избытка воздуха (см. табл.).
Найти:
1. Низшую теплоту сгорания топлива Qнр (кДж/м3);
2. Теоретически необходимое количество воздуха V0, м3/м3;
3. Действительное количество воздуха Vв, м3/м3;
4. Теоретический объем продуктов сгорания V0Г, м3/м3;
5. Общий объем продуктов сгорания VГ, м3/м3;
6. Построить Н, t – диаграмму в диапазоне температур 0-2500 оС;
7. По Н, t – диаграмме определить адиабатную температуру горения.
| Вариант | a | Газопровод | Состав, % | ||||||
| СО2 | СН4 | С2Н6 | С3Н8 | С4Н10 | С5Н12 | N2 | |||
| 1,02 | Саратов – Москва | 0,8 | 84,5 | 3,8 | 1,9 | 0,9 | 0,3 | 7,8 | |
| 1,03 | Ставрополь – Москва | 0,5 | 91,2 | 3,9 | 1,2 | 0,5 | 0,1 | 2,6 | |
| 1,04 | Дашава – Киев | 0,2 | 98,9 | 0,3 | 0,1 | 0,1 | - | 0,4 | |
| 1,05 | Шеболинка – Харьков | 0,1 | 92,8 | 3,9 | 1,0 | 0,4 | 0,3 | 1,5 | |
| 1,06 | Газли – Коган | 0,2 | 95,4 | 2,6 | 0,3 | 0,2 | 0,2 | 1,1 | |
| 1,07 | Карадаг – Тбилиси | 0,2 | 93,9 | 3,1 | 1,1 | 0,3 | 0,1 | 1,3 | |
| 1,08 | Бухара – Урал | 0,4 | 94,9 | 3,2 | 0,4 | 0,1 | 0,1 | 0,9 | |
| 1,09 | Средняя Азия – Центр | 0,6 | 93,8 | 3,6 | 0,7 | 0,2 | 0,4 | 0,7 | |
| 1,1 | Игрим – Нижний Тагил | - | 95,9 | 1,9 | 0,5 | 0,3 | 0,1 | 1,3 | |
| 1,11 | Оренбург - Совхозное | 0,7 | 92,5 | 4,1 | 1,9 | 0,6 | - | 0,2 |
12. Список использованной литературы:
1. Хзмалян Д.М. Каган Я.А. Теория горения и топочные устройства. Учебное пособие для студентов ВУЗов. М., «Энергия». 1976 г.
2. Ионин А.А. Газоснабжение. Учебник для ВУЗов. М., Стройиздат, 1989 г.
3. Баскаков А.П. Теплотехника. Учебник для ВУЗов. М., Энергоатомиздат, 1991 г.
4. Иссерлин А.С. Основы сжигания газового топлива. Справочное пособие. Л., Недра, 1987 г.
 2015-05-05
2015-05-05 2016
2016