К Ароматическим углеводородам относят циклические углеводороды, которые, несмотря на высокую степень ненасыщенности, но обнаруживаютхарактерных свойств непредельных соединений.
Типичным представителем ароматического ряда является бензол.
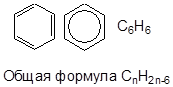
Изомерия
1. по положению заместителей
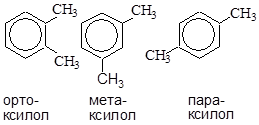
2. по боковой цепи
3. по величине радикалов (см. «Циклоалканы»)
Способы получения
1. Дегидрирование алканов и циклоалканов
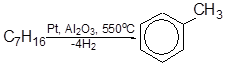
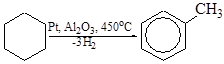
2. Сухая перегонка каменного угля
При нагревании каменного угля без доступа воздуха до 1200оС образуются летучие вещества и кокс. Газовая смесь частично конденсируется с образованием бензола и его гомологов.
3. Полимеризация алкинов
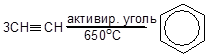
4. Реакция Вюрца
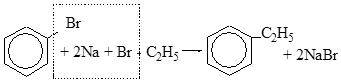
5. Реакция Фриделя-Крафтса
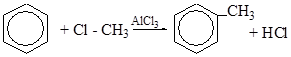
Физические свойства
Бензол – легкоподвижная жидкость с tкип = 81оС, tпл = 5оС. Бензол и алкилбензолы – малополярные соединения, легче воды, нерастворимы в ней, но хорошо растворяются в неполярных органических растворителях (эфире, хлороформе и т.п.)
Химические свойства
Характерной особенностью ароматических соединений является термодинамическая устойчивость бензольного кольца. Это объясняется образованием единого электронного облака, возникающего как результат p-p-сопряжения трёх p-связей.
Атомы углерода в бензольном кольце находятся в состоянии sp2-гибридизации:
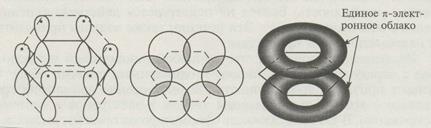
В составе общего электронного облака р-электроны не локализованы возле своих углеродных атомов, они получают большую степень свободы, что делает молекулу более устойчивой.
Вследствие этого:
- ароматические соединения не вступают в реакции присоединения (АЕ) по кратным связям, для них характерны реакции электрофильного замещения (SE).
- они достаточно устойчивы к действию окислителей (не взаимодействуют с водными растворами KMnO4)
Механизм электрофильного замещения (SE)
Механизм заключается в замене ароматически связанного атома водорода электрофильным агентом.

p-комплекс s-комплекс
Реагент, приближаясь к молекуле бензола, прежде всего, сталкивается с отрицательно заряженным p-электронным облаком, экранирующим плоскость s-связей в молекуле. При этом легче всего ядро бензола будет взаимодействовать с электрофилом (частицей с положительным зарядом), образуя p-комплекс.
В отличие от алкенов s-комплекс образует вновь энергетически выгодную ароматическую систему путем отщепления протона.
Ориентирующие действие заместителей в бензольном кольце.
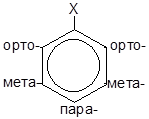
Электронная плотность ароматической системы повышается при наличии ЭД-заместителей (+М; +J), при этом облегчается атака электрофильными агентами.
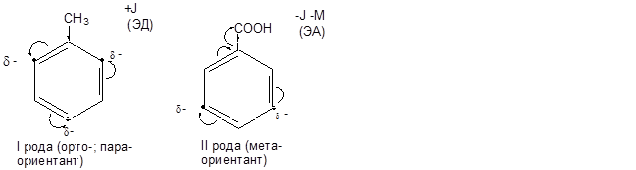
Ориентанты I рода:
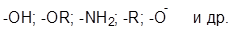
Электронная плотность ядра уменьшается при наличии ЭА-заместителей, при этом замедляется атака его электрофилами. ЭА-заместители направляют атаку электрофилом в места-положение и называются ориентантами II рода.
Ориентанты II рода:
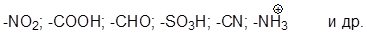
Бензол и его гомологи вступают в реакции со многими электрофильными реагентами так, что один или несколько атомов водорода бензольного кольца может замещаться на галоген, нитрогруппу, сульфогруппу, алкильный радикал и т.д.
d
 2015-05-06
2015-05-06 966
966








