| Молекула (химический элемент) | Молекулярная масса | Плотность кг/м3 | Молекула (химический элемент) | Молекулярная масса | Плотность, кг/м3 |
| С | 12,0 | 0,536 | C2H6 | 30,1 | 1,342 |
| Н2 | 2,0 | 0,090 | C3H8 | 44,1 | 1,967 |
| N2 | 28,0 | 1,251 | C4H10 | 58,1 | 2,593 |
| S | 32,0 | 1,92 | CO2 | 44,0 | 1,964 |
| O2 | 32,0 | 1,428 | SO2 | 64,1 | 2,858 |
| CO | 28,0 | 1,250 | H2O | 18,0 | 0,804 |
| CH4 | 16,0 | 0,716 | NO | 30,0 | 1,339 |
| H2S | 34, | 1,520 | NO2 | 46,0 | 2,053 |
При неполном горении углерода таким же путем образуется:
С + 1/2О2 = СО; (4.35)
12 кг С + 16 кг О2 = 28 кг СО;
1 кг С + 1,33 кг О2 = 2,33 кг СО;
т. е. при неполном сжигании 1 кг углерода, до оксида углерода, требуется 0,933 м3 кислорода и образуется 1,866 м3 оксида углерода.
Теоретическое количество воздуха для горения (V в 0 м3/кг). Для получения значений теоретического (стехиометрического) количества воздуха необходимого для полного сгорания углерода, водорода и серы в объемных единицах и с учетом содержания кислорода в воздухе в количестве 21 % об. получим выражение:
V в 0 = (2,67Ср + 8Нр + Sлр – Ор)/(21× 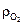 ), (4.36)
), (4.36)
или
V в 0 = 0,0889(Ср + 0,375 Sлр) + 0,265Нр - 0,033Ор, (4.37)
Выражение (4.37) используется для определения стехиометрического количества воздуха при сжигании твердых и жидких видов топлива.
При сжигании газообразного топлива количество теоретически необходимого воздуха находят, исходя из стехиометрических уравнений реакций горения компонентов газообразного топлива. При этом принимают, что объем одного моля компонентов, как и у идеальных газов, одинаков. Тогда при горении: оксида углерода
СО + 0,5О2 = СО2; (4.38)
1 м3 СО + 0,5 м3 О2 = 1 м3 СО2;
Н2 + 0,5О2 = Н2О; (4.39)
1 м3 Н2 + 0,5 м3 О2 = 1 м3 Н2О;
H2S + 1,5O2 = H2O + SO2; (4.40)
1 м3 H2S + 1,5О2 = 1 м3 Н2О + 1 м3 SО2;
С m Н n + (m + n /4)×O2 = m СO2 + (n /2)Н2O, (4.41)
при сжигании в воздухе:
С m Н n + (m + n /4)×(O2 + 3,76×N2) =
= m СO2 + (n /2)Н2O + (m + n /4)×3,76N2, (4.42)
Иначе говоря, исходя из реакций полного горения составляющих газообразного топлива, следует, что каждый 1 м3 СО требует - 0,5 м3 O2 и после реакции образуется 1 м3 СО2.
Подобные рассуждения можно повторить и для всех других составляющих газообразного топлива. Если помнить, что количество горючих газов в топливе выражено в процентах и 1 м3 О2 содержится в 4,76 м3 воздуха, м3/м3 тогда теоретическое количество воздуха будет определено:
V в0 = 0,0476[0,5СО + 0,5Н2 +1,5Н2S +
+S(m + n /4)С m Н n – О2] (4.43)
Теоретическое количество продуктов сгорания (V г0, м3/кг). Используя те же стехиометрические выражения можно определить и теоретическое количество продуктов полного сгорания, которое представляет собой сумму:
V г0 = 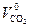 +
+ 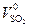 +
+ 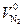 +
+ 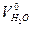 , (4.44)
, (4.44)
где 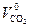 ,
, 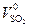 ,
, 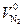 ,
, 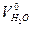 – соответственно, теоретические объемы диоксида углерода, диоксида серы, азота и водяных паров, м3/кг, теоретический объем сухих газов:
– соответственно, теоретические объемы диоксида углерода, диоксида серы, азота и водяных паров, м3/кг, теоретический объем сухих газов:
V 0c.г = 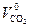 +
+ 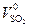 +
+ 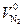 (4.45)
(4.45)
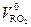 = (
= (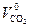 +
+ 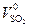 ) (4.46)
) (4.46)
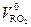 = 1,866(Ср/100) + 0,7(SРл/100) =
= 1,866(Ср/100) + 0,7(SРл/100) =
= 0,0187(Ср + 0,375Sрл) (4.47)
Основной азот поступает в топку с воздухом в количестве 79 % об., некоторое количество переходит из топлива, которого содержится в топливе не более - 1,8 %, тогда:
N2т = Nр/(100×1,251) = 0,008Nр,
V 0N2 = 0,79 V ов + 0,008Nр, (4.48)
вторым слагаемым можно пренебречь, тогда:
V оN2 = 0,79 V ов (4.49)
При этих допущениях теоретический объем сухих газов, полученных от сгорания 1 кг твердого или жидкого топлива, м3/кг, составит:
V 0c.г = 0,0187(Ср + 0,375Sрл) + 0,79 V 0в. (4.50)
Количество водяные пары, получаемое в результате окисления водорода топлива, м3/кг, составит:
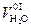 = 9Нр/(100×0,804) = 0,111Нр (4.51)
= 9Нр/(100×0,804) = 0,111Нр (4.51)
где 9 - количество воды, полученной при окислении 1 кг водорода, кг; 0,804 - плотность 1 кг водяных паров при нормальных условиях, кг/м3.
Количество водяных паров, полученных от испарения влаги топлива, м3/кг:
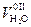 = W p/(100×0,804) = 0,0124 W p (4.52)
= W p/(100×0,804) = 0,0124 W p (4.52)
Количество влаги, содержащейся в воздухе, принимают равным 13 г на 1 кг воздуха, тогда:
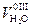 = d × V ов×rв/(1000×0,804) = 0,0161 V ов (4.53)
= d × V ов×rв/(1000×0,804) = 0,0161 V ов (4.53)
Количество влаги, вносимой в топку в виде водяных паров (например, при распыливании жидкого топлива), W ф при расходе, кг/кг, топлива определяет дополнительный объем водяных паров, м3/кг:
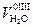 = W ф/0,804= 1,24 W ф (4.54)
= W ф/0,804= 1,24 W ф (4.54)
Полный теоретический объем водяных паров в продуктах сгорания при сжигании твердого или жидкого топлива будет суммой, определенных выше в формулах (3.22)-(3.25):
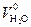 =
= 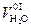 +
+ 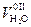 +
+ 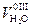 +
+ 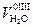 (4.55)
(4.55)
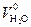 = 0,111Нр + 0,0124 W p + 0,0161 V 0в + 1,24 W ф (4.56)
= 0,111Нр + 0,0124 W p + 0,0161 V 0в + 1,24 W ф (4.56)
Теоретическое количество продуктов сгорания при сжигании газообразного топлива, м3/м3,находится из тех же условий, что были рассмотрены выше. Для трехатомных газов можно записать:
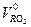 = 0,01(СО2 + СО +Н2S + S m С m Н n) (4.57)
= 0,01(СО2 + СО +Н2S + S m С m Н n) (4.57)
Объем азота в продуктах сгорания
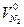 = 0,79 V 0в + 0,01N2, (4.58)
= 0,79 V 0в + 0,01N2, (4.58)
тогда сухих газов
V 0c.г = 0,01(СО2 + СО + Н2S + S m С m Н n) + 0,79 V 0в.
(4.59)
Теоретический объем водяных паров в продуктах сгорания газообразного топлива
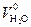 = 0,01(Н2 + Н2S + S(n /2)С m Н n + 0,124 d т) + 0,0161 V 0в (4.60)
= 0,01(Н2 + Н2S + S(n /2)С m Н n + 0,124 d т) + 0,0161 V 0в (4.60)
где d т – влажность газообразного топлива (для осушенного газа принимается 10 г/м3).
Полный теоретический объем продуктов сгорания газообразного топлива, м3/м3:
V г0 = 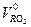 +
+ 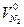 +
+ 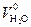 , (4.61)
, (4.61)
При приведенной величине уноса золы из топки (см. формулу 4.62) более 6 необходимо определять количество летучей золы в продуктах сгорания по выражению (4.63), кг/м3:
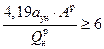 (4.62)
(4.62)
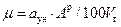 (4.63)
(4.63)
где а ун - доля золы топлива в уносе; А р - зольность топлива, %; Q рн - низшая рабочая теплота сгорания топлива, МДж/кг; V г - объем продуктов сгорания м3/кг.
Коэффициент избытка воздуха. Для полного сгорания топлива в топочные устройства подводят большее, чем теоретически необходимо, количество воздуха. Отношение действительно поступившего количества воздуха V двк теоретически необходимому количеству V 0вназывают коэффициентом избытка воздуха и обозначают через a:
a = V дв/ V 0в. (4.64)
Величина коэффициента избытка воздуха для современных топочных устройств колеблется от 1,02 (природный газа) до 1,45-1,70 (твердое топливо).
Азот N2, вводимый с воздухом в топочное устройство, не участвует в процессе горения топлива, но при высоких температурах, близких к температуре горения топлива и температуре газов на выходе из топочной камеры, и при определенных соотношениях N2/O2 дает весьма токсичные оксиды азота, вредно действующие на биосферу.
При работе котла под разрежением (давлением меньшим, чем атмосферное) внутрь котла через неплотности обмуровки и гарнитуры проникает дополнительный воздух. Этот воздух называется присосами - Da. Нормируемая, допустимая величина присосов приведена в табл. 4.5.
Таблица 4.5
Нормативные присосы воздуха по газоходам котла
| Газоходы котла | Da |
| топка с металлической обшивкой то же, без металлической обшивки то же, при тяжелой обмуровке пароперегреватель первый конвективный пучок второй конвективный пучок стальной экономайзер чугунный экономайзер с обшивкой то же, без обшивки воздухоподогреватель трубчатый на каждую ступень стальной газоход, на 10 м длины то же, кирпичный на 10 м длины | 0,05 0,08 0,10 0,03 0,05 0,10 0,08 0,10 0,20 0,05 0.01 0,05 0,1 |
Если присосы воздуха, при экспериментальном определении, больше допустимых, то принимают меры по ликвидации неплотностей, после чего вторично определяют значения присосов.
Примеры №1 и №2. Определить теоретическое и действительное количество воздуха и продуктов сгорания, а также парциальные объемы трехатомных газов. Исходные данные приведены в табл. 4.6.
Таблица 4.6
 2015-04-20
2015-04-20 590
590








