Температуры и объёмы газа, совершающего адиабатный процесс, связаны между собой соотношением
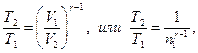
где γ – отношение теплоёмкостей газа при постоянном давлении и постоянном объёме; 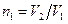 .
.
Отсюда получаем следующее выражение для конечной температуры
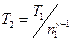 .
.
Работа газа при адиабатном расширении может быть определена по формуле
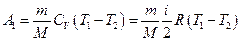 ,
,
где СV – молярная теплоёмкость газа при постоянном объёме.
Работа А2 газа при изотермическом процессе может быть выражена в виде
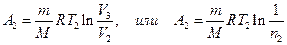 ,
,
где n2 = V2/V3.
Произведём вычисления, учитывая что для водорода как двухатомного газа γ =1,4, i =5 и M =2·10-3 кг/моль, получим
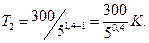
Так как 50,4=1,91 (находится логарифмированием), то
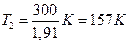 .
.
Тогда 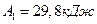 ;
; 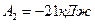 .
.
Знак минус показывает, что при сжатии работа газа совершается над внешними силами. График процесса представлен на рисунке.

Пример 5. Вычислить КПД цикла, состоящего из изобарного, адиабатного и изотермического процессов, если в результате изобарного процесса газ нагревается от Т1 =300 К до Т2 =600 К.

 Решение
Решение
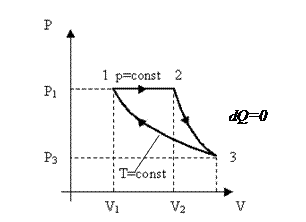
В процессе изобарного нагревания 1-2 газ расширяется за счёт поступившего от нагревателя количества тепла Q 12, в процессе адиабатного расширения 2-3 dQ =0, в процессе изотермического сжатия газ отдаёт количество теплоты Q3 1 холодильнику. КПД цикла определяется выражением
|
|
|
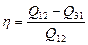 .
.
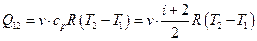 .
.
Первый закон термодинамики для процесса 3-1 имеет вид:
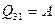 . Так как работа при изотермическом процессе равна
. Так как работа при изотермическом процессе равна
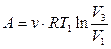 , то
, то 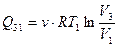 . Объём газа в состоянии 1 найдём из уравнения изобары
. Объём газа в состоянии 1 найдём из уравнения изобары 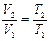 ;
; 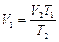 .
.
Тогда 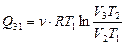 .
.
Отношение объёмов 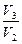 найдём из уравнения адиабаты
найдём из уравнения адиабаты
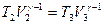 ;
; 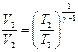 .
.
Следовательно,
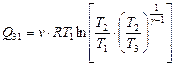
и с учётом того, что Т3 = Т1, получим
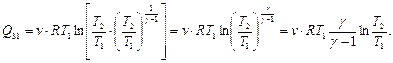 Так как
Так как 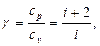 то
то 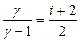 .
.
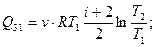
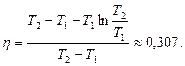
Пример 6. Найти изменение энтропии при следующих процессах:
а) при нагревании 100 г воды от 0О С до 100О С и последую- щим превращении воды в пар той же температуры;
б) при изотермическом расширении 10 г кислорода от объёма 25 л до объёма 100 л.
 2015-05-14
2015-05-14 1353
1353








