Интегрируя выражение (2) получаем DG при постоянном давлении в температурном интервале от T1 до Т2:
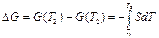 (P=const) (3)
(P=const) (3)
В уравнениях (2) и (3) S является функцией Т при постоянном давлении.
Для расчета температурной зависимости изменения свободной энергии Гиббса химической реакции
пАА + пBВ ® пCС + nDD (4)
изменение свободной энергии реакции равно:
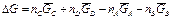
где 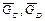 ит. д. — мольные свободные энергии соединений С, D и т. д.
ит. д. — мольные свободные энергии соединений С, D и т. д.
Взяв производные уравнения (4) по температуре при постоянном давлении, получаем
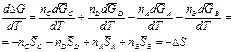 (5)
(5)
где DS – изменение энтропии реакции. Интегрируя уравнение (5), получаем
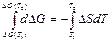
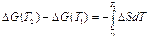 (6)
(6)
Если D S реакции не изменяется значительно в температурном интервале от Т1 до Т2, уравнение (6) дает
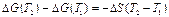
Рассмотрим другое полезное уравнение для расчета температурной зависимости DG при постоянном давлении:
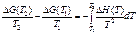
Это уравнение Гиббса—Гельмгольца. Его можно вывести, взяв дифференциал от (G/Т) по температуре при постоянном давлении:
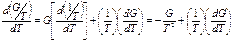
Считая 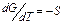 , получаем
, получаем
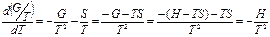 (7)
(7)
Умножив обе части уравнения (7) на Т2 и учитывая, что (dT/T2) = —d(1/T), получаем
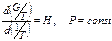 (8)
(8)
|
|
|
Для рассматриваемой химической реакции (4) из уравнений (7) и (8) следует, что
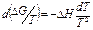 , (9)
, (9)
где D Н — изменение энтальпии реакции
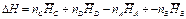
Если изменение D Н мало по всему температурному интервалу, то из уравнения (9) получаем уравнение Гиббса-Гельмгольца:
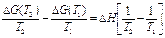 (9)
(9)
 2015-05-13
2015-05-13 753
753








