Самопроизвольное образование растворов полимеров (неограниченное или ограниченное набухание) сопровождается уменьшением изобарио-изотермического потенциала,' т. е. в результате получается термодинамически устойчивая система. Многочисленные экспериментальные данные свидетельствуют о постоянстве концентраций таких растворов, следовательно, эти растворы обладают некоторыми признаками истинных растворов. Однако основным доказательством термодинамической устойчивости растворов полимеров является подчинение их правилу фаз Гиббса.
Правило фаз — это основной закон равновесия сформулированный Гиббсом для гетерогенных систем. Правило фаз устанавливает взаимосвязь между числом фаз (r), числом компонентов в системе (п) и числом ее степеней свободы (Ф):
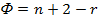
Компоненты системы — это индивидуальные вещества, наименьшее число которых достаточно для образования всех фаз данной термодинамической системы.
Число степеней свободы показывает, сколько термодинамических переменных, определяющих состояние системы (давление, температура и др), можно изменять произвольно, не вызывая изменения числа фаз в системе, т. е. не нарушая ее равновесия. Правило фаз применимо только к равновесным обратимым системам и, наоборот, применимость правила фаз является критерием обратимости и термодинамической устойчивости системы
В конденсированных системах (системы, в которых компонент находятся только в жидком и твердом состоянии) изменение давления незначительно сказывается па свойствах, поэтому давление можно считать постоянным, и уравнение принимает вид:

Согласно уравнению, двухкомпонентная однофазная конденсированная система имеет две степени свободы (состояние системы определяется температурой и концентрацией одного из компонентов).
При наличии двух фаз (r = 2) конденсированная двухкомпонентная система имеет одну степень свободы. Это значит, что изменение температуры вызывает изменение концентрации обеих фаз.1
 2015-05-26
2015-05-26 1521
1521
