Состав бинарного соединения можно выразить общей формулой Э'mЭ''n, где атом элемента (Э'') имеет отрицательную степень окисления. Названия бинарных соединений составляются из корня латинского названия электроотрицательного элемента (Э'') с окончанием ''ид'' и русского названия элемента Э' (Э' – элемент с положительной степенью окисления).
Если элемент (Э'), имеющий положительную степень окисления, может находиться в различных степенях окисления, то в скобках римскими цифрами указывается окислительное число (количественное выражение степени окисления).
Примеры бинарных соединений и их названия:
NaH – гидрид натрия, СаН2 – гидрид кальция;
CaF2 –фторид кальция, NaI – иодид натрия;
CrCl3 – хлорид хрома (III), СаС2 – карбид кальция;
Ca3N2 – нитрид кальция, SiC – карбид кремния (IV);
Al4C3 – карбид алюминия, BN – нитрид бора.
К бинарным соединениям относятся оксиды, в составе которых атомы кислорода имеют С.О., равную (-2): Al2+3O3-2, Cr+6O3-2, C+4O2-2.
Названия оксидов составляют аналогично другим бинарным соединениям, например, СаО – оксид кальция, Al2O3 – оксид алюминия, СО2 – оксид углерода (IV), CrO3 – оксид хрома (VI).
 |
При названии оксидов можно указывать греческими числительными (моно, ди, три, тетра) число атомов кислорода, приходящееся на один атом элемента в соединении, например, MnO – монооксид марганца, СО2 – диоксид углерода, СrО3 – триоксид хрома.
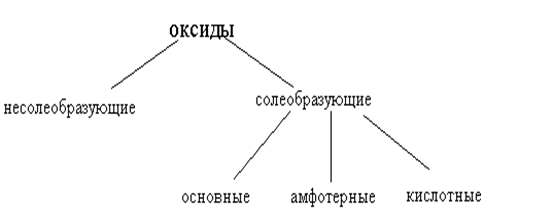
По химическим свойствам оксиды делятся на следующие типы:
Основные оксиды – соединения металлов (в низших степенях окисления) с кислородом. Им соответствуют гидроксиды, являющиеся основаниями. Оксиды щелочных и щелочноземельных металлов взаимодействуют (растворяются) с водой с образованием оснований (растворимых в воде – щелочей). Например:Na2O + H2O = 2NaOH; CaO + H2O = Ca(OH)2.
Основные оксиды остальных металлов не растворяются в воде и соответствующие им гидроксиды (основания) получают из солей реакцией обмена со щёлочью. Названия основных гидроксидов определяется названием образующих их металлов:
| Оксид | Соответствующий оксиду гидроксид | |
| Формула | Название | |
| K2O | KOH | Гидроксид калия |
| ВаО | Ва(ОН)2 | Гидроксид бария |
| Al2O3 | Al(OH)3 | Гидроксид алюминия |
| FeO | Fe(OH)2 | Гидроксид железа (II) |
| Cr2O3 | Cr(OH)3 | Гидроксид хрома (III) |
Кислотные оксиды (или ангидриды кислот)- это такие оксиды, которым соответствуют гидроксиды – кислоты. К ним относятся оксиды неметаллов (например, СО2, SO3, P2O2) и оксиды некоторых металлов в их высших степенях окисления (например, CrO3, V2O5, Mn2O7).
Кислотные оксиды можно рассматривать как продукты дегидратации (отщепления воды) кислот (ангидриды). Например:
| Кислота | Ангидрид кислоты |
| H2C+4 O3 | C+4O2 |
| H2S+6O4 | S+6O3 |
| HN+5O3 | N2+5O5 |
| H3P+5O4 | P2+5O5 |
Таким образом, зная формулу кислотного оксида, можно легко вывести формулу соответствующей кислоты и наоборот, зная формулу кислоты, можно написать формулу соответствующего ангидрида.
Амфотерные оксиды – такие оксиды, которые в зависимости от условий проявляют и основные, и кислотные свойства, т.е. могут взаимодействовать как с кислотами, так и с основаниями. К ним относятся оксиды цинка - ZnO, алюминия – Al2O3, хрома (III) – Cr2O3, марганца (IV) – MnO2 и др.
Оксиды основные, кислотные, амфотерные называются солеобразующими. Все они способны образовывать соли при взаимодействии с кислотами или основаниями. Есть небольшая группа оксидов, которые не способны образовывать соли. Они называются несолеобразующими, или индифферентными (NO, CO).
УПРАЖНЕНИЕ 3.
Какие из перечисленных оксидов относятся к основным? К кислотным? К амфотерным? P2O5, CaO, Na2O, Mn2O7, Ni2O3, ZnO, Al2O3, SiO2. Запишите формулы соответствующих им гидроксидов и укажите, какие из них являются основаниями, какие - кислотами, какие проявляют амфотерные свойства. Какие из перечисленных оксидов могут использоваться в качестве осушителей?
ОТВЕТ К основным оксидам относятся оксиды металлов при невысоких степенях окисления. Из приведенных оксидов основными являются: СаО, Na2O, Ni2O3, FeO.
К кислотным относятся: P2O5, Mn2O7, SiO2, т.к. P2O5 и SiO2 – это оксиды неметаллов, а Mn2O7 – оксид марганца в высшей С.О. (+7). Оксиды ZnO и Al2O3 относятся к амфотерным.
Гидроксиды Са(ОН)2, Fe(OH)2, NaOH, Ni(OH)2 – основания; гидроксиды Н3РО4, HMnO4 и H2SiO3 – кислоты; Zn(OH)2 и Al(OH)3 – имеют амфотерный характер.
В качестве осушителей могут использоваться оксиды: Р2О5, СаО, Na2O, т.к. они активно взаимодействуют с водой.
ЗАДАНИЕ 4 (для самоконтроля)
1. Какие основания соответствуют следующим оксидам: Ag2O, MgO, Cu2O, CrO?
2. Каким кислотам соответствуют следующие ангидриды: N2O5, Cl2O7, SO2, CrO3, SiO2?
3. Какие оксиды соответствуют следующим гидроксидам: Cr(OH)3, Zn(OH)2, LiOH, Ba(OH)2?
4. Какие из приведенных оксидов ZnO, FeO, Al2O3, CaO, P2O3, Cr2O3, Mn2O7 обладают амфотерными свойствами?
5. Какие из оксидов: Fe2O3, CaO, MgO, SO3, P2O5, Na2O, CO2, MnO взаимодействуют с водой?
6. Какие оксиды соответствуют следующим кислотам: H2SO3, HNO2, HPO3, H3PO4, H2CrO4?
7. Какие из перечисленных оксидов могут использоваться в качестве осушителей: CaO, SiO2, CuO, P2O5, Fe2O3?
8. Какие из перечисленных выше оксидов (п.7) могут быть использованы для осушки углекислого газа?
9. Каждому основанию соответствует основной оксид – оксид металла. Можно ли утверждать, что всякому оксиду металла соответствует основание? Почему?
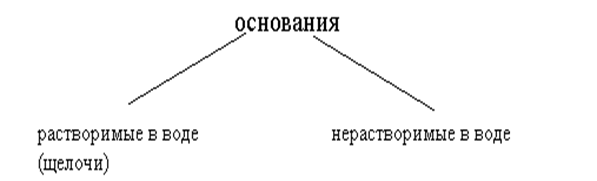 |
§ 5. ОСНОВАНИЯ (КЛАССИФИКАЦИЯ, НОМЕНКЛАТУРА)
Растворимые в воде основания – гидроксиды щелочных и щелочно-земельных металлов и аммония. Например, NaOH, KOH, Ca(OH)2, NH4OH. Нерастворимые основания составляют подавляющее большинство. Номенклатуру оснований смотрите в § 4.
Для некоторых основных гидроксидов приняты технические названия: едкий натр (гидроксид натрия) - NaOH, едкий калий (гидроксид калия) - КОН, едкий барий (гидроксид бария) – Ва(ОН)2.
ЗАДАНИЕ 5 (для самоконтроля).
1. Дайте названия следующим гидроксидам: Fe(OH)3, Zn(OH)2, LiOH, Sn(OH)4
2. Запишите формулы отвечающих им оксидов и укажите их характер.
3. Запишите формулы: а) гидроксида Mn (IV); б) дигидроксида олова. Как их можно назвать иначе?
4. Пользуясь таблицей растворимости, укажите, какие из оснований: а) Fe(OH)2, Cu(OH)2, NaOH, Al(OH)3, RbOH; б) LiOH, Co(OH)2, KOH, Ba(OH)2, Ni(OH)2 являются щелочами?
 2015-06-26
2015-06-26 5727
5727
