
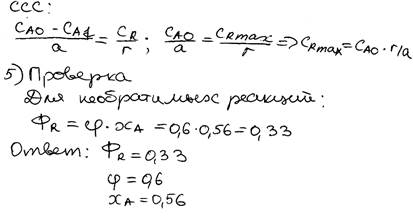
2) Анализ способов увеличения равновесной степени превращения реагентов при проведении обратимых химических реакций. Связь равновесной степени превращения и константы равновесия.
Степень превращения реагента показывает, насколько полно в химико-технологическом процессе используется исходное сырье.
Степень превращения – это доля исходного реагента, использованного на химическую реакцию. Степень превращения реагента А:
xA=∆CA/CA0=CA0-CA/CA0.
CA0 – концентрация реагента А в исходной реакционной смеси; CA – концентрация реагента А в реакционной смеси, выходящей из аппарата или находящейся в реакторе; ∆CA – изменение концентрации реагента А в ходе химической реакции.
Чаще всего в химической реакции участвует не один, а два реагента:
А+В→R
xA= CA0-CA/CA0
xВ= CВ0-CВ/CВ0
Уравнение материального баланса-система стехиометрических соотношений (ССС).
Если протекает реакция: aA+bB→rR+sS,
то в соответствии с ее стехиометрическим уравнением изменения концентраций ее участников ∆Cj связаны между собой соотношениями:
CA0-CA/a= CВ0-CВ/b=CR-CR0/r=CS-CS0/s
Если отсутствуют продукты в исходной смеси, тоCR0=0, CS0=0.
(СA0-CA)CA0/(a*CA0)=(СB0-CB)CB0/(b*CB0)
CA0*xA/a=CB0*xB/b – уравнение связи двух исходных реагентов
0≤x≤1
Не всегда можно достичь полного использования реагента (т.е. х=1). Большинство химических реакций обратимы. Для обратимых реакций предельным является состояние химического равновесия. Этому состоянию соответствует и предельно достижимая при данных условиях равновесная степень превращения:
xAе=∆CAе/CA0=CA0-CAе/CA0
CAе – концентрация реагента А в условиях равновесия; ∆CAе – изменение концентрации реагента А к моменту наступления равновесия (максимально возможное при данных условиях осуществления химической реакции).
Равновесной степенью превращения xAе называется степень превращения исходных веществ в продукты реакции, отвечающая состоянию устойчивого равновесия системы. Равновесная степень превращения характеризует глубину протекания процессов, степень приближения его результатов к оптимальным в данных условиях. Она функционально связана с константой равновесия, характер этой зависимости определяется порядком реакции.
Рассмотрим реакцию:
А↔(k1, k2) R
Скорость прямой реакции: w=k1*CA
Скорость обратной реакции: w=k2*CR
Из условия равенства скоростей прямой и обратной реакции в момент химического равновесия:
k1*CAe=k2*CRe
получаем
k1/k2=CRe/CAe
Отношение констант скоростей прямой и обратной реакции называется константой равновесия КС.
КС= k1/k2=CRe/CAe
Константа равновесия не зависит от концентрации, так как изменение концентрации одного из участников реакции вызовет такие изменения концентрации всех остальных веществ, что КС сохранит свое числовое значение.
По определению степени превращения:
САе=СА0(1-хАе)
САе=СА0 – СА0*хАе
СА0*хАе=СА0 - САе
Согласно ССС:
(СА0 - САе)/а=(СRe – СR0)/r
a=r=1
CR0=0
СА0 - САе=CRe= СА0*хАе
Тогда КС= k1/k2=CRe/CAe=СА0*хАе/ СА0(1-хАе)=хАе/(1-хАе)
КС=хАе/(1-хАе)
Для реакции:
aA+bB↔rR+sS
w=k1*CAa*CBb – скорость прямой реакции
w=k2*CRr*CSs – скорость обратной реакции
Из условия равенства скоростей прямой и обратной реакции в момент химического равновесия:
k1*CAеa*CBеb = k2*CRеr*CSеs
получаем k1/k2= CrRe * CsSe / CaAe * CbBe
Kc= k1/k2= CrRe * CsSe / CaAe * CbBe
Влияние изменения внешних условий на положение равновесия отражает принцип Ле Шателье: при смещении равновесия и переходе в новое равновесное состояние система ослабляет результат первоначального воздействия, которое вывело ее из равновесного состояния.
Влияние параметров:
1 ) температуры
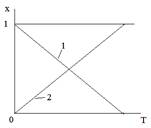
1 – для экзотермической реакции
2 – для эндотермической реакции
Так как К = ƒ(Т), то и хАе зависит от температуры. Характер этой зависимости определяется знаком теплового эффекта реакции. Для эндотермической реакции повышение температуры сдвигает равновесие в сторону образования продуктов реакции, т.е. увеличивается степень превращения, в случае экзотермической реакции – наоборот.
A↔R+Q, ∆H<0
Если Т↑, то система ослабляет результат первоначального воздействия – смещение в сторону поглощения тепла (влево). Следовательно Кс↓.
Если Т↓ - смещение равновесия в сторону выделения тепла (вправо).
Эндотермические реакции:
A↔R-Q, ∆H>0
Если Т↑, то смещение в сторону поглощения тепла (вправо). Следовательно Кс↑
Если Т↓, то в сторону выделения тепла (влево).
Зависимость константы равновесия от температуры при постоянном давлении определяется уравнением изобары Вант-Гоффа:
(d lnKp/dT)p=∆H/RT2
∆H – изменение энтальпии.
При ∆H>0 (эндотермические реакции) d lnKp/dT>0 и Кр(Т) – возрастает с повышением температуры. Если ∆H<0 (экзотермические реакции), то d lnKp/dT<0 и константа равновесия уменьшается с повышением температуры.
Для процессов, протекающих при постоянном объеме – уравнение изохоры Вант-Гоффа:
(d lnKс/dT)V=∆U/RT2
∆U – изменение внутренней энергии.
2 ) давление
Изменение давления существенно влияет на состояние равновесия в газообразных системах. Характер влияния давления определяется знаком разности числа молей газообразных участников реакции или знаком изменения объема.
Здесь возможны три случая:
– Объем газообразной системы уменьшается (ΔV<0), например, в реакции
2A↔R, ∆V=VR-VA<0
В этом случае повышение давления смещает равновесие в сторону образования продуктов
реакции.
– Объем газообразной системы увеличивается (ΔV>0), например, в реакции
A↔2R
В этом случае смещение равновесия в сторону образования продуктов реакции достигается понижением давления.
– Объем газообразной системы не изменяется, например, в реакции
A↔R
В этом случае изменение давления не влияет на равновесную степень превращения, а только на скорость реакции.
Введение инертного газа равносильно уменьшению общего давления системы (все наоборот по отношению к Р). Поэтому в технологических процессах, сопровождаемых химическими реакциями, для которых ∆V<0, стремятся к уменьшению накопления инертных газов в системе (для смещения равновесия вправо).
3) концентрации
Изменение концентрации (парциального давления) реагирующих веществ и продуктов реакции существенно влияет на состояние равновесия систем. При этом повышение концентрации исходных веществ смещает равновесие в сторону образования продуктов реакции и повышает равновесную степень превращения. Аналогично влияет уменьшение концентрации продуктов реакции, т.е. вывод их из равновесной системы. Так, например, для реакции
СО + Н2О = СО2 + Н2
равновесная степень превращения и, следовательно, равновесное парциальное давление водорода возрастает с увеличением парциального давления паров воды и понижением парциального давления двуокиси углерода.
A↔R
увеличение СА↑ сдвигает равновесие вправо, хАе ↑
уменьшение СR↓ сдвигает равновесие вправо, хАе ↑
 2015-08-13
2015-08-13 14831
14831
