Электролитическая диссоциация слабой азотистой кислоты и слабого гидроксида аммония протекают в одну ступень обратимо и характеризуются соответствующими константами диссоциации (табл. 4.4).
Двухосновные слабые кислоты и двухкислотные слабые основания диссоциируют в две ступени и имеют две константы диссоциации. Ступеней и констант диссоциации столько, какова валентность кислотного или основного многовалентного остатка.
Первая ступень диссоциации угольной кислоты ─ Н2СО3: I. Н2СО3<══> Н+ + НСО3─ ; КI Н2СО3= 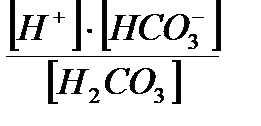 . Вторая ступень диссоциации Н2СО3: II. НСО3─ <══> Н+ + СО32─;KII Н2СО3 = . Вторая ступень диссоциации Н2СО3: II. НСО3─ <══> Н+ + СО32─;KII Н2СО3 = 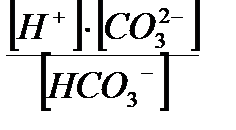 . Первая ступень диссоциации гидроксида железа (II) ─ Fe(OH)2: I. Fe(OH)2<══>FeOH+ + ОН─; КIFe(OH)2 = . Первая ступень диссоциации гидроксида железа (II) ─ Fe(OH)2: I. Fe(OH)2<══>FeOH+ + ОН─; КIFe(OH)2 = 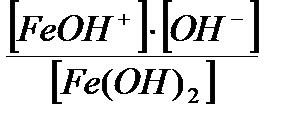 . Вторая ступень диссоциации Fe(OH)2: II. FeOH+<══>Fe2++ ОН─ ;KIIFe(OH)2 =. . Вторая ступень диссоциации Fe(OH)2: II. FeOH+<══>Fe2++ ОН─ ;KIIFe(OH)2 =. 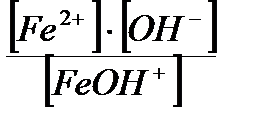 |
 2015-09-06
2015-09-06 5030
5030
