Процесс сворачивания полипептидной цепи в правильную пространственную структуру получил название "фолдинг белков".
В клетке концентрация белков настолько высока, что существует большая вероятность взаимодействия белков с несформированной конформацией. На их поверхности располагаются гидрофобные радикалы, склонные к объединению. Поэтому на время формирования нативной конформации реакционно-способные аминокислотные остатки одних белков должны быть отделены от таких же групп других белков. Всвязи с этим для многих белков, имеющих высокую молекулярную массу и сложную пространственную структуру, фолдинг протекает при участии специальной группы белков, которые называют "шапероны" (от франц. shaperon - няня), белки, способные связываться с белками, находящимися в неустойчивом, склонном к агрегации состоянии.
В соответствии с молекулярной массой все шапероны можно разделить на 6 основных групп:
· высокомолекулярные, с молекулярной массой от 100 до 110 кД;
· Ш-90 - с молекулярной массой от 83 до 90 кД;
· Ш-70 - с молекулярной массой от 66 до 78 кД;
· Ш-60;
· Ш-40;
· низкомолекулярные шапероны с молекулярной массой от 15 до 30 кД.
Среди шаперонов различают:
1) конститутивные белки (синтез которых не зависит от стрессовых воздействий на клетки организма),
2) индуцибельные, синтез которых в нормальных условиях идёт слабо, но при стрессовых воздействиях на клетку резко увеличивается. Индуцибельные шапероны относят к "белкам теплового шока", быстрый синтез которых отмечают практически во всех клетках, которые подвергаются любым стрессовым воздействиям. Название "белки теплового шока" возникло в результате того, что впервые эти белки были обнаружены в клетках, которые подвергались воздействию высокой температуры.
Фолдинг белков:
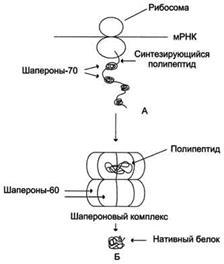
Для формирования конформации белка нужна его полная аминокислотная последовательность. Поэтому в период синтеза белка на рибосоме защиту реакционно-способных радикалов (особенно гидрофобных) осуществляют Ш-70.
Ш-70 -высококонсервативный класс белков, который присутствует во всех отделах клетки: цитоплазме, ядре, ЭР, митохондриях. В области карбоксильного конца единственной полипептидной цепи шаперонов есть участок, образованный радикалами аминокислот в форме бороздки. Он способен взаимодействовать с участками белковых молекул и развёрнутых полипептидных цепей длиной в 7-9 аминокислот, обогащённых гидрофобными радикалами. В синтезирующейся полипептидной цепи такие участки встречают примерно через каждые 16 аминокислот.
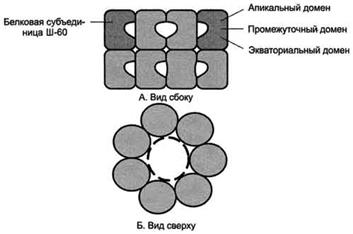
Фолдинг многих высокомолекулярных белков, имеющих сложную конформацию (например, доменное строение), осуществляется в специальном пространстве, сформированном Ш-60 (шаперонин GROEL). Ш-60 функционируют в виде олигомернoго комплекса, состоящего из 14 субъединиц. Ш-60 образуют 2 кольца, каждое из которых состоит из 7 субъединиц, соединённых друг с другом. Субъединица Ш-60 состоит из 3 доменов: апикального (верхушечного), промежуточного и экваториального. Верхушечный домен имеет ряд гидрофобных остатков, обращённых в полость кольца, сформированного субъединицами. Экваториальный домен имеет участок связывания с АТФ и обладает АТФ-азной активностью, т.е. способен гидролизовать АТФ до АДФ и Н3РО4.
Шапероновый комплекс имеет высокое сродство к белкам, на поверхности которых есть элементы, характерные для несвёрнутых молекул (прежде всего участки, обогащённые гидрофобными радикалами). Попадая в полость шаперонового комплекса, белок связывается с гидрофобными радикалами апикальных участков Ш-60. В специфической среде этой полости, в изоляции от других молекул клетки происходит перебор возможных конформации белка, пока не будет найдена единственная, энергетически наиболее выгодная конформация.
Высвобождение белка со сформированной нативной конформацией сопровождается гидролизом АТФ в экваториальном домене. Если белок не приобрёл нативной конформации, то он вступает в повторную связь с шапероновым комплексом. Такой шаперонзависимый фолдинг белков требует затрат большого количества энергии.
 2015-10-16
2015-10-16 2232
2232
