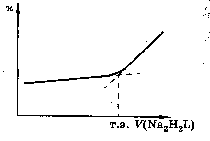Для кондуктометрического титрования катионов в качестве титрантов могут быть
использованы растворы различных кислот и оксикислот (щавелевой, винной, лимонной и др.), комплексонов.
Наибольшее практическое значение имеет кондуктометрическое титрование катионов двузамещенной солью этилендиаминтетрауксусной кислоты (ЭДТА).
При титровании, например, Fe3+ раствором ЭДТА протекает реакция:
Fe3+ + Н2 Y2- = Fe Y- + 2Н+,
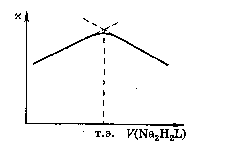
в результате которой выделяются ионы Н+ и растет электрическая проводимость раствора. После точки эквивалентности электрическая проводимость раствора падает, так как выделившиеся ионы Н+ связываются анионом Н2 Y2-
Н+ + Н2 Y2- = Н3 Y-
Кривая титрования показана на рис.5.
|
Несколько иной вид имеет кривая титрования катиона в буферном растворе (рис. 6). Выделяющиеся ионы Н+ в этом случае взаимодействуют с протоноакцепторным компонентом буферной системы и поэтому не дают заметного вклада в электрическую проводимость раствора. До точки эквивалентности электрическая проводимость раствора несколько увеличивается. Это связано с увеличением концентрации ионов Na+, вводимых с титрантом. После точки эквивалентности электрическая проводимость резко возрастает, т.к. в растворе увеличивается концентрация титранта.
|
 2014-02-12
2014-02-12 2246
2246