Билет № 1
Вопрос № 2
Экстракция. Равновесие в системах жидкость – жидкость. Методы экстракции.
ЭКСТРАКЦИЯ
Физическая сущность процесса экстракции
Экстракцией называют процесс разделения смеси компонентов, входящих в состав твердой или жидкой фаз, путем обработки их жидким растворителем.
Жидкие нефтепродукты впервые были разделены при помощи растворителя А. М. Бутлеровым в 1870 г. Этот процесс разделения был использован впоследствии К. В. Харичковым [41] для так называемой холодной фракционировки нефтепродуктов. В дальнейшем процесс экстракции получил широкое промышленное распространение при очистке масел, дизельных топлив, керосина; для выделения ароматических углеводородов, при извлечении озокерита и церезина из песчаных пород, насыщенных этими веществами, и т. д.
Разделение при помощи экстракции основано на использовании растворителей, обладающих способностью избирательно растворять одни компоненты и не растворять или ограниченно растворять другие.
В результате контакта растворителя с разделяемой смесью образуются две жидкие фазы или жидкая и твердая фазы, между которыми распределяется извлекаемое вещество.
При экстракции состояние равновесия фаз в общем случае характеризуется законом равновесного распределения
с1/с2=К (10. 1)
где с1 и с2 — соответственно концентрации извлекаемого вещества
в образующихся при экстракции фазах; К — коэффициент распределения, зависящий от природы компонентов системы, состава и температуры.
Значение коэффициента К определяют экспериментально, и для данной системы он является величиной постоянной.
В промышленных условиях при разделении жидкого нефтяного сырья используют такие растворители, как фурфурол, фенол, жидкий сернистый ангидрид, диэтиленгликоль и др.
озокерита и церезина из горных пород в качество растворителя обычно применяют бензин.
При выборе растворителя необходимо учитывать его избирательность и растворяющую способность. Чем больше избирательность растворителя, тем выше четкость разделения компонентов, т. е. тем больше коэффициент распределения К [уравнение (10.1)]. Чем выше растворяющая способность растворителя, тем большее количество извлекаемых компонентов может быть в нем растворено и тем, следовательно, меньше расход растворителя. Оба эти свойства растворителя для данной разделяемой смеси зависят от температуры экстракции. При повышении температуры избирательность растворителя уменьшается, а его растворяющая способность возрастает. При понижении температуры наблюдается обратная зависимость.
Разделение при помощи процесса экстракции может быть осуществлено только при условии, что смесь растворителя и разделяемого вещества образует двухфазную систему, что обеспечивается соответствующим выбором температуры экстракции и соотношения между количеством растворителя и разделяемой смеси. При небольшом расходе растворителя последний полностью растворяется в исходной смеси, образуя одну фазу. При большем расходе растворителя исходная смесь растворяется в растворителе, также образуя одну фазу.
Каждому количественному соотношению растворитель — исходная разделяемая смесь соответствует определенное значение температуры, при которой н выше которой данная смесь образует однофазную систему.
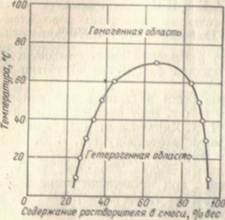 |
На рис. 10. 1 приведена кривая растворимости, устанавливающая связь между температурой растворения и составом смеси растворителя и исходного сырья. Избирательность и растворяющая способность растворителя, так же как и температура полного растворения, могут быть в известной степени изменены включением в систему растворитель — разделяемая смесь дополнительного компонента, влияющего на взаимно растворимость исходной системы.
Повышение температуры растворения, понижение растворяющей способности растворителя и повышение его избирательности могут быть достигнуты добавлением в систему компонента, который хорошо растворяется в растворителе и не растворяется или плохо растворяется в исходной разделяемой смеси. Такой метод понижения взаимной растворимости компонентов широко применяется при очистке масел фенолом с использованием воды в качестве дополнительного компонента.
Для повышения взаимной растворимости компонентов, понижения температуры растворения и избирательности растворителя в систему добавляют компонент, хорошо растворяющийся как в растворителе, так и в исходной смеси. Такова роль бензола при очистке масел жидким сернистым ангидридом.
При экстракции необходимо обеспечить интенсивное контактирование растворителя с исходной смесью, что способствует приближению системы к состоянию равновесия, а затем разделение образующихся фаз.
Скорость расслаивания в основном зависит от разности плотностей образовавшихся при экстракции фаз, степени дисперсности и вязкости среды, что в конечном счете зависит от природы растворителя и разделяемого сырья и от температуры экстракции.
Процессы и аппараты химической технологии, Скобло А.И., Москва, 1961,стр. 269-271
Процессы и аппараты химической технологии, Дытнерский Ю.И. том 1, Москва, Химия, 2002, стр. 145, 153-157
Процессы в системах жидкость-жидкость находят широкое применение в хим. н/п и н/х и других отраслях пром-ти.
Экстракция в системе жидкость-жидкость представляет собой диффузионный процесс, протекающий с участием двух взаимно нераст-ых или ограниченно раст-ых жидких фаз м/у которыми распределяется в-во (или несколько в-в).
Для повышения скорости процесса исходный р-р и экстрагент приводят в тесный контакт осуществляемый обычно многократно.в результате взаимодействия фаз получают экстракт - р-р извлеченных в-в в экстрагенте и рафинат - остаточный исходный р-р, из которого с той или иной степенью полноты удалены экстрагируемые компоненты. Полученные жидкие фазы (экстракт и рафинат) отделяются друг от друга отстаиванием, иногда центрифугированием или другими механическими способами. После этого производят извлечение целевых продуктов из экстракта и регенерацию экстрагента из рафината.
Фазовое равновесие в системе ж-ж определяет предельные концентрации экстракта и рафината. Данные о равновесии необходимы при выборе экстрагента, технологической схемы процесса, конструкции и размера (высоты и длины) апп., для расчета оптимального соотношения потоков экстрагента и исходного раствора, а также для выяснения других условий проведения процесса.
Состояние равновесия в системе ж-ж определяется равенством хим. потенциалов распределяемого в-ва в обеих фазах.
Количественно равновесие выражают двумя способами. Обычно его характеризуют отношением равновесных концентраций распределяемого в-ва в фазах, или коэффициентом распределения:
m=у*/х,
где у* и х – равновесные концентрации распределяемого в-ва в экстракте и рафинате.
 2015-01-21
2015-01-21 4225
4225