Химическое обменное взаимодействие ионов растворенной соли с водой, приводящее к образованию слабодиссоциирующих продуктов (молекул слабых кислот или оснований, анионов кислых или катионов основных солей) и сопровождающееся изменением рН среды, называется гидролизом.
Пример 1. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: a) KCN, б) Na2СО3, в) ZnSO4. Определите реакцию среды растворов этих солей.
Решение, а) Цианид калия KCN – соль слабой одноосновной кислоты (см. табл. 9) HCN и сильного основании КОН. При растворении в воде молекулы KCN полностью диссоциируют на катионы К+ и анионы CN–. Катионы К+ не могут связывать ионы ОН– воды, так как КОН – сильный электролит. Анионы же CN– связывают ионы Н+ воды, образуя молекулы слабого электролита HCN. Соль гидролизуется, как говорят, по аниону. Ионно-молекулярное уравнение гидролиза
CN– + H2O 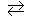 HCN + OH–
HCN + OH–
или в молекулярной форме
KCN + Н2О 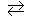 HCN + КОН
HCN + КОН
В результате гидролиза в растворе появляется некоторый избыток ионов ОН–, поэтому раствор KCN имеет щелочную реакцию (рН >7).
б) Карбонат натрия Na2СО3 – соль слабой многоосновной кислоты и сильного основания. В этом случае анионы соли CO2–3, связывая водородные ионы воды, образуют анионы кислой соли НСО–3, а не молекулы Н2СО3, так как ионы НСО3 диссоциируют гораздо труднее, чем молекулы Н2СО3. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза:
CO2–3 + Н2О 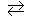 НCO–3 +ОН–
НCO–3 +ОН–
или в молекулярной форме
Na2CO3 + H2O 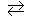 NaHCO3 + NaOH
NaHCO3 + NaOH
В растворе появляется избыток ионов ОН–, поэтому раствор Na2CО3 имеет щелочную реакцию (рН > 7).
в) Сульфат цинка ZnSO4 – соль слабого многокислотного основания Zn(ОН)2 и сильной кислоты H2SO4. В этом случае катионы Zn2+ связывают гидроксильные ионы воды, образуя катионы основной соли ZnOH+. Образование молекул Zn(OH)2 не происходит, так как ионы ZnOH+ диссоциируют гораздо труднее, чем молекулы Zn(OH)2. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
Zn2+ + Н2О 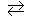 ZnOH+ + Н+
ZnOH+ + Н+
или в молекулярной форме:
2ZnSO4 + 2Н2О 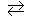 (ZnOH)2SO4 + H2SO4
(ZnOH)2SO4 + H2SO4
В растворе появляется избыток ионов водорода, поэтому раствор ZnSO4 имеет кислую реакцию (pH < 7).
Пример 2. Какие продукты образуются при смешивании растворов А1(NO3)3 и К2СО3? Составьте ионно-молекулярное и молекулярное уравнения реакции.
Решение. Соль А1(NО3)3 гидролизуется по катиону, а К2СО3 – по аниону:
Al3+ + Н2О 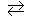 АlOН2+ + Н+
АlOН2+ + Н+
CO2–3 + H2O 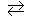 HCO3+ + OH–
HCO3+ + OH–
Если растворы этих солей находятся в одном сосуде, то идет взаимное усиление гидролиза каждой из них, ибо ионы Н+ и ОН– образуют молекулу слабого электролита Н2О. При этом гидролитическое равновесие сдвигается вправо и гидролиз каждой из взятых солей идет до конца с образованием А1(ОН)3 и СО2(Н2СО3). Ионно-молекулярное уравнение:
2А13+ + 3CO2–3 + 3Н2О = 2Аl(ОН)3 + 3СО2
молекулярное уравнение:
2Al(NO3)3 + 3К2СО3 + ЗН2O =2А1(ОН)3 + 3СО2 + 6KNO3
Контрольные вопросы
201. Составьте ионно-молекулярное и молекулярное уравнения совместного гидролиза, происходящего при смешивании растворов K2S и СrСl3. Каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты.
202. К раствору FeCl3 добавили следующие вещества: a) HCl; б) КОН; в) ZnCl2; г) Na2СОз. В каких случаях гидролиз хлорида железа (III) усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей.
203. Какие из солей Al2(SO4)3, K2S, Pb(NO3)2, КСl подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Какое значение рН (> 7<) имеют растворы этих солей?
204. При смешивании растворов FeCl3 и Na2СО3 каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты.
Выразите этот совместный гидролиз ионно-молекулярным и молекулярным уравнениями.
205. К раствору Nа2СО3 добавили следующие вещества: a) HCl; б) NaOH; в) (NО3)2; г) K2S. В каких случаях гидролиз карбоната натрия усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей.
206. Какое значение рН (> 7 <) имеют растворы солей Na2S, А1Сl3, NiSO4? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
207. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей Pb(NO3)2, Na2CO3, Fe2(SO4)3. Какое значение рН (> 7 <) имеют растворы этих солей?
208.Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей НСООК, ZnSО4, А1(NO3)3. Какое значение рН (> 7 <) имеют растворы этих солей?
209.Какое значение рН (> 7 <) имеют растворы солей Na3PO4, K2S, CuSO4? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
210.Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей CuCl2, Сs2СО3, Сr(NО3)3. Какое значение рН (> 7<) имеют растворы этих солей?
211.Какие из солей RbCl, Сr2(SО4)3, Ni(NО3)2, Na2SO3 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Какое значение рН (> 7<) имеют растворы этих солей?
212.К раствору Al2(SO4)3 добавили следующие вещества: а) Н2SО4; б) КОН, в) Na2SO3; г) ZnSO4. В каких случаях гидролиз сульфата алюминия усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей.
213.Какая из двух солей при равных условиях вбольшей степени подвергается гидролизу: Na2СО3 или Na2SO3; FеС13 или FeCl2? Почему? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
214.При смешивании растворов A12(SO4)3 и Na2CO3 каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты. Составьте ионно-молекулярное и молекулярное уравнение происходящего совместного гидролиза.
215.Какие из солей NaBr, Na2S, K2CO3, CoCl2 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Какое значение рН (> 7 <) имеют растворы этих солей?
216.Какая из двух солей при равных условиях в большей степени подвергается гидролизу: NaCN или NaClO; MgCl2 или ZnCl2? Почему? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
217.Составьте ионно-молекулярное и молекулярное уравнения гидролиза соли, раствор которой имеет: а) щелочную реакцию; б) кислую реакцию.
218.Какое значение рН (>7<) имеют растворы следующих солей: К3РО4, Pb(NO3)2, Na2S? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей.
219.Какие из солей К2СО3, FeCl3, K2SO4, ZnCl2 подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Какое значение рН (> 7 <) имеют растворы этих солей?
220.При смешивании растворов Al2(SO4)3 и Na2S каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты. Выразите этот совместный гидролиз ионно-молекулярным и молекулярным уравнениями.
 2015-05-14
2015-05-14 1743
1743
