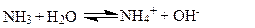 |
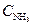 = 0.06 = 6×10-2 М
= 0.06 = 6×10-2 М
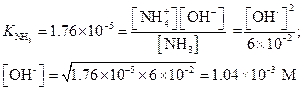
рOН = -lg(1.04×10-3) = 2.98; pH = 14 - pOH = 11.02.
Диссоциация слабых электролитов количественно характеризуется также степенью электролитической диссоциации (α). Степень диссоциации представляет собой отношение концентрации вещества, распавшегося на ионы, к общей его концентрации в растворе. Между константой диссоциации электролита КА и α существует следующая зависимость:
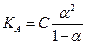 | (1.33) |
где С - молярная концентрация слабого~электролита. Если α мала (α < 5%), применимо приближенное уравнение 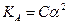 , откуда
, откуда
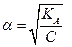 | (1.33) |
Пример 8. Вычислить степень диссоциации муравьиной кислоты в 1.5%-ном растворе.
Решение. Находим молярную концентрацию НСООН (М. м. = 46)
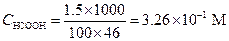
Формиат-ион и ион водорода образуются только в результате диссоциации муравьиной кислоты, следовательно, их концентрации равны
[H+] = [HCOО-] = х M,
[НСООН] = (3.26×10-1- х) М, отсюда
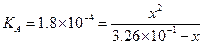
Если концентрация диссоциированной части мала по сравнению с общей концентрацией кислоты, то в знаменателе ею, как алгебраическим слагаемым, можно пренебречь. Тогда
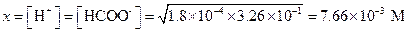
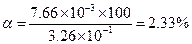
Пример 9. При какой концентрации бензойная кислота диссоциирована на 10%?
Решение. Если неизвестную общую концентрацию обозначить 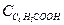 , то концентрация каждого из ионов будет равна
, то концентрация каждого из ионов будет равна
[Н+] = [С6Н5СОО-] = 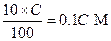 ,
,
а концентрация недиссоциированной части будет составлять
[С6Н5СООН] = С (1 - 1×10-1) = 9×10-1 С М,
отсюда
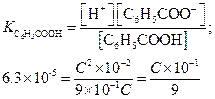
или
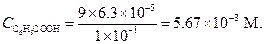
Пример 10. Уксусная кислота в 3%-ном растворе диссоциирована на 0.59 %. Вычислить приближенное значение константы диссоциации.
Решение. Находим молярную концентрацию СН3СООН (М. м. = 60.05).
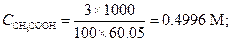
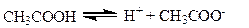 |
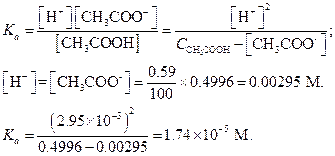
Пример 11. 0.5 М раствор гидразина имеет рН = 10.83. Вычислить константу диссоциации гидразина.
Решение.
рОН = 14-10.83 = 3.17; [ОН-] = 1×10-3.17 = 6.76×10-4 М,
 |
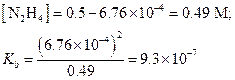
Многоосновные кислоты (H2SO4, H2SO3, H2CO3, Н2С2О4, Н3РО4 и др.) в водных растворах диссоциируют ступенчато
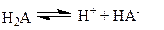 | (1.35) |
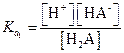 | (1.36) |
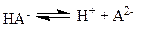 | (1.37) |
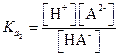 | (1.38) |
Константы диссоциации по первой ступени всегда больше, чем по второй ступени: 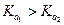 .Если
.Если 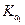 во много раз больше
во много раз больше 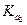 (
( 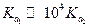 ) то концентрация ионов водорода определяется главным образом диссоциацией кислоты по первой ступени.
) то концентрация ионов водорода определяется главным образом диссоциацией кислоты по первой ступени.
Обозначим через х концентрацию диссоциированной части кислоты. Тогда, при начальной концентрации кислоты С равновесные концентрации будут равны
[Н2А] = С- х М;
[Н+] = х М;
[HA-] = х М.
Подставив эти значения в уравнение (1.36), получим:
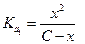 | (1.39) |
отсюда
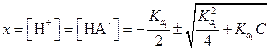 | (1.40) |
Если 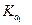 мала, то приближенно можно считать, что
мала, то приближенно можно считать, что
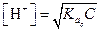 | (1.41) |
Поскольку [Н+]~[НА-], то из уравнения (1.38) находим
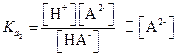 | (1.42) |
Пример 12. Вычислить концентрацию ионов водорода и анионов в 0.1 М растворе селенистой кислоты (К 1 =l.8×10-3, К 2 = 3.2×10-9).
Решение. Вычисляем концентрацию Н+и НSeО3- по уравнению (1 40)
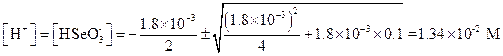
Концентрация SeO32- равна 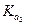 (3.2×10-9 M).
(3.2×10-9 M).
Особо следует рассмотреть равновесия в растворе серной кислоты. По первой ступени H2SO4 диссоциирует полностью. По второй ступени константа диссоциации равна 1.15×10-2.
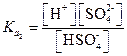 | (1.43) |
Пример 13. Найти концентрации H+, HSO4- и SO42- в 0.1 М растворе H2SO4.
Решение. Диссоциация H2SO4 может быть представлена следующими уравнениями:
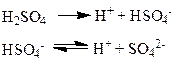 |
Обозначим концентрацию SO42- через х. Общая концентрация Н+ может быть выражена как сумма начальной концентрации H2SO4 (в соответствии с диссоциацией по первой ступени) и концентрации SO42-, образующихся по второй ступени
[Н+] = 0.1 + х
Очевидно, что концентрация HSO4- будет равна разности между начальной концентрацией H2SO4 и концентрацией SO42-
[HSO4-] = 0.l - х
Подставляя эти данные в уравнение (1.43), получим
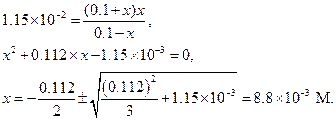
Следовательно,
[SO42-] = 8.8×10-3 M
[Н+] = 0.109 М,
[HSO4-] = 0.091 М.
 2015-05-13
2015-05-13 12221
12221
