При взаимодействии термодинамической системы с окружающей средой происходит обмен энергией. Способ передачи энергии, связанный с изменением внешних параметров, называют работой, а без изменения внешних параметров – теплотой.
Работа характеризует упорядоченную форму обмена энергией с окружающей средой, связанную с макроскопическими перемещениями в системе (сжатие, расширение, перемещение в поле сил тяжести и др.).
Работа изменения объема L, Дж, определяется как:
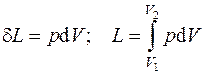 . (4.1)
. (4.1)
Работа, отнесенная к единице массы системы, называется удельной работой 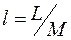 , Дж/кг. Для нее выражения (4.1) принимают вид:
, Дж/кг. Для нее выражения (4.1) принимают вид:
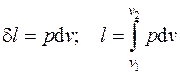 . (4.2)
. (4.2)
Работа является функцией процесса и графически изображается площадью под кривой процесса (1–2) в диаграмме p–v (рис. 4.1). Работа считается положительной, если она производится системой над внешними телами, и отрицательной, если она совершается над системой.
Теплота характеризует микроскопическую неупорядоченную форму обмена энергией, имеющую место при тепловом контакте тел с различной температурой, и самопроизвольно передается от более нагретого тела к менее нагретому на молекулярном уровне.
Количество теплоты Q, Дж, полученное или отданное системой, равно:
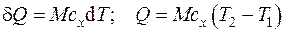 , (4.3)
, (4.3)
где 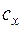 – теплоемкость вещества, определяемая по молекулярно-кинетической теории или как средняя теплоемкость в интервале температур
– теплоемкость вещества, определяемая по молекулярно-кинетической теории или как средняя теплоемкость в интервале температур 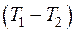 , индекс x – определяет характер процесса (
, индекс x – определяет характер процесса (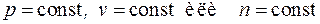 ) (см. разд. 3).
) (см. разд. 3).
Количество теплоты также можно найти, воспользовавшись вторым законом термодинамики (см. разд. 5):
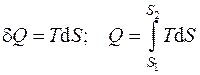 , (4.4)
, (4.4)
где S, Дж/К – энтропия системы.
Количество теплоты, отнесенное к единице массы системы, называется удельным количеством теплоты 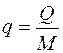 , Дж/кг и определяется как:
, Дж/кг и определяется как:
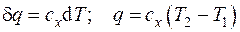 , (4.5)
, (4.5)
или
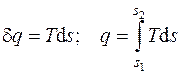 . (4.6)
. (4.6)
Графически теплота изображается площадью под кривой процесса (1–2) в диаграмме T–s (рис. 4.1). Теплота считается положительной, если она подводится к системе (энтропия в процессе подвода тепла увеличивается, 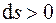 ), и отрицательной, если она отводится от системы (энтропия в процессе отвода тепла уменьшается,
), и отрицательной, если она отводится от системы (энтропия в процессе отвода тепла уменьшается, 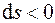 ).
).
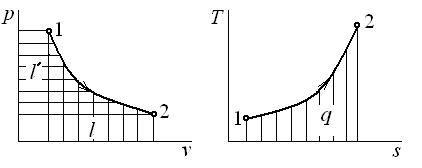
Рис. 4.1. Графическое изображение работы l,
полезной внешней работы l' и теплоты q
Первый закон термодинамики является законом сохранения и превращения энергии применительно к термодинамическим системам. В соответствии с ним теплота, подведенная к системе, идет на изменение ее внутренней энергии (см. разд. 3) и на совершение ею работы:
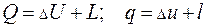 (4.7)
(4.7)
или в дифференциальной форме:
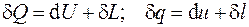 . (4.8)
. (4.8)
Первый закон термодинамики может быть записан также в терминах энтальпии (см. разд. 3):
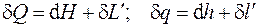 . (4.9)
. (4.9)
Здесь 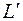 – полезная внешняя (располагаемая) работа, определяемая как
– полезная внешняя (располагаемая) работа, определяемая как
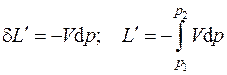 , (4.10)
, (4.10)
а 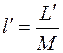 – удельная внешняя работа,
– удельная внешняя работа,
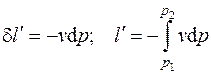 . (4.11)
. (4.11)
Графически полезная внешняя работа изображается площадью слева от кривой процесса в диаграмме p–v (рис. 4.1).
Задачи
4.1. Навстречу друг другу с одинаковой скоростью летят два одинаковых куска льда. При какой скорости они при неупругом ударе испарятся? Начальная температура кусков льда t 1= –30 оС. Теплоемкость льда с л = 2,1 кДж/(кг∙К), теплота плавления льда r пл = 333,7 кДж/кг, теплоемкость воды с в = 4,19 кДж/(кг∙К), теплота парообразования r = 2257 кДж/кг.
 2015-05-13
2015-05-13 5605
5605
