СРС№1
«Практическое применение электролиза»
Студента группы № 251 Снигерев М.С.
Преподаватель
Евсиков А.С.
Омск-2014
Электролиз – это совокупность процессов, протекающих в растворе или расплаве электролита, при пропускании через него электрического тока. Электролиз является одним из важнейших направлений в электрохимии.
Электрохимия принадлежит к числу тех немногих наук, дата рождения которых может быть установлена с высокой точностью. Это рубеж XVIII и XIX веков, когда благодаря знаменитым опытам итальянского физиолога Л. Гальвани и созданию итальянским физиком А. Вольта в 1799 г. "вольтова столба" - первого в истории человечества химического источника тока –были сформулированы проблемы, решение которых определило основные задачи электрохимии. "Без химии путь к познанию истинной природы электричества закрыт" - сказал М.В. Ломоносов. И, действительно, как бы следуя словам великого ученого, создавалась и развивается наука – электрохимия.
лектролиз, совокупность электрохимических окислительно-восстановительных процессов, происходящих при прохождении электрического тока через электролит с погруженными в него электродами. На катоде катионы восстанавливаются в ионы более низкой степени окисления или в атомы, напр.: Fe3+ + e  Fe2+, Сu2+ + 2е
Fe2+, Сu2+ + 2е  Сu (е - электрон). Нейтральные молекулы могут участвовать в превращениях на катоде непосредственно или реагировать с продуктами катодного процесса, которые рассматриваются в этом случае как промежуточные вещества электролиза На аноде происходит окисление ионов или молекул, поступающих из объема электролита или принадлежащих материалу анода; в последнем случае анод растворяется или окисляется (см. Анодное растворение). Напр.:
Сu (е - электрон). Нейтральные молекулы могут участвовать в превращениях на катоде непосредственно или реагировать с продуктами катодного процесса, которые рассматриваются в этом случае как промежуточные вещества электролиза На аноде происходит окисление ионов или молекул, поступающих из объема электролита или принадлежащих материалу анода; в последнем случае анод растворяется или окисляется (см. Анодное растворение). Напр.:
электролиз включает два процесса: миграцию реагирующих частиц под действием электрические поля к поверхности электрода и переход заряда с частицы на электрод или с электрода на частицу. Миграция ионов определяется их подвижностью и числами переноса (см. Электропроводность электролитов}. Процесс переноса нескольких электрических зарядов осуществляется, как правило, в виде последовательности одноэлектронных реакций, т. е. постадийно, с образованием промежуточных частиц (ионов или радикалов), которые иногда существуют некоторое время на электроде в адсорб
ированномсостоянии.
Скорости электродных реакций зависят от состава и концентрации электролита, материала электродов, электродного потенциала, температуры, гидродинамических условий (см. Электрохимическая кинетика). Мерой скорости служит плотность тока -количество переносимых электрических зарядов через единицу площади поверхности электрода в единицу времени. Кол-во образующихся при электролиз продуктов определяется Фарадея законами. Дня выделения 1 грамм-эквивалента вещества на электроде необходимо количество электричества, равное 26,8 А* ч. Если на каждом из электродов одновременно образуется несколько продуктов в результате ряда электрохимических реакций, доля тока (в %), идущая на образование продукта одной из реакций, наз. выходом данного продукта по току.
В электродном процессе участвуют вещества, требующие для переноса заряда наименьшего электрического потенциала; это м. б. не те в-ва, к-рые обусловливают перенос электричества в объеме р-ра. Напр., при электролиз водного р-раNaCl в миграции участвуют ионы Na+ и Сl+, однако на твердых катодах ионы Na+ не разряжаются, а протекает энергетически более выгодный процесс разряда протонированных молекул воды: Н3О+ + е --> 1/2H2 + Н2О.
Еще в начале позапрошлого столетия было установлено, что при прохождении электрического тока через водные растворы солей происходят химические превращения, приводящие к образованию новых веществ. В результате этого, в начале прошлого века возникло научное направление по изучению электрохимических процессов в растворах и расплавах веществ – электрохимия. К концу семидесятых годов оно разделилось на два самостоятельных раздела – ионику, изучающую явления электропроводности и движения заряженных частиц под воздействием электрического поля, и электродику, изучающую явления происходящие непосредственно на поверхности электродов, когда через границу электрод-раствор (расплав) протекает электрический ток. Химические превращения, происходящие при воздействии электрического тока на вещества, называются электролитическими.
Электролиз представляет собой довольно сложную совокупность процессов, к которым относятся: миграция ионов (положительных к катоду, отрицательных к аноду), диффузия ионов, разряжающихся на электродах, электрохимические реакции разряда ионов, вторичные химические реакции продуктов электролиза между собой, с веществом электролита и электрода.
Технический или прикладной электролиз характеризуется сложностью протекающих в промышленных условиях электролитических процессов, различными видами электролиза, их зависимостью от природы электролита, типа электролитической ванны, оптимизации самих электролизных процессов.
Электролитические процессы классифицируются следующим образом:
получение неорганических веществ (водорода, кислорода, хлора, щелочей и т.д.)
получение металлов(литий, натрий, калий, берилий, магний, цинк, алюминий, медь и т.д.)
очистка металлов(медь, серебро,…)
получение металлических сплавов
получение гальванических покрытий
обработка поверхностей металлов(азотирование,
борирование,электрополировка, очистка)
получение органических веществ
электродиализ и обессоливание воды
нанесение пленок при помощи электрофореза
Актуальность электролиза объясняется тем, что многие вещества получают именно этим способом. Например, такие металлы как никель, натрий, чистый водород и другие, получают только с помощью этого метода. Кроме того с его помощью электролиза относительно легко можно получить чистые металлы, массовая доля самого элемента в которых стремиться к ста процентам. В промышленности алюминий и медь в большинстве случаев получают именно электролизом. Преимущество этого способа в относительной дешевизне и простоте. Однако чтобы производство было наиболее выгодным: с наименьшими затратами электроэнергии и с наибольшим выходом продукции, необходимо учитывать различные факторы, влияющие на количество и качество продуктов электролиза (сила тока, плотность тока, температура электролита, материал электродов и др.).
На сегодняшний день большой популярностью пользуются различные предметы, покрытые драгоценными металлами. (позолоченные или посеребренные вещи).
К тому же металлические изделия покрывают слоем другого металла электролитическим способомс целью защитить его от коррозии.
Таким образом, исследование электрохимических процессов, определение факторов, влияющих на них, установление новых способов использования процессов электролиза в промышленных условиях сохранило свою актуальность и востребованность в наши дни.
Теоритеческое обоснование процессов электролиза.
Электролиз протекает только в тех средах, которые проводят электрический ток. Способностью проводить ток обладают также водные растворы оснований и солей. Безводные кислоты – очень плохие проводники, но водные растворы кислот хорошо проводят ток. Растворы кислот, оснований и солей в других жидкостях в большинстве случаев тока не проводят, но и осмотическое давление таких растворов оказывается нормальным, точно так же не проводят тока водные растворы сахара, спирта, глицерина и другие растворы с нормальным осмотическим давлением.
Различные отношения веществ к электрическому току можно иллюстрировать следующим опытом.
Соеденимпровода идущие от осветительной сети, с двумя угольными электродами. В один из проводов включим электрическую лампу, позволяющую грубо судить о наличии тока в цепи. Погрузим теперь свободные концы электродов в сухую поваренную соль или безводную серную кислоту. Лампа не загорается, т.к. эти вещества не проводят тока и цепь остается не замкнутой. То же самое происходит, если погрузить электроды в стакан с чистой дистиллированной водой. Но стоит только растворить в воде немного соли или прибавить к ней какой-нибудь кислоты или основания, как лампа тотчас же начинает ярко светиться. Свечение прекращается если опустить электроды в раствор сахара или глицерина и т.п.
Таким образом, среди растворов способностью проводить ток обладают преимущественно водные растворы кислот, оснований и солей. Сухие соли, безводные кислоты и основания (в твердом виде) тока не проводят; почти не проводит тока чистая вода, очевидно, что при растворении в воде кислоты основания или соли подвергаются каким-то глубоким изменениям, которые и обуславливают электропроводность получаемых растворов.
Электрический ток, проходя через растворы, вызывает в них, так же как и в расплавах, химические изменения, выражающиеся в том, что из растворов выделяются продукты разложения растворенного вещества или растворителя. Вещества, растворы которые проводят электрический ток, получили названия электролитов. Электролитами являются кислоты, основания и соли.
Химический процесс, происходящий при пропускании тока через раствор электролита, называется электролизом. Исследуя продукта, выделяющиеся у электрода, при электролизе кислот, оснований и солей, установили, что у катодов всегда выделяются металлы и водород, а у анода кислотные остатки или гидроксильные группы, которые затем подвергаются дальнейшим изменениям. Таким образом, первичными продуктами электролиза оказываются те же части кислот, оснований и солей, которые при реакциях обмена, не изменяются, переходят из одного вещества в другое.
Теперь, рассмотрим процесс электролиза подробнее.
Через проводники первого рода электричество переносится электронами, а через проводники второго рода—ионами. В тех местах электрической цепи, где проводник первого рода граничит с проводником второго рода, электроны вступают во взаимодействие с ионами—происходят электрохимические процессы. Если эти процессы протекают самопроизвольно, то система называется химическим источником энергии. Если же их протекание обусловлено подводом электрической энергии извне, то происходит электролиз.
Факторы от которых зависит электролиз
Эффективность электролиза оценивают рядом факторов, к которым
относятся: сила тока, напряжение, плотность тока, КПД источника тока, выход
по току, выход по веществу, коэффициент полезного действия электроэнергии
(выход по энергии), расход электроэнергии на единицу полученного продукта.
Сила тока или нагрузка на электролизёр характеризуют его
производительность. Чем выше сила тока, пропускаемого через электролизёр,
тем больше продукта можно получить при эксплуатации данного электролизёра.
Применение в промышленности
Электролиз широко применяется в различных отраслях промышленности. В химической промышленности электролизом получают такие важные продукты как хлор и щелочи, хлораты и перхлораты, надсерную кислоту и персульфаты, перманганат калия, органические соединения, химически чистые водород, кислород, фтор и ряд других ценных продуктов.
В цветной металлургии электролиз используется для рафинирования металлов, для извлечения металлов из руд. Металлы, которые не могут быть выделены из водных растворов вследствие высокого отрицательного потенциала. получают в цветной металлургии электролизом расплавленных сред, в качестве которых служат соли этих металлов, содержащие добавки различных соединений, вводимые с целью понижения температуры плавления расплава, повышения электропроводности и т.д. К числу металлов, получаемых электролизом расплавленных сред, относятся аллюминий, магний, цирконий, титан, уран, бериллий и ряд других металов.
Электролиз применяют во многих отрослях машиностроения, радиотехники, электронной, полиграфической промышленности для нанесения тонких покрытий металлов на поверхность изделий для защиты их от коррозии, придания декоративного вида, повышения износостойкости, жаростойкости, получения металических копий.
В основу классификации промышленных ванн могут быть положены различные признаки. Например, по типу полярности ванны могут быть монополярными, биполярными и комбинировнными.
В промышленных ваннах применяются различные типы катодов: неподвижные цельнометаллические, подвижные цельнометаллические(лента), неподвижные пористые неметаллические, насыпные металлические и т.д.
Аноды же могут быть расходуемые(вступающие в химическую реакцию), растворимые твердые, растворимые жидкие, нерастворимые твердые и пористые, нерастворимые.
Сочетание вышеперечисленных типов анодов и катодов с учетом целей электролиза приводит к следующим типам электролизеров: горизонтальные с жидким ртутным катодом, с вертикальными катодами и фильтруюшей диафрагмой, с горизонтальной диафрагмой, с проточным электролитом, с движущимися электродами, с насыпными электродами и т.д.
Для электролиза могут быть использованы следующие типы электролитов: водные растворы солей, кислот, оснований; неводные растворы в неорганических растворителях; неводные растворы в органических растворителях; расплавленные соли; твердые электролиты; газы.
К лучшим материалам для нерастворимых анодов относятся специальные сорта графита, двуокись свинца, магнетит, композиции на основе тантала и титана.
Несмотря на большое разнообразие электролитов, электродов, электролизеров, имеются общие проблемы технического электролиза. К ним следует отнести перенос зарядов, тепла, массы, распределение электрических полей. Для ускорения процесса переноса целесообразно увеличивать скорости всех потоков и применять принудительную конвекцию. Электродные процессы могут контролироваться путем измерения предельных токов.
При проектировании любого электрохимического производства необходимо выяснить все возможности оптимизации элетролизных процессов. Оптимизация условий электролиза имеет большое значение как при составлении энергетического баланса, так и при определении капиталовложений.
Оптимизации должны быть подвергнуты число ванн, способы очистки электролита, конструкции ванн, материалы электродов, типы электродов. Кроме того очень важно оценить оптимальные значения силы тока, сопротивления электролизной ячейки.
Практическое применение электролиза.
Электрохимические процессы широко применяются в различных областях современной техники, в аналитической химии, биохимии и т. д. В химической промышленности электролизом получают хлор и фтор, щелочи, хлораты и перхлораты, надсерную кислоту и персульфаты, химически чистые водород и кислород и т. д. При этом одни вещества получают путем восстановления на катоде (альдегиды, парааминофенол и др.), другие электроокислением на аноде (хлораты, перхлораты, перманганат калия и др.).
Получение целевых продуктов путем электролиза позволяет сравнительно просто (регулируя силу тока) управлять скоростью и направленностью процесса, благодаря чему можно осуществлять процессы как в самых "мягких", так и в предельно "жестких" условиях окисления или восстановления, получая сильнейшие окислители и восстановители. Путем электролиз производят Н2 и О2 из воды, С12 из водных р-ров NaCl, F2 из расплава KF в KH2F3.
Гидроэлектрометаллургия - важная отрасль металлургии цветных металлов (Сu, Bi, Sb, Sn, Pb, Ni, Co, Cd, Zn); она применяется также для получения благородных и рассеянных металлов, Мn, Сr. электролиз используют непосредственно для катодного выделения металла после того, как он переведен из руды в р-р, а р-р подвергнут очистке. Такой процесс наз. электроэкстракцией. электролиз применяют также для очистки металла - электролитич. рафинирования (электрорафинирование). Этот процесс состоит в анодном растворении загрязненного металла и в последующем его катодном осаждении. Рафинирование и электроэкстракцию проводят с жидкими электродами из ртути и амальгам (амальгамная металлургия) и с электродами из твердых металлов.
электролиз расплавов электролитов - важный способ произ-ва мн. металлов. Так, напр., алюминий-сырец получают электролиз криолит-глиноземного расплава (Na3AlF6 + A12O3), очистку сырца осуществляют электролитич. рафинированием. При этом анодом служит расплав А1, содержащий до 35% Сu (для утяжеления) и потому находящийся на дне ванны электролизера. Средний жидкий слой ванны содержит ВаС12, A1F3 и NaF, a верхний - расплавленный рафинир. А1 и служит катодом.
электролиз расплава хлорида магния или обезвоженного карналлита - наиб. распространенный способ получения Mg. В пром. масштабе электролиз расплавов используют для получения щелочных и щел.-зем. металлов, Be, Ti, W, Mo, Zr, U и др.
К электролитич. способам получения металлов относят также восстановление ионов металла другим, более электро-отрицат. металлом. Выделение металлов восстановлением их водородом также часто включает стадии электролиз - электрохим. ионизацию водорода и осаждение ионов металла за счет освобождающихся при этом электронов. Важную роль играют процессы совместного выделения или растворения неск. металлов, совместного выделения металлов и мол.водорода на катоде и адсорбции компонентов р-ра на электродах. электролиз используют для приготовления металлич. порошков с заданными св-вами.
Другие важнейшие применения электролиза - гальванотехника, электросинтез, электрохимическая обработка металлов, защита от коррозии (см. Электрохимическая защита).
Электролизеры. Конструкция промышленых аппаратов для проведения электролитических процессов определяется характером процесса. В гидрометаллургии и гальванотехнике используют преим. т. наз. ящичные электролизеры, представляющие собой открытую емкость с электролитом, в которой размещают чередующиеся катоды и аноды, соединенные соотв. с отрицательными и положительными полюсами источника постоянного тока. Для изготовления анодов применяют графит, углеграфитовые материалы, платину, оксиды железа, свинца, никеля, свинец и его сплавы; используют малоизнашивающиеся титановые аноды с активным покрытием из смеси оксидов рутения и титана (оксидные рутениево-титановые аноды, или ОРТА), а также из платины и ее сплавов. Для катодов в большинстве электролизеров применяют сталь, в т. ч. с различными защитными покрытиями с учетом агрессивности электролита и продуктов электролиз, температуры и др. условий процесса. Некоторые электролизеры работают в условиях высоких давлений, например, разложение воды ведется под давлением до 4 МПа; разрабатываются электролизеры и для более высоких давлений. В современных электролизерах широко применяют пластичные массы, стекло и стеклопластики, керамику.
Во мн. электрохимических производствах требуется разделение катодного и анодного пространств, которое осуществляют с помощью диафрагм, проницаемых для ионов, но затрудняющих мех.смешение и диффузию. При этом достигается разделение жидких и газообразных продуктов, образующихся на электродах или в объеме раствора, предотвращается участие исходных, промежуточных и конечных продуктов электролиз в реакциях на электроде противоположного знака и в при электродном пространстве. В пористых диафрагмах через микропоры переносятся как катионы, так и анионы в количествах, соответствующих числам переноса. В ионообменных диафрагмах (мембранах) происходит перенос либо только катионов, либо анионов, в зависимости от природы входящих в их состав ионогенных групп. При синтезе сильных окислителей используют обычно без-диафрагменные электролизеры, но в раствор электролита добавляют К2Сr2О7. В процессе электролиз на катоде образуется пористая хромит-хроматная пленка, выполняющая функции диафрагмы. При получении хлора используют катод в виде стальной сетки, на которую наносят слой асбеста, играющий роль диафрагмы. В процессе электролиз рассол подают в анодную камеру, а из анодной камеры выводят раствор NaOH.
Электролизер, применяемый для получения магния, алюминия, щелочных и щелочно - земельных металлов, представляет собой футерованную огнеупорным материалом ванну, на дне которой находится расплавленный металл, служащий катодом, аноды же в виде блоков располагают над слоем жидкого металла. В процессах мембранного получения хлора, в электросинтезе используют электролизеры фильтр-прессного типа, собранные из отд. рам, между которыми помещены ионообменные мембраны.
По характеру подключения к источнику питания различают монополярные и биполярные электролизеры (рис.). Монополярный электролизер состоит из одной электролитической ячейки с электродами одной полярности, каждый из которых может состоять из нескольких элементов, включенных параллельно в цепь тока. Биполярный электролизер имеет большое число ячеек (до 100-160), включенных последовательно в цепь тока, причем каждый электрод, за исключением двух крайних, работает одной стороной как катод, а другой как анод. Монополярные электролизеры обычно рассчитаны на большой ток и малые напряжения, биполярные - на сравнительно небольшой ток и высокие напряжения. Современные электролизеры допускают высокую токовую нагрузку: монополярные до 400-500 кА, биполярные эквивалентную 1600 кА.
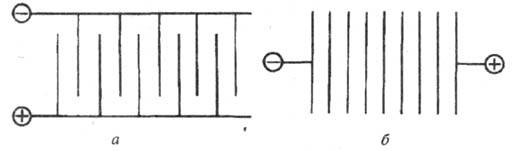
Схема подключения к источнику внеш. тока монополярного (а)и биполярного (б)электролизеров.
Электролиз в гидрометаллургии является одной из стадий переработки металлсодержащего сырья, обеспечивающей получение товарных металлов. Электролиз может осуществляться с растворимыми анодами - процесс электрорафинирования или с нерастворимыми - процесс электроэкстракции. Главной задачей при электрорафинировании металлов является обеспечения необходимой чистоты катодного металла при приемлемых энергетических расходах.
В цветной металлургии электролиз используется для извлечения металлов из руд и их очистки. Электролизом расплавленных сред получают алюминий, магний, титан, цирконий, уран, бериллий и др.
Для рафинирования (очистки) металла электролизом из него отливают пластины и помещают их в качестве анодов в электролизер. При пропускании тока металл, подлежащий очистке, подвергается анодному растворению, т. е. переходит в раствор в виде катионов. Затем эти катионы металла разряжаются на катоде, благодаря чему образуется компактный осадок уже чистого металла. Примеси, находящиеся в аноде, либо остаются нерастворимыми, либо переходят в электролит и удаляются.
Гальванотехника – область прикладной электрохимии, занимающаяся процессами нанесения металлических покрытий на поверхность как металлических, так и неметаллических изделий при прохождении постоянного электрического тока через растворы их солей. Гальванотехника пожразделяется на гальваностегию и гальванопластику.
Гальваностегия (от греч.покрывать) – это электроосаждение на поверхность металла другого металла, который прочно связывается (сцепляется) с покрываемым металлом (предметом), служащим катодом электролизера.
Перед покрытием изделия необходимо его поверхность тщательно очистить (обезжирить и протравить), в противном случае металл будет осаждаться неравномерно, а кроме того, сцепление (связь) металла покрытия с поверхностью изделия будет непрочной. Способом гальваностегии можно покрыть деталь тонким слоем золота или серебра, хрома или никеля. С помощью электролиза можно наносить тончайшие металлические покрытия на различных металлических поверхностях.При таком способе нанесения покрытий, деталь используют в качестве катода, помещенного в раствор соли того металла, покрытие из которого необходимо получить. В качестве анода используется пластинка из того же металла.
Гальванопластика – получение путем электролиза точных, легко отделяемых металлических копий относительно значительной толщины с различных как неметаллических, так и металлических предметов, называемых матрицами.
С помощью гальванопластики изготовляют бюсты, статуи и т. д.
Гальванопластика используется для нанесения сравнительно толстых металлических покрытий на другие металлы (например, образование "накладного" слоя никеля, серебра, золота и т. д.).
Заключение
Анализ научной и научно-популярной литературы свидетельствует о том, что процессы электролиза растворов и расплавов интересуют ученых и технологов в настоящее время, то есть данная тема не потеряла своей актуальности и практической значимости.
Электролиз широко используют в промышленности для выделения и очистки металлов, получения щелочей, хлора, водорода.
Аллюминий, магний, натрий, кадмий, кальций, берилий, титан получают только электролизом расплавов, т.к. потенциалы их выделения из водных ратворов более отрицательны, чем потенциал выделения водорода.
Очистку меди, никеля, свинца проводят целиком электрохимическим методом. Производство фтора основано на электролизе расплавленной смеси фторида калия и фтороводородной кислоты, хлора – при электролизе водных ратворов или расплавов хлоридов. Водород и кислород высокой степени чистоты получают электролизом водных растворов щелочей. Таким образом, с помощью электролиза удается осуществлять реакции окисления и восстановления с большим выходом и высокой селективностью, которые в обычных химических процессах трудно достижимы.
Важной отраслью применения электролиза является защита металлов от коррозии: при этом электрохимическим методом на поверхность металлических изделий наносится тонкий слой другого металла (хрома, серебра, меди, никеля, золота) устойчивого к корозии.
Отличительной особенностью электролиза растворов или расплавов
электролитов является возможность протекания на электродах совокупности
конкурирующих химических реакций окисления и восстановления. Оказывает
влияние на продукты электролиза и материал электродов.
При электролизе водных растворов электролитов окислительно-восстановительные процессы на катоде и аноде зависят от окислительной способности катионов и характера аниона электролита.
Процессы востановления и окисления на катоде и аноде определяются значениями электродных потенциалов частиц, принимающих участие в электролитических процессах. На катоде в первую очередь разряжаются те частицы, потенциал которых наиболее положителен, тогда как на аноде – частицы – потенциал котрых наиболее электроотрицателен. Кроме того, при протекании электролиза необходимо учитывать фактор электродного перенапряжения – поляризацию электрода, определяемую замедленным протеканием определенной стадии суммарного электродного процесса. В зависимости от природы замедленной стадии можно говорить о различных видах перенапряжения (концентрационное, реакционное, диффцзное).
В экспериментальной части своей работы нами были проведены процессы электролиза растворов ряда солей. Полученные продукты подтверждают основные теоретические положения процессов электролиза водных растворов электролитов и доказан факт влияния электродных потенциалов частиц, принимающих в нем участие, на состав конечных продуктов.
На основании проделанной работы можно сделать следующие выводы:
Исследование процессов электролиза растворов и расплавовэлектролитов не потеряло своей актуальности и в настоящее время, т.к. не только обогащает теоретические положения об этом достаточно сложно физико-химическом явлении, но и позволяет определить перспективные направления практического использования этого процесса с целью получения целевых продуктов с заданными свойствами и качествами.
Качественный состав конечных продуктов электролитических процессов определяется не только величиной электродного потенциала ионов, но и видом перенапряжения, возникающего при этом.
Литература:
1. Н.Л. Глинка/ Общая химия.г. Москва, 1985г. 250-253; 257-261с.
2. Н.В.Коровина. / Курс общей химии. Высш. шк., 1991. 378-380 с.
3. Фиошин М.Я., Павлов В. Н., Электролиз в неорганической химии, М., 1976
4. Зимин В. М., Камарьян Г. М., Мазанко А.Ф., Хлорные электролизеры, М., 1984
5. Фиошин М.Я., Смирнова М. Г., Электрохимические системы в синтезе химических продуктов, М., 1985
6. Мазанко А.Ф., Камарьян Г.М., Помашин О.П., Промышленный мембранный электролиз, М., 1989
 2015-08-13
2015-08-13 463
463






