Лекция 6. Классификация химических реакций и химико-технологических процессов
1. Классификация реакций, лежащих в основе ХТП
2. Классификация ХТП
Классификация реакций, лежащих в основе ХТП
В химической технологии используются следующие классификации химических реакций:
1. Для выбора конструкции реактора и способов управления проведением процесса существенное значение имеет фазовое состояние реакционной системы.
В зависимости от того, одну или несколько фаз образуют реагенты и продукты реакции химические реакции делят на гомофазные или гетерофазные. Гомофазными называют реакции, в которых исходные реагенты, стабильные промежуточные продукты и продукты реакции находятся в пределах одной фазы. Гетерофазными называют реакции, в которых исходные реагенты, стабильные промежуточные продукты и продукты реакции образуют более чем одну фазу. Различают двухфазные системы «газ – жидкость», «газ – твердое вещество», «жидкость – твердое вещество», «жидкость – жидкость» (две несмешивающиеся жидкости), «твердое – твердое» и различные варианты трехфазных систем.
2. В зависимости от зоны протекания реакции классифицируют на гетерогенные (протекают на поверхности раздела фаз)и гомогенные (протекают в объеме одной фазы).
Понятия «гомогенная» и «гетерогенная» реакции не совпадают с понятиями «гомофазный» и «гетерофазный» процессы. Гомогенность и гетерогенность реакции отражает в определенной степени ее механизм: протекает ли реакция в объеме какой-то одной фазы или на поверхности раздела фаз. Гомофазность и гетерофазность процесса позволяют лишь судить о фазовом составе участников реакции. Например, протекающий в растворе процесс нейтрализации кислоты щелочью – это гомофазный гомогенный процесс. Каталитический синтез аммиака – это гомофазный гетерогенный процесс. Окисление углеводородов в жидкой фазе газообразным кислородом – это гетерофазный процесс, но протекающая химическая реакция является гомогенной. Наконец, реакция получения гашеной извести
СаО + Н2О = Са(ОН)2,
при которой все три участника процесса находятся в разных фазах, а реакция идет на границе раздела воды и оксида кальция, является гетерофазной гетерогенной реакцией.
3. По механизму осуществления различают простые (одностадийные) и сложные (многостадийные), в т.ч. параллельные, последовательные, параллельно-последовательные, обратимые, цепные, сопряженныереакции.
Простыми называют реакции, осуществление которых связано с преодолением только одного энергетического барьера (одна стадия).
Сложные реакции включают в себя ряд параллельных и/или последовательных стадий (простых реакций).
В реальных условиях одностадийные реакции встречаются очень редко. Однако некоторые сложные реакции, проходящие через ряд промежуточных стадий, удобно считать формально простыми. Это возможно тогда, когда промежуточные продукты реакции в условиях рассматриваемой задачи не обнаруживаются.
4. По обратимости реакции подразделяют на обратимые и необратимые.
5. По знаку теплового эффекта реакции делят на экзотермические, сопровождающиеся выделением теплоты (Q > 0) и уменьшением энтальпии реакционной системы(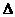 Н < 0) и эндотермические, протекающие с поглощением теплоты (Q < 0) и увеличением энтальпии реакционной системы(
Н < 0) и эндотермические, протекающие с поглощением теплоты (Q < 0) и увеличением энтальпии реакционной системы(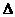 Н > 0).
Н > 0).
6. По наличию катализатора различают каталитические и некаталитические реакции.
7. По температуре проведения реакции классифицируют на низкотемпературные (менее 160оС, например, алкилирование изобутана олефинами), среднетемпературные (160-500оС, например, окисление парафинов) и высокотемпературные (более 500оС, например, пиролиз углеводородного сырья).
8. Классифицируя реакции по молекулярности, учитывают количество молекул, участвующих в элементарном акте реакции. Различают моно-, би- и тримолекулярные реакции.
9. По порядку реакцииклассифицируют по виду кинетического уравнения. Порядком реакции называют сумму показателей степени у концентраций регентов в кинетическом уравнении. Существуют реакции первого, второго, третьего и дробного порядков.
Классификация ХТП
Классификация химико-технологических процессов необходима для системного описания существующих процессов химической технологии, выработки единых подходов к управлению процессами. Чем полнее можно учесть свойства физико-химической системы, положенной в основу ХТП, тем точнее будет система классификации, ее способность к прогнозированию будет более высокой. Таким образом, цель классификации – выделить такие характеристики процесса, комбинация которых определяет те или иные свойства процесса в целом, его закономерности и особенности. Поскольку химико-технологический процесс – это система взаимосвязанных явлений, то классификацию проводят по разным признакам (уровням), и она имеет разветвленную структуру.
1-ый уровень. Маршрут физико-химического превращения, положенного в основу ХТП – простой или сложный процесс. Под простым понимают такой, в результате которого независимо от числа стадий получают только целевой продукт или целевой продукт и ему сопутствующий, если по реакции образуются два вещества. Под сложным ХТП понимают такой, в результате которого получаются не только целевой и сопутствующий, но и побочные продукты, на которые затрачивается часть сырья. Процессы, по которым получаются побочные продукты, могут развиваться как последовательно, так и параллельно целевому.
2-ой уровень. Термодинамическая характеристика физико-химической системы с учетом возможного изменения параметров режима – односторонний или двусторонний процесс. Для уточнения здесь вводят два подуровня:
подуровень 2.1. Определение возможности влияния на полноту смещения химического превращения в сторону целевого продукта – двусторонний смещаемый или двусторонний несмещаемый процесс.
подуровень 2.2. Определение разности энтальпий системы до и после химического превращения – экзотермический или эндотермический процесс. В технологических разработках изменение энтальпии реакционной системы имеет большое значение, поскольку приемы для осуществления экзотермических и эндотермических ХТП существенно отличаются.
3-ий уровен ь. Определение фаз в физико-химической системе с учетом применения катализатора – гомогенный или гетерогенный процесс.
4-ый уровень. Кинетическая характеристика системы, нахождение лимитирующей стадии ХТП – процесс с химическим или диффузионным торможением. Здесь также для уточнения вводят два подуровня:
подуровень 4.1. Определение необходимости применения катализатора в случае химического торможения – каталитический или некаталитический процесс.
подуровень 4.2. Определение дислокации диффузионного торможения – процесс с внешнедиффузионным или внутридиффузионным торможением.
Применение такой системы классификации оказывает существенную помощь в поиске оптимального варианта технологического режима и оптимизации технологической схемы.
 2018-01-08
2018-01-08 2767
2767