В) сирек металдар
Акцептор бола алады:********* A) Темір B) Кремний C) Сутегі
Алмазбен графитте көміртегі атомының гибридтелу типі:********* А) sp3 В) sp2
Алмасу механизм бойынша түзіледі:********* A)  B)
B)  C)
C) 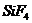
Алмасу реакциясы:********* A) AgNO3 + NaCl = AgCl ↓+ NaNO3 B) Na2SO4 + BaCl2= BaSO4↓ + 2NaCl C) (NH4)2S + ZnCl2 = ZnS↓ + NH4Cl
Алмасу реакциясы тән комплексті иондар:********* [Ag(CN)2]2-; KT =1.0*10-23********* [Fe(CN)6] 4-; KT =1.0*10-24
Алюминий гидроксокомплексін алуға болатын реакция :*********AlCl3+6KOH→****Al(OH)3+3KOH→
Алюминий сілтімен әрекеттескен кезде ****** А) сілті оксид жабынын ерітеді В) Сутегін бөледі
Алюминотермия үрдісі:********* А) Металдың алюминиймен тотықсыздануы: В) Аl + CuO®
Аминокомплекстер:********* [Zn (NH3)4]SO4 ********* [Cu(NH3)4]SO4
Аминокомплексті алуғаболатын реакция:*********
CuSO4 + NH4ОН→*********CdSO42+ NH4ОН→
Аммиак молекуласындағы тотығу дәрежесі немесе валенттілігі немесе байланыс түрі:********* үш байланыс*********В=3
Аммиак молекуласының орталық атомының гибридтелу түрі немесе геометриялық формасы немесе валенттік бұрышы :*********Sp3*********107030
Аммиак:********* A) әлсіз негіз B) сулы ерітіндісі мүсәтір спирті деп аталады
Аммоний дихроматының термиялық ыдырауында түзіледі:*********A) N2 B) Cr2O3 C) H2O
Амфотерлі оксидтер:********* A) Cr2O3 B) MnO2 C) ZnO
Амфотерлі гидроксидтер әрекеттеседі:********* Күкірт қышқылымен
Амфотерлі гидроксидтер:********* A) Al(OH)3 B) Cr(OH)3 C) Zn(OH)2
Амфотерлі гидроксидтер:********* A) Sn(OH)2 B) Zn(OH)2 C) Sb(OH)3
Амфотерлі гидроксидтер:********* A) Be(OH)2 B) Al(OH)3 C) Fe(OH)3
Амфотерлі элементтер:********* A) Al B) Zn C) Be
Анионды комплекс********* Na2[Pb(OH)4] *********K3[AlF6]
Анионды типтегі кешенді қосылыс ********* А) К4[ Fe(CN)6] B) К4[ Co(NO2)4]
Анод – электродында жүретін процесс:********* A) электролит анионының тотығуы;
АО- sp, sp2, sp3 – гибридтенуі бар молекулалар:********* A) C2H2 B) C2H4 C) CH4
АО- дың sp2-гибридтенуі молекулаларда:********* A) C2H4 B) COCl2 C) H2CO3
АО- дың sp2-гибридтенуі молекулаларда:********* A) C6H6 B) BF3 C) H2SiO3
АО- дың sp3-гибридтенуі молекулаларда:********* A) C2H6 B) NH3 C) CCl4
АО- дың sp3-гибридтенуі молекулаларда:********* A) SiF4
B) CH4 C) NH3
АО- дың sp-гибридтенуі молекулаларда:********* A) BeF2 B) HgCl2 C) CO2
АО- дың sp-гибридтенуі молекулаларда:********* A) СО2 B) HCN C) C2H2
Аралас комплекстер:********* [Cr(H2O)5Cl]Cl2********* [Cr(NH3)5Cl]SO4
Аргонды пісірілген ампула-бұл термодинамикалық жүйе:********* A) оқшауланған
Аррениус анықтамасының шектеулігінің мәні неде:********* А) бір ғана еріткішпен-сумен байланысты
Аррениус бойынша:********* Қышқыл-бұл сутегі ионын беретін қосылыс
Аррениус ұстанымына сәйкес қышқыл дегеніміз:********* А) сулы ерітінділерінде Н+ протонын босататын
Аррениус ұстанымына сәйкес негіз дегеніміз:********* А) сулы ерітінділерінде ОН- иондарын босататын
Ассоциаттарды түзуге қабілетті молекулалар:********* A) Суда B) Аммиак C) Гидразин
Атомдағы электронның күйін сипаттайды:********* А)
4 квант сандар жиынтығымен;
Атомдық орбитальдардың әртүрлі деңгейшелерде электрондармен толтыру ретін анықтайтын ереже:********* A) Клечковского
Атомдық орбитальдардың қаптасуынан түзілетін сигма байланыс :*********s – s*********p(x) - p(x)
Атомның иондану энергиясына қатысты:********* Атомның ядро мен едәуір әлсіз байланысқан электронды тартып алуға қажетті минималды энергия
Атомның негізгі күйінде электрондарының энергетикалық деңгейлерде, деңгейшелерде және орбиталдарда орналасуы анықталады:********* A) Паули принципімен B) Хунд ережесімен C) Клечковский ережесімен
Атомның салмақтық бірлігі:********* А) 12С изотопы массасының 1/12 бөлігі
Ауа сутегінен неше есе ауыр:********* А)14,5
Ауыр металдар:********* A) Хром B) Марганец C) Темір
Ауыспалы металдардың атомдардың электрондық құрылысының ерекшеліктері:********* Электртерістігі екіден аз
Ауыспалы элементтер:********* A) Sc B) Ti C) V
Ауыспалы элементтерге сәйкес келеді:********* A) d – элементтер B) ІВ тобы C) ІІІВ тобы
Ацидокомплекс:********* K2[Co(SO3)2] *********Na[Fe(SCN)4 ]
Ашық жүйенің ерекшелігі:********* A) қоршвғвн ортамен масса және энергия алмасуы мүмкін
Ә
Әдетте гетерогенді катализ фазалардың беттік шекарасында жүреді:********* А) қатты- сұйық немесе қатты- газ
Әлсіз электролиттер:********* A) H2S B) H2SO3 C) H2CO3
Әлсіз электролиттер:********* A) HCOOH B) H2SiO3 C) H2S
Әлсіз электролиттер:********* A) HNO2 B) H3BO3 C) H3PO3
Әлсіз қышқыл тұздары:********* A) Na2B4O7
B) CH3COONa C) K2S
Әлсіз қышқыл тұздары:****** A) KCN B) Na2C2O4 C) K2SO3
Әлсіз қышқылдар:********* A) HNO2 B) H3PO4 C) H2CO3
Әлсіз электролиттің диссрциациялану дәрежесі мен диссоциациялану тұрақтысы арасындағы тәуелділік:********* A) a= 
Б
Байланыстары S- және p-электрон бұлттарының бүркесуі арқылы түзілген молекула :*********NH3*********PH3
Байланыстың полярлану дәрежесі мына қатарда артады:********* A) СH4- NH3- H2O - HF
Бас және орбиталь квант сандарының қосындысы бірдей шама болатын:********* 5s
Бас квант саны 6-ға тең электрон қабатындағы электрондардың максималь санын анықтаңдар:****** A) 72
Бас квант саны анықтайды:********* A) Электрондық қабатта электрондардың максимал санын
B) Электрондық орбиталдің мөлшерін C) Атомдағы электронның энергиясын
Бас квант саны мына мәндерді қабылдайды:********* A) 1,2. … ¥
Бас квант саны сипаттайды:********* A) деңгейдегі электрон санын;
Байланыстары S- және p-электрон бұлттарының бүркесуі арқылы түзілген молекула: NH3\\\\\PH3\\\\\AsH3
Бас және орбиталь квант сандарының қосындысы бірдей шама болатын: 5s\\\\\4p\\\\\3d
Бейметалдық қасиеті анық білінетін элемент атомының валентті электрондарының электрондық конфигурациясы: 4s2 р5\2s2 р5\3s2 р4
Бейтараптану реакциясының нәтижесінде алуға болатын тұздар: Қышқыл\\\\\Орта\\\\Негіздік
Бейметалдық қасиеті анық білінетін элемент атомының валентті электрондарының электрондық конфигурациясы:********* 4s2 р5
Бейтараптану реакциясы:********* A) HCl + NaOH = NaCl + H2O B) 2HCl + Ca(OH)2 = CaCl2 + 2H2O C) HNO3 + KOH = KNO3 + H2O
Бейтараптану реакциясының нәтижесінде алуға болатын тұздар:********* Қышқыл
Бериллий топшасы элементтерінде жоғарыдан төмен қарай, берилийден барийге қарай;******* A) атомдардың иондану потенциалы кемиді B) электрон қосылғышығы төмендейді C) атомдар радиустары артады
Берілген бас квант санды электрондардың максималь саны мен деңгейдегі орбитальдар саны мына формулаға сәйкес анықталады:********* A) 2n2 және n-1
Берілген реакцияның белсендіру энергиясы-бұл:********* A) молекуланы белсендіруге қажетті энергия;
Бор галогенидтері:********* A) жазық үшбұрыш пішіні бар B) Донорлы-акцепторлық әрекеттесуге қабілетті
Бөлшек радиусы артады:********* Cl+5→ Cl-1
Бренстед-Лаури теориясы бойынша HCl қатысында су:********* А) су-протондардың акцепторы,яғни-негіз болып табылады
Бренстед-Лаури теориясы бойынша аммиактың қатысында басталды:********* А) су-протондар доноры яғни қышқыл болып табылады
Бренстед-Лаури теориясында негіз ретінде алынған үрдіс:********* А) бір заттан протонның басқаға ауысуы
Бренстед-Лаури ұстанымы бойынша қышқыл дегеніміз********* А) протондардың донор босатуға қабілеттілігі
Бренстед-Лаури ұстанымы бойынша тұз дегеніміз:********* А) кейбір бейтараптану реакцияларында иондар агрегатын түзуші
Бөлшек радиусы артады: Cl+5→ Cl-1\Na+ →Cs+\F-1→I-
Бір мезгілде қысымды 4 есе кеміткенде, CO+Cl2↔ COCl2 температураны 600 (γ=2) арттырғанда реакция жылдамдығы артады: 0,4*10есе\\\\\40*10-1 есе\\\\\0,04*102 есе
Бір сатыда диссоциацияланатын тұздар: NaCІ, K3PO4, КАІ(SO4)2\\\\\\\K2CO3, CaCl2, CH3COONa\\\\\\\\\K2CO3, CaCl2, (NH4)Fe(SO4)2
Бір сатыда диссоциацияланатын электролиттер: CaCl2\\\\\(NH4)Fe(SO4)2\\\\\\K2CO3
Бір топтағы элементтерде периодты түрде қайталанады: Сыртқы энергетикалық деңгейдегі электрондар саны\\\\\Валентті электрондар саны\\\\\\Сыртқы энергетикалық ддеңгейдегі электрондар конфигурациясы
Бірдей жағдайда ɑ˂30% болғанда, электролит: H2SO3\\\\\HCN\\\\\\H2CO3
Бірдей жағдайда ɑ˃30% болғанда, электролит: H2SO4\\\\\\\HNO3\\\\\\HCl
Бірінші негізгі топтың элементтері үшін жоғарыдан төмен: Электртерістігі төмендейді\Иондану энегриясы төмендейді\Электр тартқыштығы төмендейді
Бір деңгейше шегінде атомдық орбитальдар электрондардың орналасуын анықайтын ереже:********* A) Гунд
Бір кванттық ұяшықтағы электрондар санын анықтайтын принцип:********* A) Паули
Бір лиганд алатын координациялық орын саны былай аталады:********* A)дентанттылық
Бір мезгілде қысымды 4 есе кеміткенде, CO+Cl2↔ COCl2 температураны 600 (γ=2) арттырғанда реакция жылдамдығы артады :*********0,4*10есе*********40*10-1 есе
Бір негізді қышқылдар:********* A) HCl B) HI C) HBr
Бір топтағы элементтерде периодты түрде қайталанады:********* Сыртқы энергетикалық деңгейдегі электрондар саны
Бірдей сыртқы жағдайларда максимальды энтропияға ие:********* A) H2O(г.)
Бірінші негізгі топтың элементтері үшін жоғарыдан төмен:********* Электртерістігі төмендейді
В
BaSO4 ерігіштік көбейтіндісі (ЕК)1,1*10-10тең. BaSO4(г/л) ерігіштігін есептеу:********* А) 2,45*10-3г/л В)24,5*10-4г/л С) 0,245*10-2г/л
Be(OH)2 әрекеттесуі мүмкін:********* Күшті қышқылмен
Be(OH)2→Mg(OH)2→Ca(OH)2→Sr(OH)2→Ba(OH)2:********* Негіздердің күші артады
BeCl2 BF3 және SF6 молекулаларында бериллий, бор және күкірттің гибридтену түрі:********* A) sp B) sp2 C) sp3d2
BеCl2 молекуласының геометриялықформасы немесе валенттік бұрышы немесе гибридтену типі :*********Sp*********1800
В.Гейзенбергтің анықталмағыштық принципі:********* A) бір уақытта микробөлшектің орны мен оның қозғалу санын дәл анықтау мүмкін емес
ВF3 молекуласында бордың валеттік бұрышы және гибридтелу типі********* А) 1200 B) sp2
Ванадий оксидтеріндегі ванадийдің тотығу дәрежесі төмендеу ретімен орналастыр:********* A) V2O5, VO2, V2O3, VO
Вант-Гоффтың заңына сәйкес:********* A) pосм. = C(x)RT
ВБ әдісін және кристалдық өріс теориясын қолданып, [AuCl4]- кешенді ионның орталық атом зарядын және гибридтену типін анықтаңдар:********* A) +3 B) sp3
ВБ әдісін және кристалдық өріс теориясын қолданып, [Fе(СN)6]-4 кешенді ионның орталық атом зарядын және гибридтену типін анықтаңдар:********* А) d2sp3 В) октаэдр
ВБ әдісін және кристалдық өріс теориясын қолданып, [Мn(CN)6]4- кешенді ионның орталық атом зарядын және гибридтену типін анықтаңдар:********* А) d2sp3 B) +2
ВБ теориясы бойынша көміртегі (II) оксиді молекуласында:********* A) С және О атомдарының қос байланысы 2р- электрондардың жұптасуы есебінен түзіледі B) біреуі - донорлы-акцепторлы механизм бойынша С бос 2р-орбиталі есебінен, О электрондық жұбынан C) үштік байланыс
Г
Газдың сутегі бойынша тығыздығы 16-ға тең болса, ол газдың молекулалық массасы қанша:********* А)32
Галогендер:********* A) FB) Cl C) Br
Гальваникалық элементтегі:********* A) ТТР энергия электр энергиясына айналады
Гальваникалық элементтің ЭҚК неге тең:********* A) ЭДС = jкатод - jанод
Гей-Люссак пен Бойль-Мариоттың біріккен заңдары:********* А) 
Гелий бойынша тығыздығы 10,5 және құрамы (массалық бөлігіне байланысты): С -85,71%, Н-14,29% бар заттың:
Гельмгольц энергиясы мынаған тең:********* A) U – TS
Гесс заңы есептеуге мүмкіндік береді:********* Изобаралық процестердің жылу эффектісі*********Изохоралық процестің жылу эффектісі
Гесс заңынан шығатын дұрыс емес формуланы көрсет:********* A) 
Гесс заңынан шығатын дұрыс емес формуланы көрсет:********* A)  B)
B)
Гетерогенді реакция:********* FeО+С→Fe+СО
Гиббс энргиясы мынаның критериі болып табылады:********* A) үрдістің өздігінен жүру мүмкіндігіне;
Гидроксидтердің қышқылдық-негіздік сипаттамасын ескере отырып, мүмкін болатын реакция:********* Zn(OH)2+HCl→
Гидроксокомплекс: *********Na2[Pb(OH)4]*****K[Al(OH)4]
Гомогенді реакция:********* HNO3+KOH→KNO3+H2O
Д
Дипольді моменті нөлге тең молекулалар :*********CO2*********CH4
Диспропорциялану реакциясы:********* A) 3CrO2 → Cr2O3 + CrO3 B) 4KClO3 → KCl + 3KClO4 C) NH4NO2 → N2 + 2H2O
Диспропорциялану реакциясы:********* A) 3S + 6NaOH = 2Na2S + Na2SO3 + 3H2O B) 2NO2 + H2O = HNO3 + HNO2 C) 3H2MnO4 = MnO2 + 2HMnO4 + 2H2O
Диссоциациялану дәрежесі-бұл:********* A) иондарға ыдыраған молекула санының еріген молекулалардың жалпы санына қатынасы
Донор бола алады:********* A) Азот B) Хлорид-анион C) Оттегі
Донорлы-акцепторлы механизм бойынша түзіледі:********* A) 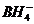 B)
B)  C)
C) 
Дұрыс тұжырымды көрсетіңіз (КК-аз еритін қосылыс иондарының тепе-теңдіксіз концентрацияларының көбейтіндісі, ал ЕК-тепе-теңдікті концентрацияларының көбейтіндісі):********* КК<ЕК кезінде тұнба ериді****КК>ЕК кезінде тұнба түседі****КК=ЕК кезінде тұнба ерітіндімен тепе-теңдікте болады
Е
«Ерігіштік көбейтіндісі» түсігінін қолданады:********* А)Кальций карбонаты В)Күміс хлориді С) Барий сульфаты
Егер 500 мл натрий гидроксиді ерітіндісінде 3,4 гидроксид ион болса, еріген заттың молярлық концентрациясы(моль/л)****** А)0,04*10 В)4*10-3 С)40*10-2
Егер 2SO2 + O2 = 2SO3, [SO2]=0.04, [SO3]=0.02, [O2]=0.06 тепе-теңдік концентрациясы тең болса,жүйедегі тепе-теңдік константасын көрсет:********* A) 4,17
ЕК(PbСІ2)=1,7*10-5 кезіндегі PbСІ2-нің тұнбаға түсу жағдайы**** [Pb2+]*[СІ-]2 =2,2*10-2****[Pb2+]*[СІ-]2 =3,4*10-4**** [Pb2+]*[СІ-]2 =5,6*10-3
ЕК(Ba3(PO4)2=6*10-39 кезіндегі тұнбаға түсу жағдайына барий фосфаты иондары концентрациясы көбейтіндісінің мәні :*********1,5*10-24****15*10-23****6*10-21
ЕКPbS= 1·10-28. PbS(тв)↔ Pb2+(р) + S2-(р) литрдегі мольге шаққанда тұздың ерігіштігі:********* А) қорғасын сульфатының еріткіштігі 1·10-14 моль/л
Екі негізді қышқылдар:********* A) H2S B) H2SO4
C) H2CO3
Екіатомды молекулаларда байланыстардың иондық сипатының арту реттілігін анықтаңдар 1- CaCl2, 2- MgCl2, 3- Cl2, 4- HCl, 5- KCl:********* A) 34215
Екіатомды молекулалардың полярлығы мына ретте артады:  ********* A) 51243
********* A) 51243
Ең берік емемс химиялық байланыс:********* A) Сутектік B) молекула аралық
Ең берік молекулааралық сутектік байланысы бар заттар:********* A) HF
Ең берік сутектік қосылыстың химиялық формуласы:********* A) NH3
Еріген затты еріткішке қосу мынаған алып келеді:********* А) ерітіндінің қайнау температурасын жоғарылатады B) еріткіштің қаныққан бу қысымын төмендетеді C) осмостық қысымды көтереді
Ерітінді бетіндегі қаныққан бу қысымы:********* A) таза ерітінді бетінен төмен
Ерітіндідегі сутегі иондарының концентрацисы 10-3моль\л ерітіндінің рН және рОН-ы:********* А) рН=3 В) рОН=11
Ерітінділерден мырышты жеңіл ығыстырады:********* A) Кадмий B) Кобальт C) Мыс
Ерітіндінің қайнау температурасы:********* A) еріткіштің қайнау температурасынан жоғары
Ерітіндінің молярлығы-бұл сан:********* A) 1 кг еріткіште еріген заттың молі
Ерітіндінің молярлығы-бұл сан:********* A) 1 л ерітіндіде еріген заттың молі
Еру шегінің дәрежесі бойынша ерітінділер бөлінеді******** Қаныққан\\\\\\\Аса қаныққан\\\\\\\\\Қанықпаған
Ерітіндіде еритін заттыңдисперстік бөлшегі бойынша ажыратады****** Нағыз\\\\\\\Коллоидты\\\\\\Өрескел дисперсті
Ерітіндінің массалық үлесі- еритін заттардың массасы********* 100 г ерітіндіде\\\\0,1 кг ерітіндіде\\\\\102г ерітіндіде
Ж
Жабық жүйеге тән ерекшеліктер:********* A) қоршаған ортамен зат алмасу болмай,тек энергия алмасуы мүмкін
Жалпақ квадратты формалы комплексі бар иондар :*********[Аu(CN)4]- ********* [Pd(NH3)4]2+
Жалпақ квадратты формалы комплексі бар иондар: [Аu(CN)4]-\\\\\\\[Pd(NH3)4]2+\\\\\\\\\\[PtCl4]2-
Жану энтальпиясы (ΔН298) С2H5OH(ж) -реакция энтальпиясына тең:********* A)С2H5OH(ж) + 3О2(г) = 2CO2(г) + 3H2O(ж)
Жәй заттар – типтік тотықсыздандырғыштар:********* A) сутегі B) көміртегі C) магний
Жоғарғы электртерістілік мына элементтерде:********* A) F B) СІ C) І
Жоғары температурада реакция өздігінен өтеді:******** *энтропия артуымен,эндотермиялық жүйенің көлемінің артуымен және энергия жұтылумен
Жүйе СаСО3→Са2++СО32- үшін ерігіштік көбейтіндісін(ЕК) қолданып, оның тұнбаға түсу жолын көрсетіңіз(ЕК(СаСО3)=5*10-9):********* CdCl2; EK(CdCO3) =2.5*10-14****MnCl2; EK(MnCO3) =8.8*10-11****AgNO3; EK(Ag2CO3) =6.2*10-12
Жүйе үшін энтропияның максималды мәні:********* 2 моль Br2(газ) *********4 моль Br2(газ)
Жүйенің қысымын екі, үш, төрт есе кеміткенде CО2+Н2↔ CO+ H2O реакция жылдамдығы сәйкесінше төмендейді :*********4есе*********9есе
Жүйенің реттілік және ретсіздік өлшемін анықтаушы:********* А) энтропия B) энтальпия
Жүйенің энтропиясы өседі:********* A) Қатты зат балқығанда B) Газ таралғанда C) Сұйықтың қайнау үрдісінде
Жылдамдық жүйенің көлем бірлігіне заттың концентрациясының өзгеруісен анықталатын реакциялар:********* H2+Cl2↔ 2HCl*********2CO+O2↔ 2CO2
Жылдамдық фазааралық аумағының бірлік бетіндегі заттың концентрациясының өзгеруімен анықталатын реакциялар:********* 2Na+Cl2↔ 2NaCl*********Fe+CuCl2↔FeCl2+Cu
Жылу эффектілері нөлден жоғары реакциялар:********* N2O4↔2NO2*********CH4+ 2H2O ↔ CO2+4H2
Жылу эффектісі нөлден төмен реакциялар:********* 2H2O2→ H2O+O2*********N2 +3H2↔ 2NH3
З
Зертханада гидроксидтердің ерімтал тұздарын сілтімен әрекеттестіру жолымен алынатын металдар:********* Mg, Zn
Зертханада оттегін мына реакция бойынша алады:********* A) KClO3  B) KMnO4
B) KMnO4  C) NaNO3
C) NaNO3 
Зертханада хлорды мына реакция бойынша алады:********* A) HCl(конц) + MnO2 → B) HCl + KMnO4 → C) NaCl(раствор) 
И
Идеал ерітінділерге жатады ********* A) ∆H=0 B) ∆V=0
Идеал ерітінділердің заңдары:********* Рауль****Вант-Гофф****Коновалов
Инертті анодқа жатады:********* A) графит, платина
Иондану энергиясы ең төмен мәнде болатын:********* A) I топтың s-элементтері
Иондану энергиясы өлшемі:********* A)  B)
B) 
Иондану энергиясы-бұл:********* A) бейтарап атомнан электронды үзуге қажет энергия мөлшері;
Иондардың поляризациясы тұрғысынан тұздардың термиялық беріктілігін шартты салыстыруға болады:********* BaCO3 -MgCO3
Иондық химиялық байланыс мынадай байланыс болып табылады:********* A) бағытталмаған B) қаннықпаған C) берік
К
k1 және k2 – тура және кері химиялық реакциялардың жылдамдық константасы  Химиялық тепе-теңдік күйіне жеткен кезінде тепе-теңдік тұрақтысы К =...:********* A) k1/k2
Химиялық тепе-теңдік күйіне жеткен кезінде тепе-теңдік тұрақтысы К =...:********* A) k1/k2
K2S; SiS2; Al2S2 сульфиттері кіреді және гидролизденеді:********* A) SiS2 – қышқылдық қайтымсыз гидролизденеді B) K2S – негіздік қайтымды гидролизденеді
K2SO3 + KMnO4 + H2SO4→ реакция өнімдері ********* А) H2O, MnSO4 В) K2SO4
KJ + H2O2 + H2SO4 → J2 + K2SO4 + H2O реакциясында сутегі пероксидінің, калий иодидінің рөлін және теңдеудің оң жағының коэффициенттерінің қосындысы нешеге тең:********* A) Тотықтырғыш B) Тотықсыздандырғыш C) 4
KMnO₄ + H₂O₂ + H₂S₄O →….. реакциясындағы тек тотықтырғыш қасиет көрсететін және тотықсыздандырғышты, оның эквивалентін анықтаңыздар:********* A) KMnO₄, SO₃ B) сутегі пероксиді C) ½
KNO3 ерітіндісінің электролизі кезінде катодта жүретін процесс:****** A) су молекуласының тотықсыздануы
К электрондық қабаттың қабаттың максимальді сиымдылығы:********* A) 2
К[Ag(СN)2] қосылысында кешенді ионның зарядын,тотығу дәрежесі және кешен түзушінің координациялық санын анықтаңдар:********* А) -1, +1, 2
К+, Cl3+, F- иондарының электрондық формуласы:********* A) 1S2 2S2 2p6 3S2 3p6 4S1 B) 1S2 2S2 2p6 3S2 3p5 C) 1S2 2S2 2p5
К3[Fe(CN)6] кешенді қосылысында кешентүзушінің d-орбиталдарының тармақталу энергиясы жұптасқан энергиядан жоғары. Аталған кешен:********* A) төменгіспинді B)парамагнитті C)октаэдрлі
К4[Fe(CN)6] қосылысына тән:********* А) сары қан түсті тұз В) орталық атомы темір (ІІ)
Калий перманганады тотықсызданады:********* A) бейтарап ортада MnO2 – дейін B) сілтілік ортада K2MnO4 – дейін
Калий перманганады тотықсызданады:********* A) қышқыл ортада Mn+2 – дейін B) сілтілік ортада K2MnO4 – дейін
Калий гидроксиді әрекеттесетін оксид:********* SO3
Кальций сульфатының қаныққан ерітіндісі тепе-теңдік CaSO4(тв)↔ Ca2+ (р) + SO42- (р) Кальций сульфатының еріткіштік көбейтіндісі тең:********* А) ПР CaSO4=[ Ca2+]·[ SO42-]
Кальцийдің дигидрофосфатында фосфордың, кальцийдің, оттегінің массалық үлесі:********* A) 26 B) 27 C) 17
Кальцийдің қышқылдық тұзы:********* Ca(HCO3)2
Катионды комплекс:********* [Cr(NH3)5Cl]SO4********* [Cu(NH3)4] SO4
Катионды типтегі кешенді қосылыс********* А) [Co(NH3)4]Cl3 В) [ Fe(H2O)6]SO4
Катионы, необразующие с фосфат-анионами осадок:********* A) K+ B) Rb+ C) Cs+
Катод – электродында жүретін процесс:********* A) электролит катиондарының тотықсыздануы;
Кванттық энергия туралы болжамды алғаш айтқан ғалым:********* A) М.Планк
Кез-келген температурада реакция өз бетінше өтеді:********* Энтропияның өсуімен экзотермиялық********* Энергия бөлінуімен және жүйенің көлемінің артуымен
Кестеде n, l, ml және ms электрондардың квант сандары келтірілген
| Электрон | первый | второй | третий |
| n | |||
| L | |||
| ml | +1 | -1 | |
| ms | +1/2 | +1/2 | +1/2 |
электрондар күйін анықтаңдар:********* A) 5d3
Кейбір реакциялар үшін активтендіру энергиясы (ЕА) және реакцияның жылу эффектісі (∆H) мынадай мәндерге ие:********* ЕА=50 кДж/моль; ∆H= +40 кДж.
Катализатор қатысында ЕА және ∆H мәндері тең болуы мүмкін:********* ЕА=30, ∆H= +40****ЕА=20, ∆H= +40****ЕА=10, ∆H= +40
Кейбір реакциялар үшін активтенедіру энергиясы (ЕА) және реакцияның жылу эффектісі (∆H) мынадай мәндерге ие:********* ЕА=100 кДж/моль; ∆H=-20 кДж.
Катализатор қатысында ЕА және ∆H мәндері тең болуы мүмкін:***** ЕА=60, ∆H= -20 ****ЕА=50, ∆H= -20****ЕА=40, ∆H= -20
Келесі қосылыстарда иондық байланыс:********* A) AlCl3 B) NaCl
Келесі қышқылдарүшін молярлық және нормалдық концентрациялары бір-біріне тең:********* HBr****HNO3****HCl
Келтірілген реакцияның типін көрсетіңіз 2Zn+O2®2ZnO********* А)қосылу
Келтірілегн фазалық ауысудан эндотермиялық болатыны:********* A) Hg(с) = Hg(г) B) Na(қ) = Na(г) C) SO3(с) = SO3(г)
Келтірілегн фазалық ауысудан эндотермиялық болатыны:********* A) I2(қ) = I2(г) B) S(ромб.) = S(г) C) NaOH(қ) = NaOH(г)
Кері химиялық реацияның жылдамдығы тең 2NO2 = 2NO + O2:********* A) k2*[NO]2*[O2]
Кешеннің геометриялық формасы-жазық квадрат,гибридтену түрі:********* A)sp2d
Кешеннің геометриялық формасы-октоэдр,гибридтену түрі:********* A)sp3d2
Кешеннің геометриялық формасы-сызықтық,гибридтену түрі:********* A)sp
Кешеннің геометриялық формасы-тетраэдр,гибридтену түрі:********* A)sp3
Кипп аппараты мына затты алуға қолданады:********* А) СО2 B) Н2
Ковалентті байланыс қасиеті:********* A) бағытталуы B) қанығуы C) полярлығы
Ковалентті полюссіз молекулалар:********* А) N2, O2
Ковалентті химиялық байланыс мынадай байланыс болып табылады:********* A) қанныққан B) бағытталған C) берік
Коваленттік полюссіз байланыс мына молекулаларда:********* A) H2 B) O2 C) СІ2
Коваленттік полюсті байланыс мына молекулаларда:********* A) HCl B) НІ C) НҒ
Комплекс түзуші мен лигандалар арасындағы байланыс********* Комплекстің ерігіштігі*********Комплекстің тұтқырлығы
Комплекстер – диамагнитиктер, орталық атомның конфигурциясы :*********d6*********d10
Комплекстүзушінің концентрациясы неғұрлым төмен болатын ион:********* [Ag(CN)2]2-; KT =1.0*10-21********* [Hg(SCN)4] 2- ; KT =1.0*10-22
Комплексті қосылыстарға тән реакциялар :*********Алмасу*********Орынбасу
Комплексті негіздер:********* [Zn (NH3)4] (OH)2********* [Cu(NH3)4] (OH)2
Комплекстік ионда координациялық сан анықтайды:********* Комплекс түзуші гибридтелу типі*********Комплекстің геометриялық формасы
Комплекстің сыртқы және ішкі сфераларының иондары арасындағы байланыс:********* Иондық*********Күшті полярлы коваленттік
КОН балқымасының электролизі кезінде катодта және анодта бөлінетін зат:********* А) К, О2
КОН ерітіндісімен реакциясында, егер КН₂РО₄; К₂НРО₄; К₃РО₄ түзілсе, Н₃РО₄ - тің эквиваленттік молярлық массасы тең:********* A) 98 B) 49 C) 32,7
КОН ерітіндісінің электролизі кезінде катодта және анодта бөлінетін зат:********* А) Н2, О2
КОН және KCl суда еру үрдісі:********* A) экзотермиялық B)эндотермиялық
КОН эквивалентінің молярлық массасы:********* А) 56
Конц. НNO3 мен конц. Н2SO4 пассивтенеді:********* А) Al В) Cr
Концентрлі күкірт қышқылының артық мөлшерінде қыздырып, мысты еріткенде түзілетін заттар:********* А) H2O, CuSO4 и SO2 В) CuSO4, H2O, SO2
Кординациялық изомерия мүмкіндігі бар, кешенді қосылыс:********* A) [Pt(NH3)4][CuCl4]
B) [Co(NH3)6][Cr(CN)6]
Көміртегі (IV) оксиді молекуласына тән:********* A) 2π- байланыстар B) 2σ- байланыстар C) сызықтық молекула
Көміртегі мына қосылыстарда ең жоғарғы тотығу дәрежесін көрсетеді:********* А) СаСО3 В) СО2
көміртегі атомнының гиридтену түрі:********* A) сызықтық B) 2σ және 2π C) sp
Көміртек диоксиді молекуласының құрылысы, σ- және π – байланыстарының саны, көміртегі атомнының гиридтену түрі:********* A) сызықтық B) 2σ және 2π C) sp
Кристаллизация және конденсация үрдістері мынаған алып келеді:********* A) энтропияның төмендеуіне;
Күй функциясы болмайтын термодинамикалық функциялар:********* А)жылу B) жұмыс
Күйдің термодинамикалық функциялары:********* Энтропия, энтальпия*********энтропия, Гиббс энергиясы
Күкірт атомындағы протондар мен нейтрондардың қосындысы:********* A) 32
Күкірт қышқылы:********* A) екі типті тұздар түзеді: гидросульфидтер, сульфидтер B) ерітінділерінде мына иондар болады:********* HSO3-, SO32-
Күкірт элементінің соңғы электроны үшін оның максималды қозған күйінде бас орбиталь немесе квант сандары:********* n=3
Күміс иондары(I)****** A) d10 конфигурациялы****B) гдроксиді тұрақсыз
Күрделі заттар:********* Қант
Күшті тотықтырғыштар:********* A) K2Cr2O7 B) KMnO4 C) K2CrO4
Күшті электролиттер:********* A) HNO3 B) HCl C) HI
Күшті электролиттер:********* A) K2SO4 B) KNO3 C) NaCl
Күшті электролиттер:********* A) Na2SO4 B) HCl C) Cu(NO3)2
Күшті қышқылдар:********* A) H2SO4 B) HCl C) HNO3
Күшті полярлы байланысқан заттар:********* H2O; ЭТ(Н)=2,1; ЭТ(О)=3,5*********HF; ЭТ(Н)=2,1; ЭТ(F)=4,0
Күшті электролиттер молекулаларындағы байланыс түрі:********* Иондық
Кіші периодтарда элементтердің атом радиустарының кішіреюі мынаған байланысты:********* A) сыртқы электрондық қабаттың толуымен
Қ
Қай зат Льюис қышқылы және Льюис негізі болып табылады: MgO+CO2→********* А) MgO – негіз, CO2 – қышқыл
Қай зат Льюис қышқылы және Льюис негізі болып табылады: Na2O+SO2→*********А) Na2O – негіз, SO2 - қышқыл
Қай реакция тотығу-тотықсыздану реакциясы бола алады:********* A) Аg + Н2SO4 = Аg2SO4 + SO2 + Н2O
B) КМnO4 + КОН = К2МnO4 + O2 + Н2O C) Н2S + НСlO = S + НСl + Н2O
Қай реакция тотығу-тотықсыздану реакциясы бола алмайды:********* A) Н2SO4 + ВаС12 → ВаSO4 + 2НСl
B) СuSO4 + КОН → Сu(ОН)2 + К2SO4 C) Nа2Сr2O7 + NаОН → 2Nа2СrO4 + Н2O
Қай элементте негізінен барлық электрондары жұптасқан:********* А) Hg B) Cd
Қайтымды реакция:********* A) N2 + 3H2 = 3NH2
B) H2 + I2 = 2HI C) CO + H2 = CO2 + H2
Қайтымды реакция:********* A) H2O = H+ + OH-
B) HCO  = H+ + CO
= H+ + CO  C) 2SO2 + O2 = 2SO3
C) 2SO2 + O2 = 2SO3
Қайтымсыз реакция:********* A) NH4NO3 → N2O + H2O
B) Fe(OH)3 → Fe2O3 + H2O C) (NH4)2Cr2O7 → N2 + Cr2O7 + H2O
Қалыпты жағдай:********* А) Р=101,3 кПа: В) Т=273К
Қалыпты жағдайда температура мен қысым:********* А)273 и 101,3
Қалыпты жағдайдағы бір моль газдың көлемі:********* А)22,4
Қандай жағдайда реакция өздігінен жүруі мүмкін:********* А) ΔG < 0 B) ΔH < 0
Қатардағы диамагнитті бөлшектер:********* A) 
Қатардағы парамагнитті бөлшектер:********* A) 
Қатты заттың ерігіштігі тәуелді:********* еріген заттың полярлығы****еріткіштің полярлығы****температуралар
Қозған күй мүмкін болмайтын элемент:********* Хром
Қозған күйдегі үш жұптаспаған электроны бар:********* Бор
Қосылу реакциясы:********* 2Na+Cl2→2NaCl
Қосылу реакциясы:********* A) NH3 + HCl = NH4Cl
B) S + O2 = SO2 C) Na + O2 = Na2 O
Қосылыстарда хлордың тотығу дәрежесі:********* A) -1
B) +3 C) +7
Қосылыстарында валенттігі топ нөмірінен артатын химиялық элементтер:********* A) мыс,күміс,алтын
Қосылыстарында орталық атомдары sp2-гибридтенукүйінде:********* A) ВCl3 B) HCHO
Қосымша квант саны l = 2 болатын,электрондық қабаттағы электрондардың максималь саны мынаған тең:********* A) 10
Қосымша квант саны l = 4 болатын электрондық қабаттағы электрондардың максималь саны:********* A) 18
Қосымша квант саны l мәндері мен d, f, p, s электрондық орбитальдардың мәндері арасындағы сәйкестікті анықтаңдар:********* A) 2310
Құрамы(массалық бөлігі бойынша): С-54,54%, Н-9,1%, О-36,36% және ауа бойынша тығыздығы 3,03 болатын заттың болярлық массасы, формуласы, атауы:********* 88 г/моль
Құрамында 60% метан және 40% этан бар 10 л газ қоспасын жағу үшін қажетті оттегінің (қ.ж.) көлемі:********* 2,6*10л
Құрылым бірлігі иондар болатын заттар:********* Натрий хлориді
Қыздырғанда термиялықтұрақсыз және жеңіл ыдырайды:********* A) аммонийдің барлық түрлері B) азот қышқылының барлық тұздары C) оттекті қышқылдардың барлық тұздары
Қысымды жоғарылатқанда газдардың суда ерігіштігі:********* A) артады
Қысымды жоғарылату реакцияларда өнімнің шығымын жоғарылатады:********* A) 2NO(г) + O2(г) = 2NO2(г) B) PCl3(г) + Cl2(г) = PCl5(г) C) 6HF(г) + N2(г) = 2NF3(г) + 3H2(г)
Қысымның өзгеруі химиялық тепе-теңдіктің ығысуына ешқандай әсер етпейтін реакция:********* N2 +O2↔ 2NO*********C+O2↔ CO2
Қышқыл орта мына тұздар ерітінділерінде:*********A) NH4Cl B) FeCl2 C) Cu SO4
Қышқыл тұзды көрсет:********* А)Na HSO3
Қышқыл түзбейтін оксидтер:********* A) NO B) BaO C) Ag2O
Қышқылдармен де, сілтілермен де әрекеттеседі:********* A) Мырыш B) Бериллий C) Алюминий
Қышқылдық оксидтер қатарын көрсет********* А)SiO2,Mn2O7,CrO3
Қышқылдық тұз түзетін қышқыл:********* Күкірт және күкіртті қышқыл
Қышқылдық-негіздік қасиет көрсететін гидроксидтер:********* Zn(OH)2 және Al(OH)3
Л
Лантанойдтар********** A) сирек металдар B) f-элементы
Луи Де Бройль теңдеуінің өрнектелуі:********* A) 
Луи Де Бройль:********* A) микробөлшектің қозғалысы-толқындық үрдіс
Льюис теориясында негіз ретінде алынатын үрдіс:********* А) электрон жұбының рөлін ерекшелейді
Льюис ұстанымына сәйкес қышқылға анықтама бер:*********А) қышқыл-электрон жұбын беретін акцептор
Льюис ұстанымына сәйкес негізге анықтама бер:*********А) негіз-электрон жұбын беретін донор
М
М.Планк теңдеуінің өрнектелуі:********* A) 
Магний тұзы (II):********* A) кристаллогидраттар түзеді B) көбіне суда ерігіш
Магнит квант саны мына мәндерді қабылдайды:********* A) - l, 0, + l
Максимальная емкость электронного N:********* A) 32
Максимальная емкость электронного слоя L:********* A) 18
Максимальная емкость электронного слоя М:********* A) 8
Марганец оксидтерінің қасиеттері:********* A) MnO2 – қышқыл сипатты амфотерлі оксид В) Mn2O7 – қышқылдық оксид
Марганец оксидтерінің негіздік қасиетінің арту реттілігін анықтаңдар 1- MnO2, 2- Mn2O7, 3MnO, 4- MnO3:********* A) 2413
Масса- энергия сақталу заңының өрнектелуі:********* A) 
Мәндері жүйенің бастакпқы және соңғы күйімен анықталатын термодинамикалық функциялар :*********Энтропия, энтальпия*********Энтропия, Гиббс энергиясы
Металдың электрондық потенциалы анықтайды:********* A) тотықтырғыштық қабілеттілігінВ) тотықсыздандырғыштық қабілеттігі
Металл атомдарының иондану энергиясының арту ретін анықтаңдар
Металл магний сумен бөледі:********* А) сутегі B) гидроксид
Металлдарға тән қасиет:********* A) Механикалық беріктігі B) Жоғары балқу температурасы
Металлдарға тән қасиет:********* A) Электрөткізгіштік B) жылуөткізгіштік C) майырылғыштық
Метан молекуласының орталық атомының гибриттелу түрі, геометриялық формасы, немесе валенттік бұрышы:*********Sp3*********109028
Минимальды энергия тұрғысына сәйкес атомдық орбитальдарды электрондармен толтыру реті:********* 4s→3d
Молекулада донорлы-акцепторлы байланыс түзіледі:*********[ Cu(ОH)4]SO4*********NH4Cl
Молекулалар арасында сутекті байланыс:********* А)HF B) H2O
Молекулалар арасында сутектік байланыс:********* A) H2O B) NH3 C) N2H4
Молекулалар арасында сутектік байланыс:********* A) HF B) NH2ОН C) Н2О
Молекулалар арасында сутектік байланыс:********* A) Н2О2 B) NH3 C) N2H4
Молекулалар арасындағы сутектік байланыс:********* А)HF B) H2O
Молекулалардағы донорлы-акцепторлы байланыс түзілу шарттары:********* Акцептор рөлін атқаратаны атом (атомдар тобы) *********Донор рөлін атқаратаны атом (атомдар тобы)
Молекулалығы (М) және реакция реті (n) CO+Cl2↔ COCl2:********* М=2****n=2****М=n
Молекулалығы (М) және реакция реті (n) FeO+ C↔ Fe+CO:********* М=2****n=0****М≠n
Молекуласында бір σ-және екі π-байланысы бар:********* A) N2
Молекуласында төрт σ-байланысы бар:*********A) CH4
Молекулаішілік тотығу-тотықсыздану реакциясы:********* A) (NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O B) 2Cu(NO3)2 = 2CuO + 4NO2 + O2 C) CH4 = C + 2H2
Молекулаішілік тотығу-тотықсыздану реакциясы:********* A) 3AuF = AuF3 + 2Au B) 2KMnO4 = K2MnO4 + MnO2 + O2 C) 2KNO3 = 2KNO2 + O2
Молекулаішілік тотығу-тотықсыздану реакциясы:********* A) 3AuF → AuF3 + 2Au B) 2KMnO4 → K2MnO4 + MnO2 + O2 C) 2KNO3 → 2KNO2 + O2
Молекулярлық торы бар зат:********* А)I2 B) Br2
Молярлық және нормалдық концентрациялары бір-біріне тең болатын негіздер үшін:********* NaOH****NH4OH****KOH
Монодентантты лигандалар:********* A) СN-, NH3-, I- B) Сl-, Br-, F-
Мұзы бар термос-бұл термодинамикалық жүйе:********* A) оқшауланған
Мүмкін емес реакциялар:********* Na2SO4+H2CO3→
Мына әрекеттесулелдің реакция теңдеулеріндегі барлық стехиометриялық коэффиценттердің қосындысы:********* A) натрий мен тұз қышқылы B) натримен судың қышқылы
Мына тұздар қышқылдық орта көрсетеді:********* А) FeSО4 В) FeCl2
Мына бөлшектерде донорлы – акцепторлы механизм бойынша байланыс түзілді:********* A) NH 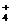 B) ВH
B) ВH 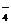 C) H2SiF6
C) H2SiF6
Мына бөлшектерде донорлы – акцепторлы механизм бойынша байланыс түзілді:********* A) NH B) ВH  C) H2SiF6
C) H2SiF6
Мына зат үшін түзілу энтальпиясы нөльге тең:********* A) оттегі
Мына заттарды қосқанда натри карбонатының гидролизі күшейеді:********* A) ZnCl2 B) CuCl2
Мына заттың түзілу жылуы нөльге тең:********* A) оттегі
Мына иондардың түзілуі мырыштың амфотерлігін дәлелдейді:********* А) [Zn(NH3)4 ]2+ В) [Zn(OH)4 ]2-
Мына қатар бойынша
HNO3→ H2SO4→ HСlO4:********* Оксоқышқылдардың күші артады
Мына қатар бойынша HNO3→HPO3→HAsO3:********* Оксоқышқылдардың күші төмендейді
Мына қатарларда атом радиустары артады:********* A) F –Cl- Br B) Li –Na- K C) N –P- Bi
Мына қатарларда солдан оңға қарай иондар радиустары өседі:********* A) Al+3, Mg+2, Na+ B) Be+2, Mg+2, Ca+2 C) Cl-, S-2, P-3
Мына қосылыстарда ең жоғарғы иондану дәрежесі:********* A) K-Cl B) K-I C) Na-Cl
Мына металдардың нитраттары ыдырағанда оксидтер түзіледі:********* А) мыс В) барий
Мына молекулада валенттік бұрыш 180о тең:********* A) BeCl2 B) CO2 C) XeF2
Мына реакция: N2 +3H2↔ 2NH3, ∆H <0 үшін химиялық тепе-теңдіктің кері реакция бағытына ығысатын жағдай:********* Аммиактың концентрациясы өскенде*********Азоттың концентрациясы кемігенде
Мына реакцияда 2H2S + SO2 = 3S + 2H2O тотықсыздандырғыштың эквиваленттік факторы:********* A) 
Мына реакцияда 4NH3(г) +3O2(г)®2N2(г) + 6H2O(г) тепе теңдік оңға ығысады:********* А) қысымның төмендеуі B) NH3 концентрациясының артуы
Мына реакцияда 3K2SO3 + K2Cr2O7 + 4H2SO4 = 3K2SO4
 2018-01-21
2018-01-21 2010
2010






