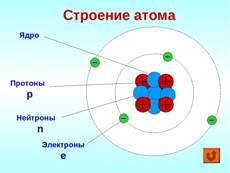
 Атом состоит из положительного ядра, в состав которого входят положительные протоны (р) и нейтральные нейтроны (n). Вокруг ядра движутся отрицательные электроны (e)
Атом состоит из положительного ядра, в состав которого входят положительные протоны (р) и нейтральные нейтроны (n). Вокруг ядра движутся отрицательные электроны (e)
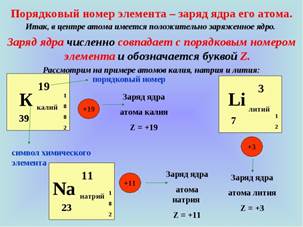 Порядковый номер элемента в Периодической системе равен заряду ядра атома.
Порядковый номер элемента в Периодической системе равен заряду ядра атома.
Электроны движутся вокруг ядра на разном расстоянии от него, говорят, движутся по энергетическим уровням (орбиталям).
№ периода Периодической в таблице равен количеству энергетических уровней.
 Например. Литий находится во втором периоде (горизонтальном ряду), значит у него два энергетических уровня
Например. Литий находится во втором периоде (горизонтальном ряду), значит у него два энергетических уровня
 Это изображают так: 3 – это заряд ядра (его порядковый номер) и две дуги - - два энергетических уровня
Это изображают так: 3 – это заряд ядра (его порядковый номер) и две дуги - - два энергетических уровня
Теперь разберемся как распределяются электроны по энергетическим уровням.
Нужно запомнить, что на первом уровне может находиться только 1 или 2 электрона, на втором и третьем – от одного до восьми.
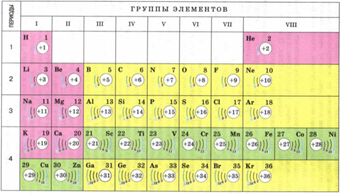
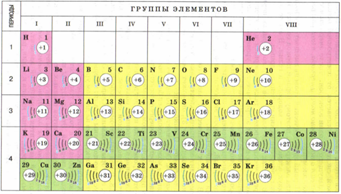 Для того, чтобы понять сколько у атома электронов на каждом уровне нужно обратиться к Периодической системе.
Для того, чтобы понять сколько у атома электронов на каждом уровне нужно обратиться к Периодической системе.
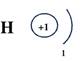 Начнем с водорода. Он первый в таблице. Его порядковый номер=1, значит заряд ядра тоже 1. Заряд ядра равен количеству электронов, следовательно у водорода всего 1 электрон. Водород находится в первом периоде, значит у него один энергетический уровень и на этом уровне находится 1 электрон.
Начнем с водорода. Он первый в таблице. Его порядковый номер=1, значит заряд ядра тоже 1. Заряд ядра равен количеству электронов, следовательно у водорода всего 1 электрон. Водород находится в первом периоде, значит у него один энергетический уровень и на этом уровне находится 1 электрон.
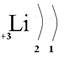 Теперь попробуем составить такую же схему для лития. Порядковый номер лития =3, значит заряд ядра +3, он находится во втором периоде, значит у него два энергетических уровня. Таким образом, на двух уровнях у лития будет три электрона. Как они распределяться? Первые два электрона пойдут на первый уровень (на первом уровне максимально может быть только 2 электрона), а один электрон пойдет на второй уровень.
Теперь попробуем составить такую же схему для лития. Порядковый номер лития =3, значит заряд ядра +3, он находится во втором периоде, значит у него два энергетических уровня. Таким образом, на двух уровнях у лития будет три электрона. Как они распределяться? Первые два электрона пойдут на первый уровень (на первом уровне максимально может быть только 2 электрона), а один электрон пойдет на второй уровень.
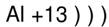 Составим схему для алюминия. Его порядковый номер 13, значит заряд ядра у него +13 и всего электронов 13.. Он находится в третьем периоде, значит у него три энергетических уровня.
Составим схему для алюминия. Его порядковый номер 13, значит заряд ядра у него +13 и всего электронов 13.. Он находится в третьем периоде, значит у него три энергетических уровня.
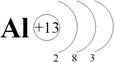 Теперь нужно распределить эти электроны (13) по трем уровням. На первом уровне максимально может находиться 2 электрона, значит на перовом уровне 2 электрона. На втором и третьем уровне, как писалось выше, может быть 1-8 электронов. Если уровень завершен, т.е. за ним появился следующий уровень, тогда на нем будет 8 электронов. Значит на первом уровне у алюминия – 2 электрона, на втором 8, следовательно, на третьем остается 3 электрона.
Теперь нужно распределить эти электроны (13) по трем уровням. На первом уровне максимально может находиться 2 электрона, значит на перовом уровне 2 электрона. На втором и третьем уровне, как писалось выше, может быть 1-8 электронов. Если уровень завершен, т.е. за ним появился следующий уровень, тогда на нем будет 8 электронов. Значит на первом уровне у алюминия – 2 электрона, на втором 8, следовательно, на третьем остается 3 электрона.
Такую запись строения атома с распределением электронов по уровням называют электронной конфигурацией атомов или электронным паспортом атома.
 2020-05-21
2020-05-21 306
306






