Эмиссионная фотометрия пламени основана на измерен интенсивности излучения атомов, возбуждетных пламенем. Эмиссионнaя фотометрия применяется для определения легковоэбуждаемых элементов (потенциал возбужденияС4 эв), имеющих потенциал ионизации не более 8 эв. При постоянной температуре интенсивность излучения 1 прямопропорциональиа концентрации определяемого элемента в анализируемом растворе. Однако прямолинейная зависимость 1 от C при возбуждении атомов в пламени в действительности существует лишь в определенных областях концентрации. Прямолинейная зависимость 1 от C нарушает вследствие явлений самопоглощения, ионизации, образовани в пламени газообразных или труднолетучих соединений. Кром того, на интенсивность излучения влияет состав анализируемо раствора, степень го ‚распылениаи качеСтво пламени. (1n_ рабочий прямолиненныи участок калибровочного графика всегда определяют экспериментально и все измерения производят при неизменном режиме работы прибора..(рис. 60) [1j. Если в пламени преобладающим влиянием оказывается влияние самопоглощения, то при малых концентрациях между 1 и C наблюдается прямолинейная зависимость, a при больших концентрациях определяемого эле-мента величина 1 изменяется пропорцио- ig! нальио У C (рис. 60, кривая 1J. Если- преоб-ладающее влияние оказывает ионизация (на-пример, для щелочных металлов c низкими потенциалами ионизации), то при малых кон-центрациях (P/Ки < 0,01) интенсивность излу-чения 1 изменяется пропорционально квадрату концентрации, a при больших значениях С(Р/Кн > 100) наблюдается линейная зависимость 1 от C (кривая 2). Крнвы е 1 и 2 характерны для щелочных и щелочноземельных металлов. Y элементов третьей группы часто наблюдается линейная зависимость 1 от C. На форме кривой зависимости 1 = f (C) часто сказывается влияние самопоглощения.._ и ионизации опновоеменно.
ИЗМЕРЕНИЕ ИНТЕНСИВНОСТИ ИЗЛУЧЕНИЯ Для измерения интенсивности излучения применяются различ-ны е приборы: фотометры co светофильтрами и спектрофотометры многоканальные, rtозволяющие проводить анализ одновременно»а несколько элементов, одноканальны е, работающие по методу пря-мого отсчета, и регистрирующие [1-4]. Наиболее распространен-ными приборами являются пламенные фотометры или спектрофо-тометры, работающие по методу прямого отсчета. Схема действия такого прибора состоит в следующем (рис. 61): анализируемый раствор из стакана 2 при помощи струи сжатого воздуха или дру-гого газа подается через распылитель 3 в камеру и затем в виде аэрозоля поступает в пламя горелки 7. Излучение пламени соби-рается вогнутым зеркалом 8 и. направляется фокусирующей лин-зой 9 на светофильтр (или монохроматор) 10, который пропускает к фотоэлементу 11 излучение только определяемого элемента. Возникающий под действием излучения фототок усиливается усилителем 12 и измеряется чувствительным гальваномет-ром 13.. Многие из описанных приборов для фотометрии пламени яв-ляются оригинальными установками, созданнь;ми на основе спект-рофотометра СФ-4, спектрографов ИСП-28 и ИСП-51 и монохро-маторов УМ-2, ЗМР-2, ИСП-17А. Использование спектрографа ИСП-51 в сочетании c фотоэлектрической приставкой типа ФЭП-1 позволяет проводить анализ с высокой чувствительностью (д, 10-' мкг/мл Na, 10-;.икг/.и_: Li, 1О-3 мкг/мл Rb [8]). фотометры co светофильтрами предназначены для акал в основном, щелочных и щелочноземельных элементов. Опредё ние других элементов требует применения специальных света фильтров. Фотометр ФПЛ-1.предназначен для экспрессанализо Na, K и Са. Пламенный фотометр ГП-21А, работающий на ацет леново-воздушном пламени и имеющий набор интерференциальных светофильтров, применяется для определения
щелочных и щелочнозе,мельныx элементов. Еще большими возможностям обладают пламенный фотометрФПФ -58 и высокочувствтельные фотометры ВПф ВТИ и ПФМ.
Порядок работы. Но робко порядок работы фотометре излагается в` струкции, прилагаемой прибору. Для большинства фотометров он сводится следую щему: включают прибор в сеть переменного тока `(127 или 220 в) и открывают кран газопровода вентиль редуктора балл c горючим газом. Затем зажигают газовую горелку' (рис. 61), и включают компрессор 1, нагнетающий воздуХ в распылитель З, и при помощи регулирующего вентиля добиваются однородного пламени всей сетчатой поверхностью газовой горелки 7. Манометр 5 показывает избыточное давление воздуха, которое не должно превышать 0,5-0,6 ат. B таком состоянии прибор готов для фотометрирования растворов. Для измерения интенсивности излучения определяемого элемента исследуемый раствор при помощи сжатого воздуха подают в распылитель З, откуда он в виде аэрозоля попадает в пламя газовой горелки 7. Перед измерением интенсивности на пути излучения вводят нужный светофильтр (или монохроматор), который пропускает к фотоэлементу только излучение определяемого элемента. Перед фотометрированием исследуемого раствора измеряют интенсивность излучения определяемого элемента в раствор сравнения или дистиллированной воде. После каждого распыления распылитель и горелку тщательно промывают дистиллирова ной водой. Измерение интенсивности изл чения оп.еделяемого элемента в исследуемом и стандартном растворах производят при неизменном режиме работы фотометра. Предосторожности. 1. Не создавать избы точного давления qжа-того воздуха более 1 ат. 2. Не оставлять открытую газовую горелку незажженной. З. Следить за тем, чтобы пламя газовой горелки было одно-родным. 4. При работе c баллоном горючего газа соблюдать все ин-струкции, предусмотренные правилами техники безопасности.
МЕТОДЫ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ Метод сравнения. Определение основано на сравнении интен-сивности излучения исследуемого и стандартного растворов. При-готавливают исследуемый и стандартный растворы определяемого элемента, вводят их в пламя и измеряют величину фототока (от-клонение стрелки гальванометра). Неизвестную копцентрацию С рассчитывают по формуле
С х = Сст ах/а ст
где С и Сст — концентрации исследуемого и стандартного раство-ров; ах и аст — величины фототоков (величины отклонения стрелки гальванометра), соответствующие концентрациям С н Сот. При линейной зависимости a= f (C) более точные результаты получаются c использованйем двух стандартных растворов c кок-центрациёй С, немного большей чем концентрация С исследуе-мого раствора, и С'т — немного меньшей, чем. Неизвестная концентрация Сх рассчитывается интерполированием по формуле:
Сх=С’’ст + С’ст-С’’ст/ a’ст – a’’ ст (а х – а’’ст)
где С' и С'— концентрации стандартных растворов; ах — откло-нение стрелки гальванометра, соответствующее излучению эле-мента при концентрации С; а�т — отклонение стрелки гальвано-метра, соответствующее излучению элемента в стандартном растворе c концентрацией С; аст -- отклонение стрелки гальвано-метра, соответствующее излучению элемента в стандартном рас- творе c концентрацией Сст.
Метод калибровочного графика. По серии стандартных раство-ров известной концентрации на миллиметровой бумаге строят ка-либровочны й график, выражающий зависимость интенсивности излучения (измеренной в делениях шкалы прибора) от концентра-ции элемента в растворе I = f (C) (рис. 62, стр. 216). Затем изме-ряют интенсивность выбранной аналитической линии этого же эле-мента в исследуемом растворе и по калиоровочному графику нахо-дят его концентрацию. Если в выбранном интервале концентраций зависимо 1= f (С) не прямолинейная, то калибровочный график стро 8-10 стандартный растворам, отличаiЬщимся по концентрац не более, чем на 14-15%. Угол наклона прямой калибровочнг графика на самом ПОЛОГОМ участке должен быть не менее 15градусов
Метод добавок. Определение этим методом основано на ср пении интенсивности излучения при фотометрировании исcле мого раствора и исследуемого раствора c добавкой известного.личества определяемого элемента. Неизвестную концентрацию С наxодят графически (стр. 218 или рассчитывают по формуле
Сx = Сq а/ ах+q – ах
где С4 —концентрация добавки в фотометрируемом растворе, ах и ах+q — отклонения стрелки гальванометра (отсчеты), получёi ные при фотометрировании исследуемого раствора и того же р творя c добавкой q определяемого элемента. Метод добавок учитывает влияние уолевого фона и обес вает одинаковые условия для фотометрирования стандартногг исследуемого растворов
ЧУВСТВИТЕЛЬНОСТЬ СПЕКТРОФОТОМЕТРИЧЕСКИх И ФОТОКОЛОРИМЕТРИЧЕСКИХ МЕТОДОВ При спектрофотометриllеских опреде лениях необходима объектllвн я оценка; наименьшего количества вещества, которое может бытьть определено npи помощи цветной реакции. В ряде случаев для таких оцеиок используют максимальные значения молярных коэффициентов погащения Емдкс• Так, например, зная величину Емакс, из уравнения (б) можно рассчитать ми' нимальнуго кониентрацию (н мo:-1r,/,г) вещества, пoддающyюс ся спектрофотометрическому onpeделению
Смин=Dмин/Е макс Lмакс
Если Принять D= 0,001; L= 1 см, Емакс= 100000, то
Смин=1*10в -3/1*10в 5=1*10в-8 моль/л
При увелнченнгг толщНны слоя до L= 10 см чувствительност определения можно повысить в 10 раз, т. e. Смин = l• 10в -9.имогь/л При фотоколориметрисгеских определениях в настоящее время величину Dмин около 0,01 пpизнaют предельно достижимой, a молярны й коэффициент погашении окрашенных соединений обычно не превышает 50000 и С»»» соответственно умегТъгпится д 10 (при l= 1 см). Если иомггить, что в ходе выполнёни анализов производят разбавления и ггспользуют окрашенные c единения co значительно меньшими значениями Емакс, то минимальная определяемая концентрация примесей составит 10в-5 10в-6 моль/л. Как известно, чувствительность реакliии характеризуется н только минимальной концентрац11е1•i, нo н определяемым минимом, т. e. наименьшим количеством вещества, которое может бы' еще обнаружено данным реактивом при определенных условия наблюдения продуктов реакции [8, 10]. Гинзбург и Лурье [11], a также Сендел [2] показали, что чув ствительность цветной реакции одноэначно выражается числом
Микрограммов (1 мкг = 1 • 10_s г) определяемого элемента, превра-щенного в окрашенное соединение, которое в слое раствора c по-ггеречным сечением 1 см2 показывает оптическую плотность, рав-чг1ю 0,001 (условная чувствительность цветной реакции).
B большинстве чувствительных цветных реакций определяемый Минимум при спектрофотометрических и фотоколорсгметрическггх определениях находится в пределах 0,01-0,001 мкг/см2. Во многих paбoтаx чувствителыiость выражают в мкг/.ил, хотя без указания толщиНы поглощaющeго слоя такая характеристика не является ооъектiiвногг. B то же время во многих методических работах чувствитель-ность цветной реакции обычно оценивают, исходя из воспроизво-дНМости предлагаемого аналитического метода. В связи c этим, очевидно, целесообразно [12, 13] использовать две ризли'гные характеристики цветной реакции, одна из которых рассмотрена выше и определяется лишь интенсивностью окраски соответствуюгцего соединения (условная чувствительность цветной реакции: m/s, где m — наименьшее количество определяемого ве-щества, мкг; S — эффективное сечение кюветы, см2), п вторая учи-тывиет погрешности конкретного метода анализа (определяемый минимум m — мкг). Для расчета m/S ы m в уравнении (б) следует заменить C (в моль/л) ее значением
ггг • 10з
С=m*10 в 3/nVA где,г — число атомов определяемого элементаонен моле Кvлу поглощающего свет соединения; твора, мл; A — атомный вес элемента. Следовательно
D = elm 10 в 3/ пVА
(10)
учитывая, что V/l = S, и решая уравнение (10) относительио т вт S = a, получаем соответственfiо: т _
m=DS/e nA*10в3
а=m/S=D/e nA*10в3
Если D — минимальное допустимое значение оптической плотности, то уравнения (11) и (12) позволяют рассчитать наименьшее количество определяемого вещества.
Из уравнения (11) видно, что снижение определяемого мини- ] мума достигается за счет: увеличения молярного коэффициента ] погашения, уменьшения эффективного сечения кюветы, наименьшего допустимого значения оптической плотности Оти.
Первый путь связан с использованием монохроматоров или] узкополосных светофильтров, для которых е примерно равна е.макс (где £ — сред-! ний молярный коэффициент погашения, зависящий от характери-] стики используемого светофильтра), и с поисками новых высоко-1 чувствительных реактивов.
Молярные коэффициенты погашения наиболее интенсивно окра, шенных соединений, как правило, не превышают 100000—120000 и, следовательно, возможности увеличения чувствительности на этой основе принципиально ограничены. Однако, если следы определяемого иона могут служить катализатором какой-либо реакции [14—18], продукты которой окрашены, то чувствительность может быть повышена во много раз. Например, используя каталитическое действие диэтилдитиокарбамината меди на обесцвечивание иод-азидных растворов при К = 420 нм, Бабко и др. [18] предложили методику определения следов меди (до 0,06 мк'г); ^Максимальное значение молярного коэффициента погашения. емакс диэтилдитиокарбамината меди составляет 12800, а условный" моляр-! ный коэффициент каталитической реакции ек равен 3,4-10s при Я = 420 нм, т. е. в 50 раз больше емаКс- Во столько же раз чувстви--тельность определения меди по иод-азидной реакции больше, чем с диэтилдитиокарбаминатом.
Второй путь повышения чувствительности связан с у совершен-! ствованием аналитической методики, аппаратуры и техники изме-1 рений. Уменьшение площади поперечного сечения кювет в сочетав нии с экстракционным концентрированием микропримесей позволяет значительно уменьшить определяемый минимум.
лать следующие оощие заключения по точности дифференциальных спектрофотометрических измерений. r\f Ошибка будет меньше, если:
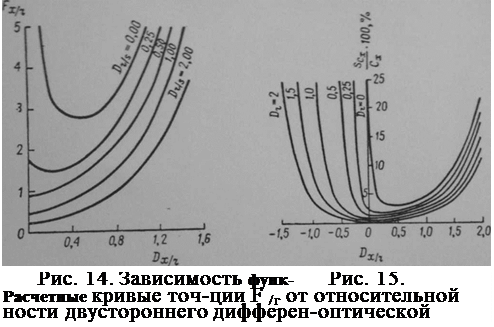 |
1) больше концентрация раствора сравнения (его относительная оптическая плотность, измеренная по отношению к растворителю, должна быть >0,4343);
2) меньше оптическая плотность неизвестного раствора, изме ренная по отношению к раствору сравнения, — наиболее благопри
ятный случай, когда Dxfr '= 0, т. е. концентрации неизвестного рас твора и раствора сравнения равны;
3) меньше стандартное отклонение показаний пропускания;
4) меньше расхождения в длинах рабочих кювет; *;||
5) длиннее используемые кюветы;
6) выше концентрация неизвестного раствора;
7) круче наклон калибровочной кривой, т. е. выше коэффициент
погашения окрашенного соединения;
8) меньше стандартное отклонение наклона*
Некоторые из этих требований находятся в противоречии. Так,
согласно пункту 1, раствор сравнения должен быть как можно более концентрированным. Однако с увеличением концентрации измеряемый фотоэлементом или другим приемником световой сигнал становится все слабее, поэтому величина стандартного отклонения пропускания $г будет увеличиваться, что противоречит пункту 3.
На практике при дифференциальных спектрофотометрических определениях раствор сравнения рекомендуется выбирать возможно более высокой концентрации, при которой еще не наблюдается нарушение закона Бера или оно невелико и удается произвести отсчет с точноегью абсолютного метода [31, 34].
Отметим, что в ряде случаев относительная ошибка определения концентрации оказывается значительно большей, чем это следует из уравнений (14) и (16), из-за ошибок определения параметров калибровочных графиков.
ОСНОВНЫЕ ПРИЕМЫ ФОТОМЕТРИЧЕСКОГО АНАЛИЗА
В зависимости от наличия фотометрической аппаратуры и условий проведения анализа используют различные приемы определения концентрации раствора по светопоглощению. Измерения оптических плотностей стандартных и исследуемых растворов производят при одинаковых условиях.
Метод стандартных серий. В одинаковых колориметрических пробирках равного объема приготавливают исследуемый и стандартные окрашенные растворы. Концентрация исследуемого раствора принимается равной концентрации стандартного раствора, одинакового с ним по интенсивности окраски.
Колориметрическое титрование. В две одинаковые пробирки (или цилиндры) помещают исследуемый окрашенный раствор и дистиллированную воду. Затем в пробирку с водой при перемешивании добавляют из бюретки окрашенный стандартный раствор до одинаковой окраски в обеих пробирках. Неизвестное количество определяемого вещества принимается равным количеству, содержащемуся в добавленном стандартном растворе.
Метод уравнивания. Определение концентрации раствора этим методом основано на уравнивании интенсивности окраски или све-топоглощения исследуемого и стандартного окрашенных растворов.
Способ разбавления..В двух одинаковых градуированных пробирках приготавливают исследуемый и стандартный окрашенные растворы. Добавлением растворителя (дистиллированной воды) к наиболее интенсивно окрашенному раствору добиваются равенства интенсивности окрасок. Неизвестное содержание анализируемого вещества рассчитывают по формула
Qx=qст Vх/Vст или qx=qст hx/hст
где qC7 — количество определяемого вещества в стандартном рас- творе; Ух и Уст — объем исследуемого и стандартного растворов,
соответственно; hx и Аст — высота столба жидкости в пробирках с исследуемым и стандартным растворами, соответственно.
Способ уравнивания в колориметрахсливания. В два одинаковых плоскодонных цилиндра с кранами для сливания (цилиндры Генера) помещают исследуемый и стандартный1 окрашенные растворы. Затем изменением толщины поглощающего слоя / добиваются уравнивания интенсивности окрасок в обоих цилиндрах. Оптические плотности сравниваемых растворов при этбк становятся одинаковыми: Dx = Ьст.
Согласно основному закону светопоглощения
Dx=eСхlx b Dст=еСстlст
откуда СХ1Х == Сст/ст. Измерив толщины слоев окрашенных растворов {1Х и lCt) и зная концентрацию стандартного раствора Сст, рассчитывают неизвестную концентрацию исследуемого раствора:
Cx=Cст Lст/Lx
Уравнивание в колориметрах погружения. Опре-1 деление основано на визуальном уравнивании светопоглощения] стандартного и исследуемого окрашенных растворов путем измене- ] ния толщины поглощающего слоя. Неизвестная концентрация рас-1 твора рассчитывается, как и в предыдущем способе.
Визуальное определение концентрации раствора при помощи универсального фотометра ФМ-56 принципиально ничем не отли-j чается от методов определения концентрации, применяемых в фо- j токолор и метрическом анализе.
ФОТОКОЛОРИМЕТРИЯ И СПЕКТРОФОТОМЕТРИЯ j
Метод сравнения. Измеряют оптические плотности исследуемо-1 го Dx и стандартного DCT окрашенных растворов при одной и той! же толщине поглощающего слоя (/х = /ст). Применяя основной за-] кон светопоглощения к сравниваемым растворам, имеем: Dx = еСх/| и DCt = eCcrl. Решая эти уравнения относительно неизвестной! концентрации Сх, получают расчетную формулу:
Cx=Cст Dx/Dст
Метод калибровочного графика. Измеряют оптические плот-*ж ности стандартных растворов с известной концентрацией. По полу-j ченным данным строят калибровочный график, откладывая на оси] ординат значения оптической плотности, а на оси абсцисс — соот-1 ветствующие им значения концентрации. Затем измеряют оптиче-1 скую плотность исследуемых растворов и по графику находят их концентрации. Этот метод наиболее удобен для выполнения серийных определений.
Метод добавок. Измеряют оптическую плотность Dx исследуемого раствора. Затем к нему добавляют известное количество
определяемого вещества и снова измеряют оптическую плотность Озс+а. Неизвестную концентрацию определяемого вещества находят путем сравнения оптической плотности исследуемого раствора и раствора с добавкой. Применяя основной закон светопоглощения к сравниваемым растворам, получают уравнения:
Dх=eLCx Dx+a=eL(Cx+Ca)
Решением этих уравнений относительно неизвестной концентрации Сх получают расчетную формулу для метода добавок
Cx=Ca Dx/ Dx+a --Dx
где Са — концентрация добавки в фотометрируемом растворе.
Метод добавок создает одинаковые условия при фотометриро-вании исследуемого и стандартного растворов и позволяет уменьшить влияние примеси на результаты анализа.
Дифференциальный метод [4, 27—28]. Сущность метода состоит
в том, что оптические плотности исследуемого и стандартного окра-
шенных растворов измеряют не по отношению к чистому раствори-
телю с нулевым поглощением, а по отношению к окрашенному
раствору определяемого элемента с концентрацией Со («нулевой»
раствор), близкой к концентрации исследуемого раствора. Неиз-
вестную концентрацию Сх находят либо по калибровочному гра-
фику «относительная оптическая плотность — концентрация», либо
расчетным путем по методу сравнения
Сх=С0+FD’x
где F — фактор пересчета (рассчитывается по нескольким стандартным растворам), определяемый по формуле:
F=Cст-С0/ D’ст=дельтаС/ D’ст
| СТ |
D'x и Dct— относительная оптическая плотность исследуемого и стандартных растворов; ССт — концентрация стандартных растворов.
Дифференциальный метод применяют для повышения точности анализа при определении больших количеств веществ, а также дляижтр анения мешающего влияния посторонних компонентов и
исключения поглощения реактивa: эТОТ метод, в отличие от другихх, можно использовать еще и в случаях, когда из-за большой концeнтрации растворенного вещества нарушается ОСНОВНОЙ закон светопоглощения, a также, если значения оптических плoтнocтeй ВЫХОДЯТ за пределы шкалы прибора, a разбавление анализируемого раствора нежелательно.. Дифференциальный метод может иметь несколько вариантов: когда Со <Сх и _Со > С двусторонне дифференцирование и дифференциальный метод добавок. Этот метод используется для определения основных компонентов в растворах солей, сплавах и других объектах.
АНАЛИЗ C ПРИМЕНЕНИЕМ ОКРАШЕННОГО РЕАКТИВА. Если в исследуемом растворе присутствует окрашенная при-месь или для анализа используется окрашенный реактив, оптиче-скую плотность исследуемого раствор измеряют отггоснтельгга раствора холостой пробы, содержащего те же количества окрашен-ном примеси или реактива, либо производят последовательное измерение оптических плотностей исследуемого раствора и раствора холостой пробы относительно чистого растворителя (дистиллиро-ванной воды). B последнем случае неизвестное содержание анали-зируемого вещества определяют одним из методов по найденному значению разнoсти оптических плотностей исследуемого раствора и холостой пробы.
ЭКСТРАКЦИОННО-ФОТОМЕТРИЧЕСКИИ МЕТОД Экстракцггонно-фотометрический метод основан па сочетании экстракции продукта реакции анализируемого вещества c его по- следующим фотометрическим определением. Этот метод применяют при анализе сложных смесей, если определяют малые количества одних веществ в присутствии больших количеств других, при опре-делении примесей в присутствии основных компонентов, или когда непосредственное определение исследуемого элемента в смеси связaно c большими трудностями. при экстракигггг малых количеств примесей происходит не только их выделение, но и концентрирование.ПоэтоМу экстpaкционно-фотометрическггй метод прггобретает и. особо важное значение при определении малых количеств примесей в вешествах вы сокой степени чистоты, широко применяемых в атомной и полупроводниковой технике.
 2014-02-24
2014-02-24 598
598






