Большинство металлов содержится в природе в виде их оксидов или сульфидов, которые в результате обжига превращаются в оксиды. Металлургический процесс извлечения металлов из руд заключается в восстановлении их оксидов. В качестве восстановителей используют углерод, СО2, водород или металл.
В промышленности получение металлов из их оксидов восстановлением водородом находит применение в бездоменных процессах или для получения тугоплавких металлов. Применение водорода как в промышленности, так и в лаборатории сопряжено с большими трудностями, т.к. он образует с воздухом взрывоопасную смесь.
Цель работы: получить металл при восстановлении его оксида водородом и определить его практический выход.
Реактивы: цинк, соляная кислота (1:1), концентрированная серная кислота, порошки оксидов меди (II), железа (II), Pb, Sn.
Оборудование: аппарат Киппа, промывная склянка, осушительная колонка, кварцевая трубка, кварцевая лодочка, муфельная трубчатая печь.
Порядок выполнения работы: собирают установку по схеме на рисунке 3.
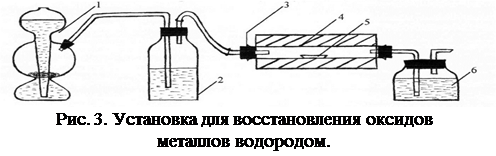
1 – аппарат Киппа; 2 – промывная склянка с концентрированной серной кислотой; 3 – кварцевая трубка;
4 – муфельная трубчатая печь; 5 – лодочка с оксидом металла; 6 – промывная склянка
Выполнение этой работы требует особых мер предосторожности:
1) установку продуть газом-восстановителем до полного вытеснения воздуха и проверить газ на чистоту. Категорически запрещается проводить эти операции при повышенной температуре;
2) после окончания работы, водород подавать до ее охлаждения.
Оксид металла восстанавливается в кварцевой лодочке, помещенной в кварцевую трубку диаметром 15 мм, которая расположена в трубчатой электропечи, температура в которой регулируется автоматическим терморегулятором.
Водород получают электролизом или в аппарате Киппа. Прибор подсоединяют к аппарату Киппа через промывную склянку с концентрированной серной кислотой. Навеску оксида металла массой 1,5-2 г, взвешенную с точностью до 0,01 г, насыпают в кварцевую лодочку и помещают ее посредине кварцевой трубки. Закрывают трубку и начинают пропускать в течение 10-15 минут водород для вытеснения воздуха из системы. Проверяют газ на чистоту и установку на герметичность, надевая на выход промывной склянки резиновую трубку с зажимом. При полной герметичности прибора ток кислорода вскоре должен прекратиться.
Если весь воздух вытеснен, то электропечь включают и нагревают трубку в токе водорода, пропуская его со скоростью 1-2 пузырька в секунду. Появление влаги в газоотводной трубке, а также уменьшение или полное прекращение прохождения пузырьков водорода через промывную склянку на выходе из установки показывает, что реакция началась. Об окончании реакции можно судить о приблизительно одинаковом количестве пузырьков водорода, проходящих через промывные склянки до реактора и после него.
После окончания реакции печь отключают и отодвигают, а водород продолжают пропускать через установку до ее полного охлаждения. Если водород отсоединить при нагретом реакторе, то воздух с оставшимся в реакторе водородом образует взрывоопасную смесь, а восстановленный металл с кислородом воздуха - оксид металла. После полного охлаждения установки отсоединяют газоподводящую трубку и вынимают лодочку с металлом.
Оформление результатов работы.
1. Напишите уравнение реакции восстановления оксида металла.
2. Приведите необходимые расчеты.
3. Результаты работы оформите в виде таблицы.
| Оксид металла | m, г | Восстановленный металл | m, г | Выход, % |
Вопросы семинара по теме: "Получение металлов"
1. Сырье металлургической промышленности: руды, кокс, флюсы.
2. Подготовка сырья к доменной плавке.
3. Методы получения металлов из руд.
4. Теоретические основы доменного процесса.
5. Устройство домны и каупера.
6. Методы преобразования чугуна в сталь: мартеновский и конверторные способы.
7. Кислородно-конверторный способ выплавки стали и получение стали в электропечах.
8. Производство алюминия электрохимическим способом.
Лабораторная работа № 7
 2015-03-08
2015-03-08 1412
1412
