Растворы – гомогенные многокомпонентные системы, состав которых может меняться в некоторых пределах без скачкообразного изменения свойств.
Компоненты растворов – простейшие составные части (молекулы, атомы, ионы). Размер частиц менее .10-9 м (< 1 нм). Если размеры больше - дисперсные системы.
В зависимости от агрегатного состояния:
Твердые: замещения, внедрения (Au-Cu, H2-Pd)
Газообразные или газовые смеси (воздух - О2, N2, СО2, пары Н2О)
Жидкие: «ж -т» (Н2О – NaCl, С2Н5ОН - сахар)
«ж -ж» (Н2О -С2Н5ОН, Н2О -Н2SО4)
«ж -г» (Н2О-СО2, Н2О- НCl ).
Компоненты растворов: растворитель и растворенное вещество.
Растворитель - обычно компонент раствора, который не меняет своего фазового состояния при образовании раствора и концентрация которого выше, чем у других компонентов.
По способности проводить электрический ток:
· Растворы электролитов - проводят
· Растворы неэлектролитов - не проводят.
Концентрация и растворимость -основные характеристики растворов.
Концентрация – содержание компонента раствора в единице объема или массы раствора или растворителя
|
|
|
Способы выражения концентрации растворов.
1. Молярная концентрация, С -количество растворенного вещества в единице объема этого раствора
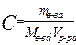 , [моль/л, моль/м3]
, [моль/л, моль/м3]
2. Молярная концентрация эквивалента, Сэк -количество молей эквивалента растворенного вещества в единице объема этого раствора
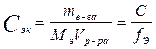 , [моль экв/л, моль экв/м3], где fэ - фактор эквивалентности
, [моль экв/л, моль экв/м3], где fэ - фактор эквивалентности
Задача 1:
Вычислите молярную концентрацию эквивалентов Н2SО4, если молярная концентрация Н2SО4 в растворе С = 2 моль/л
 2015-05-26
2015-05-26 952
952







