Клинические проявления зависят от быстроты развития обструкции и распространённости процесса в печёночных венах. Возможна различная выраженность синдрома — от злокачественного течения, при котором заболевание проявляется энцефалопатией и ведёт к гибели больного в течение 2-3 нед, до хронического, медленно прогрессирующего процесса в паренхиме печени, сходного с другими формами цирроза.
В большинстве случаев острого течения синдрома отмечается тяжёлое общее состояние больного и, как правило, наличие у него сопутствующего заболевания, например рака почки или печени, мигрирующего тромбофлебита или эритремии. Первыми проявлениями синдрома служат боли в животе, рвота, увеличение печени, асцит и умеренно выраженная желтуха. В терминальной стадии может возникать водянистый понос вследствие тромбоза брыжеечных вен. У больных с тотальной окклюзией печёночных вен развивается делирий, переходящий в кому, и в течение нескольких дней наступает смерть.
Хроническое течение встречается чаще. У больных отмечаются боли в области печени, которая увеличена, болезненна. В течение 1—6 мес развивается асцит. При отсутствии обширного некроза зоны 3 печёночной дольки желтухи не наблюдается или она слабо выражена. При надавливании на печень яремные вены могут не набухать (отрицательный гепатоюгулярный рефлюкс). По мере развития портальной гипертензии начинает пальпироваться селезёнка. При пальпации в эпигастральной области можно обнаружить увеличенную хвостатую долю печени, которую иногда принимают за опухоль.
Возможно бессимптомное течение, при котором у больных печень не увеличена, отсутствуют асцит и боли в животе [19]. Нарушение венозного оттока от печени обнаруживают случайно, с помощью методов визуализации или при обследовании больных с изменёнными лабораторными показателями функции печени. Отсутствие симптомов может объясняться проходимостью одной из крупных печёночных вен или наличием хорошо развитой системы венозных коллатералей.
При обструкции нижней полой вены появляются выраженные отёки ног, расширение вен передней и боковых поверхностей живота и спины, а также альбуминурия.
В течение нескольких месяцев развиваются асцит и истощение больного.
Биохимическое исследование. Уровень билирубина в сыворотке, как правило, не превышает 34 мкмоль/л (2 мг%). Возрастает активность ЩФ сыворотки, снижается уровень альбумина. Повышается активность печёночных трансаминаз, значительный её рост характерен для сопутствующей обструкции воротной вены. Выраженное увеличение протромбинового времени особенно часто встречается при остром течении синдрома. Гипопротеинемия может быть следствием экссудативной энтеропатии.
Теоретически асцитическая жидкость должна содержать большое количество белка. В действительности так бывает не всегда.
Необходима пункционная биопсия печени. Зона 3 имеет пятнистый вид и отличается от бледной портальной зоны. При гистологическом исследовании обнаруживается картина застоя в зоне 3 (см. рис. 11-9 и 11-10). Следует обратить внимание на признаки алкогольного гепатита или флебита печёночных вен.
Проведение печёночной венографии не всегда возможно, однако она позволяет увидеть узкие, непроходимые печёночные вены. Рядом с ними определяются вены с извилистым, «кружевным» рисунком, похожим на паутину (рис. 11-11) [9], возможно представляющие собой аномальные венозные коллатерали. Продвижение катетера по печёночной вене на обычное расстояние невозможно, точка его заклинивания отстоит от диафрагмы на 2—12 см.
Для определения проходимости нижней полой вены прибегают к нижней кавографии. При этом катетер проводят сверху, через правое предсердие, или снизу, через бедренную вену, иногда используют сочетание обоих путей. Можно выявить боковое сужение печёночного сегмента нижней полой вены вследствие сдавления увеличенной хвостатой долей (рис. 11-12). Измеряют давление на всем протяжении нижней полой вены, чтобы подтвердить её проходимость и установить выраженность обструкции, обусловленной мембранами в её просвете или увеличением хвостатой доли.
Селективная целиакография. Печёночная артерия имеет небольшие размеры, калибр её ветвей уменьшен, они удлинены и смещены, создаётся впечатление о наличии множественных объёмных образований. Сходная картина отмечается при метастазах [21]. Опорожнение портальных сосудов в венозной фазе замедлено.
УЗИ представляет собой оптимальный метод неотложной диагностики. Он позволяет выявить изменения печёночных вен, гипертрофию хвостатой доли, повышенную эхогенность и сдавление нижней полой вены. Ткань печени гипоэхогенна в раннем периоде острого тромбоза и гиперэхогенна при наличии фиброза в отдаленном периоде. Метод используют для диагностики асцита.
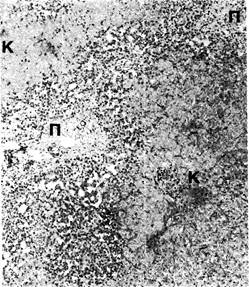
Рис. 11-9. Синдром Бадда—Киари. При гистологическом исследовании отчётливо определяется кровоизлияние в зоне 3 печёночной дольки (К). Гепатоциты вблизи портальных трактов (П) не изменены. Окраска гематоксилином и эозином, х100.
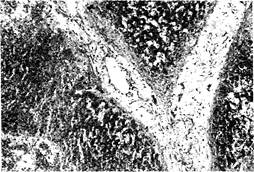
Рис. 11-10. Синдром Бадда—Киари. На продольном срезе через печёночную венулу определяются фиброзирование её просвета, утолщение стенки и уменьшение количества гепатоцитов вокруг сосуда. Окраска хромофобным анилиновым синим. См. также цветную иллюстрацию на с. 772.
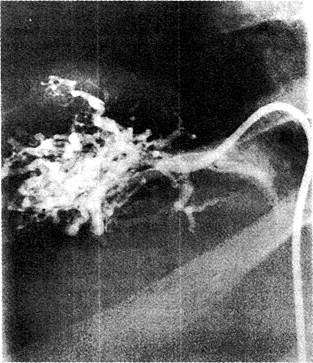
Рис. 11-11. На печёночной венограмме при синдроме Бадда—Киари виден «кружевной», похожий на паутину сосудистый рисунок.
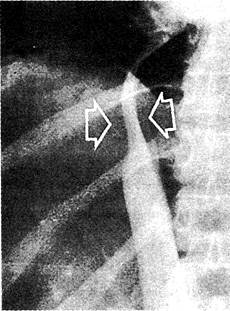
Рис. 11-12. Нижняя кавография. На снимках, сделанных в переднезадней проекции, определяется суженная с боков и изогнутая нижняя полая вена (указана стрелками). Давление слева обусловлено увеличенной хвостатой долей печени [42].
С помощью импульсного допплеровского УЗИ выявляют изменение направления кровотока по печёночным венам и печёночному сегменту нижней полой вены. Кровоток в нижней полой и печёночных венах может отсутствовать, становиться обратным, быть турбулентным или непрерывным. Цветное допплеровское картирование позволяет обнаружить нарушения тока крови по печёночным, воротной и нижней полой венам; его результаты соответствуют данным венографии [29].
В дифференциальной диагностике синдрома Бадда—Киари с циррозом печени важную роль играет обнаружение внутрипеченочных коллатеральных сосудов. Метод также имеет значение при неудовлетворительной визуализации печёночных вен с помощью УЗИ [29].
На компьютерных томограммах печень увеличена, диффузно пониженной плотности, после введения контрастного вещества отмечается пятнистый характер его распределения. Неоднородность контрастирования печёночной паренхимы связана с очаговыми различиями в портальном кровотоке [48]. После введения контрастного вещества в участках с полной обструкцией печёночной вены сохраняется низкая плотность ткани, вероятно, из-за инверсии портального кровотока. При этом возможно контрастирование субкапсулярных областей.
На компьютерных томограммах без контрастирования плотность хвостатой доли повышена по сравнению с окружающей паренхимой с низким кровоснабжением (рис. 11-13).
Дефект наполнения в просвете сосуда, сохраняющийся после контрастирования, может указывать на тромбы в нижней полой или печёночных венах [30].
Сходство компьютерных томограмм при синдроме Бадда—Киари и метастазах печени служит источником диагностических ошибок.
МРТ позволяет обнаружить нарушение венозного оттока в нижнюю полую вену, коллатеральные вены печени и сдавление нижней полой вены увеличенной хвостатой долей. Интенсивность сигнала от паренхимы печени изменяется (рис. 11-14) [17].
 2015-06-10
2015-06-10 434
434








