ГЛАВА 1.1. СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О ПРИРОДЕ И СТРОЕНИИ ТВЕРДЫХ И ЖИДКИХ МЕТАЛЛОВ И СПЛАВОВ
В зависимости от давления и температуры любое вещество может находиться в твердом, жидком, газообразном состояниях, а также в состоянии плазмы. Диаграмма состояния однокомпонентного вещества приведена на рис. 1.1. Линии АД и АД' на диаграмме разделяют
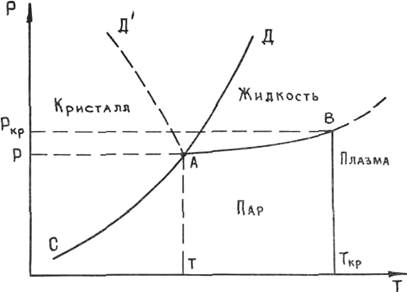
Рис. 1.1. Диаграмма состояния однокомпонентной системы
области кристаллического состояния и жидкости. Линия АД относится к веществам, удельный объем которых при плавлении увеличивается (большинство веществ), а линия АД' — к воде, галлию, висмуту, сурьме, германию и кремнию, удельный объем которых при плавлении уменьшается. Из диаграммы видно, что с увеличением давления температура плавления этих веществ уменьшается. Температура плавления большинства веществ с ростом давления увеличивается. Следует отметить, что линии АД и АД' представляют собой линии равновесия кристалл — жидкость, т. е. геометрическое место точек, отвечающих значениям параметров (давление Р и температура Т), при которых кристалл и жидкость находятся в динамическом равновесии друг с другом. В этом случае граница раздела твердой и жидкой фаз является плоской. При искривлении поверхности раздела характер зависимости температуры плавления остается таким же, но линии смещаются влево или вправо в зависимости от того, выпуклое или вогнутое твердое тело.
Температура плавления выпуклых кристаллов (сферических частиц) меньше, чем плоских, а температура плавления вогнутых кристаллов (включения металла в различных неметаллических частицах) выше, чем плоских. Связь температуры плавления кристаллов с их радиусом кривизны и температурой плавления плоских кристаллов Травн, которую будем называть равновесной, выражается следующей формулой:
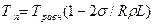 , (1.1)
, (1.1)
где а — коэффициент межфазного натяжения кристалла на границе с жидкостью; R — радиус кривизны кристалла и L — удельная теплота плавления. В формуле радиус кривизны выпуклого кристалла положительный, а вогнутого — отрицательный. Из формулы видно, что для плоского кристалла (R = ∞) Тп = Травн, с уменьшением радиуса кривизны температура плавления выпуклого кристалла уменьшается, а вогнутого — увеличивается.
Формула (1.1) написана для кристаллов, ограниченных сферической поверхностью. При произвольной конфигурации поверхности формула имеет вид
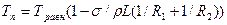 , (1.2)
, (1.2)
где R1 и R2 — главные (наибольший и наименьший) радиусы кривизны поверхности. Следует отметить, что изменения температуры плавления становятся существенными лишь при радиусах поверхностей кристаллов, меньших 0,001 мм.
Линия АВ является линией равновесия жидкости и пара. Для каждого значения температуры в пределах от Т до Ткр по линии АВ мы можем найти давление насыщенного пара жидкости. Точка В отвечает критическому состоянию (точка абсолютного кипения), при котором исчезает различие между жидким и газообразным состояниями вещества. При температуре выше Ткр газ невозможно перевести в жидкость ни при каких давлениях. При атмосферном давлении ширина области жидкого состояния (между линиями АД и АВ) для многих металлов достаточно велика и значительно превышает применяемые в практике литья перегревы металла выше его температуры плавления. Например, температура плавления (Тп) алюминия — 660°С, а температура кипения (Ткип) — 2327°С; для меди Тп = 1083°С, Ткип = 2596°С; для железа Тп = 15Зб0С, Tки п = 2 880°С. Для этих металлов испарение в условиях литейных процессов не играет большой роли. В то же время для цинка Тп = 419,5°С, Ткип = 906°С; для магния Тп = 651°С, Ткип = 1 107°С. Для этих металлов температура кипения близка к температуре плавления. Они отличаются, как говорят, большой летучестью. Поэтому при их наличии в сплавах необходимо учитывать процессы парообразования.
При температурах, значительно превышающих Ткр, происходит ионизация газов и они переходят в состояние плазмы, представляющей собой совокупность ионов и электронов.
Как видно из диаграммы, жидкое состояние вещества занимает промежуточное место между твердым и газообразным состояниями. Поэтому жидкости сохраняют отдельные свойства как твердых, так и газообразных тел. Твердые тела по характеру расположения и движения атомов и молекул подразделяются на кристаллические и аморфные.
1.1.1. ПРИРОДА И СТРОЕНИЕ ТВЕРДЫХ МЕТАЛЛОВ И СПЛАВОВ
Основным свойством кристаллического состояния вещества является правильное, упорядоченное расположение атомов в пространстве. Кристаллическое состояние вещества характеризуется четкой пространственной структурой, называемой кристаллической решеткой.
О. Браве установил, что любой кристалл можно построить на основе 14 элементарных ячеек. Наиболее распространенными ячейками металлических кристаллов являются кубическая объемно центрированная (ОЦК), кубическая гранецентрированная (ГЦК), компактная гексагональная (рис. 1.2). Предполагается, что в идеальном кристалле атомы расположены строго в узлах решетки и неподвижны. Кроме того, считается, что решетка является бесконечно протяженной, т. е. каждая элементарная ячейка окружена достаточным количеством других ячеек (далека от поверхностей реальных тел).
Важнейшей характеристикой кристаллической решетки является координационное число, т. е. число ближайших соседей данного атома. С помощью элементарных геометрических расчетов можно определить, что в объемно центрированной кубической решетке координационное число — 8, т. е. около каждого атома в решетке находится 8 атомов, расположенных на минимальном расстоянии r1 = а 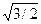 , где а — параметр решетки. На расстоянии r2, равном а, находится 6 атомов, и на расстоянии r4 = а
, где а — параметр решетки. На расстоянии r2, равном а, находится 6 атомов, и на расстоянии r4 = а 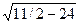 атома. Расположение атомов в решетке дискретно, так как они находятся лишь на определенных расстояниях от данного атома, называемых радиусами координационных сфер. Таким образом, в объемно центрированной кубической решетке на первой координационной сфере с r1 = а
атома. Расположение атомов в решетке дискретно, так как они находятся лишь на определенных расстояниях от данного атома, называемых радиусами координационных сфер. Таким образом, в объемно центрированной кубической решетке на первой координационной сфере с r1 = а 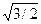 , находится 8 атомов, на второй с r2 = а — 6 атомов, на четвертой с r4 = а
, находится 8 атомов, на второй с r2 = а — 6 атомов, на четвертой с r4 = а 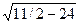 и т. д. Между сферами атомов нет.
и т. д. Между сферами атомов нет.
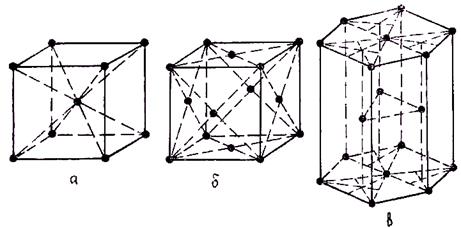
Рис. 1.2. Распространенные типы кристаллических решеток металлов и сплавов:
а — объемно центрированная; б — гранецентрированная; в — компактная гексагональная.
Для гранецентрированной кубической решетки легко установить, что на первой координационной сфере с r1 = а 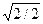 находится 12 атомов, на второй с r2 = a — 6 атомов, на третьей с r3 = а
находится 12 атомов, на второй с r2 = a — 6 атомов, на третьей с r3 = а 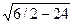 атома и т. д.
атома и т. д.
Приняв в идеальном приближении, что кристалл плотно упакован и соседние атомы касаются друг друга, можно радиус первой сферы принять равным 2R, где R — атомный радиус. С учетом этого получаем, что для объемно центрированного куба r1 = 2R, r2 = 4R 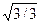 , r4 = 2R
, r4 = 2R 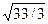 , а для гранецентрированного куба r1 = 2R, r2 = 2R
, а для гранецентрированного куба r1 = 2R, r2 = 2R 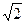 , r3 = 2R
, r3 = 2R 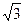 и r4 = 4R.
и r4 = 4R.
С учетом полученных значений радиусов координационных сфер и числа находящихся на них атомов можно построить графики пространственного расположения атомов в объемно центрированной и гранецентрированной кубических решетках (рис. 1.3).
Такова в общих чертах характеристика идеального кристалла. Реальный кристалл имеет целый ряд существенных особенностей. Прежде всего, атомы не находятся неподвижно в узлах решетки, а их атомные диаметры не совпадают с радиусом первой координационной сферы.
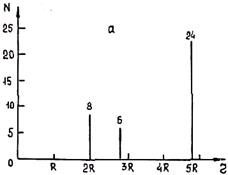
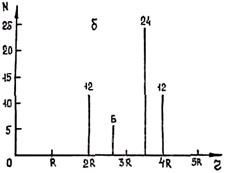
Рис. 1.3. Распределение числа атомов по первым координационным сферам для
объемно центрированного (а) и гранецентрированного (б) куба.
Известно, что атомы совершают колебания относительно узлов решетки, которые являются положениями равновесия. Интенсивность колебаний, или теплового движения атомов, увеличивается с ростом температуры. При низких температурах атомы совершают колебания относительно фиксированных узлов, т. е. так называемое трансляционное движение отсутствует и атомы не перемещаются поступательно по решетке. Однако с увеличением температуры вероятность появления трансляционного поступательного движения атомов увеличивается. Для того чтобы охарактеризовать механику реального кристалла, рассмотрим вопрос о межчастичном взаимодействии в кристаллах.
Как известно, атомы металлов, как и других элементов, представляют собой положительные ядра с вращающимися относительно них электронами, обладающими разными энергиями (находящимися на разных энергетических уровнях). При сближении любых двух атомов, начиная с некоторого расстояния, их электронные оболочки перекрываются (речь идет о внешних оболочках), подобно тому как при образовании молекулы водорода электроны каждого атома попадают в сферу влияния ядер обоих атомов и обобществляются, т. е. процесс сближения атомов металла приводит к обобществлению части их электронов. В пределах кристаллической решетки эти электроны уже не принадлежат только своим атомам. В результате образуется система, в которой в узлах решетки находятся положительно заряженные ионные остовы, а в объеме решетки расположены свободные коллективизированные электроны. Именно наличием этих электронов объясняется высокая электропроводность металлов.
Рассмотрим процесс сближения атомов. Если расстояние между ними достаточно велико, то атомы можно представить как два диполя, которые притягиваются друг к другу. При этом заряды ближайших атомов обоих диполей вследствие электростатической индукции имеют разную полярность. Это явление, как известно из физики, называется поляризацией. Силы притяжения, возникающие вследствие поляризации, обратно пропорциональны расстоянию между атомами в седьмой степени (Fпр ~ 1/R7). Эти силы называются силами Ван-дер-Ваальса. Такая зависимость сил притяжения говорит о том, что они при увеличении расстояния между атомами быстро убывают (на расстоянии, в несколько раз превышающем размеры атомов, эти силы практически исчезают).
Если атомы сблизить на расстояние, сравнимое с размерами электронных орбит, например несколько меньшее диаметра этих орбит, то электронные оболочки начинают деформироваться и между атомами возникают силы отталкивания, называемые обменными силами. Силы отталкивания близкодействующие, они убывают с увеличением расстояния быстрее, чем силы притяжения. Известно эмпирическое приближение, что Fот ~ 1/R13. Простейшей и широко применяемой формулой для описания потенциала межчастичных взаимодействий является потенциал Ленарда — Джонса:
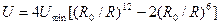 , (1.3)
, (1.3)
где R0 — расстояние, отвечающее минимуму потенциала; Umin — модуль минимума потенциала.
Формула Ленарда — Джонса моделирует изменение потенциала взаимодействия двух частиц. Рассмотрим две частицы, причем левую закрепим неподвижно. Изменение потенциала при изменении расстояния на dR равно работе сил взаимодействия, т. е.
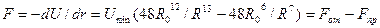 , (1.4)
, (1.4)
где 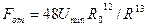 и
и 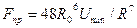
Графически изменение результирующей силы взаимодействия и энергии связи частиц с изменением расстояния показано' на рис. 1.4. Видно, что при R = R0 F = 0, т. е. |Fпр| = |Fот|. Положению равновесия отвечает минимум энергии связи, т. е. потенциальная яма. Если бы не было теплового движения атомов, то! атомы в кристаллической решетке располагались бы на расстоянии Ro друг от друга, которое физически определяет параметр решетки.
Отмеченные выше закономерности имеют общий характер. В чем же специфика металлов? Обменные силы отталкивания зависят от степени заполнения внешней электронной оболочки. С ее увеличением силы отталкивания возрастают. Как известно, наибольшую заполненность внешней оболочки имеют инертные газы (гелий, аргон, криптон и т. д.). На внешних оболочках у них максимально возможное число электронов — 8. При сближении атомов оболочки практически не перекрываются и не происходит образование обобщенных электронов и ионов. Поэтому инертные газы — диэлектрики.
Рассмотрим случай, когда внешние электронные оболочки не заполнены электронами (число внешних электронов меньше 8). Здесь возможно большее сближение атомов и перекрытие электронных оболочек с образованием ионов и коллективизированных электронов. Свободные электроны оказывают влияние на силы притяжения. Электроны, находящиеся между двумя положительными ионами, притягивают их с силой, большей силы притяжения ионов, так как расстояние между каждым ионом и электронами меньше, чем расстояние между ионами. При этом всякое изменение параметра решетки вызывает изменение плотности электронов между ионами, что, в свою очередь, приводит к возникновению сил, стремящихся вернуть решетку в исходное состояние. Такой тип связи называется металлическим. Силы отталкивания теперь связаны с деформацией внутренней заполненной электронной оболочки иона, имеющей радиус R2 < R1, где R1 — радиус внешней оболочки, электроны которой коллективизированы. Равновесие ионов достигается на расстоянии R0, находящемся в интервале 2R1 — 2R2.
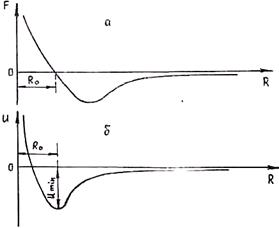
Рис. 1.4. Зависимость силы (а) и потенциала взаимодействия (б) двух атомов от расстояния между ними.
Металлические чистые кристаллы очень устойчивы по отношению к сильным смещениям частиц. Если металл растянуть, то увеличится вероятность нахождения электронов между ионами (электронная плотность) и появятся силы, стремящиеся вернуть решетку в исходное состояние. Если металл сжать, то электроны вытесняются из межионного пространства, электронная плотность падает и силы отталкивания начинают превышать силы притяжения. При снятии внешнего воздействия решетка вернется в исходное состояние. Поэтому чистые металлы способны без разрушения выдерживать большие пластические деформации. Хрупкость отдельных металлов и сплавов объясняется наличием в решетке различных кристаллических дефектов (вакансии, дислокации и т. п.).
Электроны оказывают существенное влияние на свойства металлов. Однако более детальное рассмотрение электронной теории металлов выходит за рамки данного курса. Интересующимся можно рекомендовать книгу Н. Б. Брандта, С. М. Чудинова «Электронная структура металлов» (М.: Изд-во Моск. ун-та, 1973. 332 с.).
До сих пор мы рассматривали кристалл в условиях, когда кинетическая энергия частиц равна нулю, т. е. частицы неподвижно находятся в положениях равновесия (параметр решетки равен R0) • Однако это невозможно даже при абсолютном нуле. Как и в любом теле, частицы в твердом металле обладают кинетической энергией Е, которая связана с температурой. В первом приближении можно принять, что E = kT, т. е. с ростом температуры Е увеличивается. Если под действием теплового движения положение равновесия нарушится и расстояние между частицами увеличится, то силы притяжения превзойдут силы отталкивания и появится сила, возвращающая частицы в положение равновесия. При уменьшении расстояния между частицами силы отталкивания превзойдут силы притяжения и возвращающая сила снова будет направлена к положению равновесия. Таким образом, возникает ситуация, характерная для колебательного движения. Однако колебания частиц в данном случае будут ангармоническими.
Для возникновения гармонических колебаний необходимо, что бы возвращающая сила была пропорциональна отклонению от положения равновесия. В этом случае кривая энергии связи симметрична (рис. 1.5). Пусть при температуре Т1 энергия теплового движения Е1, а при температуре Т2 > Т1 энергия теплового движения Е2 > Е1. Видно, что частица совершает симметричные колебания, причем с ростом температуры амплитуда колебаний увеличивается. Положение же равновесия при этом не изменяется.
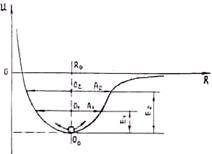
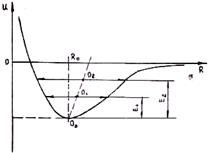
Рис. 1.5. Зависимость потенциала взаимодей- Рис. 1.6. Изменение параметра кристаллической
ствия частиц от расстояния между ними при решётки при нагревании
гармоническом характере колебаний
В кристаллах же возвращающая сила, как видно из формулы (1.4), не пропорциональна отклонению от положения равновесия (R — в знаменателе). С ростом расстояния силы отталкивания убывают быстрее, чем силы притяжения. Поэтому кривая энергии связи несимметрична (рис. 1.6). С увеличением температуры, а следовательно, и энергии теплового движения возрастает амплитуда колебаний, но положение равновесия смещается в сторону увеличения расстояния между частицами. Это приводит к увеличению параметра решетки, т. е. к тепловому расширению. Таким образом, термическое расширение тел объясняется не ростом амплитуды тепловых колебаний частиц, а ангармоническим характером этих колебаний.
Мы рассмотрели характер движения частиц в упрощенном случае двухчастичного линейного кристалла. В действительности в пространственной решетке колебания носят сложный характер. Каждая частица испытывает действие сил связи со стороны всех окружающих ее частиц кристалла. Так как силы связи быстро убывают с увеличением расстояния, то учитывают действие только ближайших «соседей». Если изменить характер движения какой-либо одной частицы, то это изменение будет передано соседним частицам, а от них — к их «соседям» и т. д. Например, если тело с одной стороны нагреть, то колебания частиц в этой части кристалла усилятся. Это усиление теплового движения через силы связи передастся соседним частицам и достигнет противоположного конца тела, т. е. повышение температуры в какой-либо части тела приведет к ее повышению в остальных. Такова природа теплопроводности.
Следует отметить, что при этом не происходит направленного перемещения частиц. Они колеблются около своих положений равновесия. В кристалле разные частицы колеблются с разными частотами и в разных фазах. Период колебаний частиц имеет порядок 10-13 с. Таким образом, если мы «сфотографируем» частицы в кристалле с временем экспозиции, меньшим 10-13 с, то никакого порядка в расположении частиц не увидим, так как все они будут находиться на разных расстояниях от положений равновесия. Реально же время экспозиции всегда больше 10-13 с. Поэтому фактически мы увидим частицы в положениях равновесия, т. е. упорядоченную структуру кристалла.
В кристалле энергия теплового движения меньше энергии связи, т. е. E < |Umin|. С увеличением температуры растет энергия теплового движения, и при некоторой температуре она приблизится к энергии связи. При этом произойдет плавление кристалла» т. е. переход в жидкое состояние. Для иллюстрации поведения частиц в кристалле при нагревании рассмотрим изменение энергии связи двух частиц в зависимости от положения между ними средней частицы. Если расстояние между частицами достаточно мало (температура значительно меньше температуры плавления), то энергия средней частицы распределена в соответствии с рис. 1.7, а. При этом средняя частица имеет минимум энергии посредине между крайними частицами, что отвечает правильному расположению частиц в кристалле. Если же крайние частицы раздвинуть на очень большое расстояние, что соответствует испарению металла, то средним положениям частицы будет соответствовать отсутствие сил взаимодействия. Кривая энергии средней частицы при этом показана на рис. 1.7,б. Видно, что на значительных расстояниях между частицами средняя частица не будет испытывать взаимодействия с крайними, как в идеальном газе.
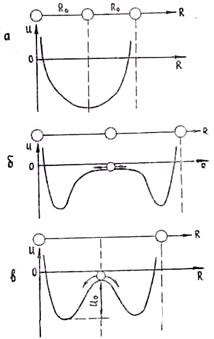
Рис. 1.7. Изменение потенциала средней частицы при малых (а), очень больших (б) и некоторых средних (в) расстояниях между крайними атомами
Рассмотрим случай, когда температура близка к температуре плавления. Крайние частицы находятся на таком расстоянии друг от друга, что энергия связи средней частицы будет изменяться в зависимости от расстояния, как показано на рис. 1.7, в. Положение в центре промежутка между крайними частицами будет неустойчивым и частица перейдет в потенциальную яму около левой или правой частицы. При этом кристалл разрушится. Нарушится дальний порядок в размещении частиц. Частицы первой координационной сферы (ближайшие к данной частице) останутся связанными с этой частицей, а более удаленные потеряют с ней связь. Говорят, что сохранился ближний порядок в размещении атомов. Средняя частица при этом совершает колебания только около одной из указанных на рисунке частиц. Следует, однако, отметить, что данное положение будет динамическим. Глубина потенциальной ямы не столь велика, чтобы средний атом, накопив вследствие флуктуации энергию, не перешел в потенциальную яму около соседней, т. е. правой, частицы. При этом происходит смена положения равновесия колебаний. Описанная картина отвечает жидкому состоянию.
Таким образом, частицы в жидкостях совершают колебания такого же типа, что и в кристаллах, но положения равновесия, относительно которых совершаются колебания, не остаются неподвижными. Совершив некоторое число колебаний около данного положения равновесия, частица скачком переходит в новое положение и продолжает там колебаться, пока снова не перескочит в новое положение. По Я. И. Френкелю, длительность пребывания частицы около данного положения равновесия — время оседлой жизни — определяется по формуле т^т-ое^0^7', где t0 — период колебания около положения равновесия; U0 — высота потенциального барьера, отделяющего два положения равновесия (глубина потенциальной ямы); k — постоянная Больцмана; Т — абсолютная температура. Обычно t имеет порядок 10-10 с. Период же колебаний то имеет порядок 10-12 — 10-13 с. Значит, частица, прежде чем переменить место, совершит 100 — 1000 колебаний.
Молекулы жидкости в основном ведут оседлый образ жизни, что сближает их с молекулами твердых тел. С увеличением температуры время оседлой жизни уменьшается, т. е. снижается доля колебательного движения и увеличивается доля поступательного трансляционного движения. Таким образом, в жидкостях сохраняется на достаточно высоком уровне взаимодействие между частицами, сосуществующее с тепловым движением. Такое состояние в отличие от газов, где энергия взаимодействия значительно меньше энергии теплового движения, называется конденсированным состоянием. Отличие жидкости от твердых кристаллических тел состоит в наличии кроме колебательного движения трансляционного движения, доля которого увеличивается с повышением температуры. Однако для более полного понимания процесса плавления необходимо отметить, что и в твердых телах частицы могут иметь трансляционное движение, усиливающееся по мере приближения к температуре плавления.
Как известно из молекулярно-кинетической теории, среди частиц газа или жидкости, находящихся при данной температуре, можно найти частицы, обладающие разной кинетической энергией, в том числе и значительно отличающейся от соответствующего данной температуре среднего значения E = kT.
Однако кривая распределения числа частиц по энергиям имеет острый максимум при E = kT, т. е. относительное количество частиц, обладающих энергией, сильно отличающейся от E = kT, невелико. Например, количество частиц, имеющих энергию, в 2 раза большую этой величины, составляет всего 5%. Таким образом, в жидкости при данной температуре имеется определенное количество частиц, обладающих кинетической энергией, превышающей энергию
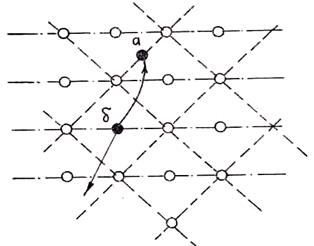
Рис. 1.8. Схема образования вакансий и дислоцированных атомов
связи частиц в кристалле. Вспомним, что именно наличием этих быстрых частиц в физике объясняют процесс испарения. Такая быстрая частица в кристалле преодолеет силы связи с «соседями» и покинет данную ячейку, переместившись в соседнюю. Там она займет место в узле, если оно свободно, или разместится в объеме узла (в междоузлии). Место этой частицы в прежней ячейке окажется вакантным. Говорят, что там образовалась вакансия (или дырка). Переместившийся атом, если он находится в междоузлии, называется дислоцированным. Схема образования дислоцированных атомов и вакансий показана на рис. 1.8.
Наличие вакансий в твердом теле создает условия для трансляционного поступательного движения частиц. Процесс перемещения частиц и вакансий в чистом металле называется самодиффузией. Для оценки числа вакансий Я. И. Френкелем предложена следующая формула: Nв=Ne-u/kт, где Nв — число вакансий; N — общее число частиц; U — энергия образования вакансии, близкая к энергии испарения. Я. И. Френкелем выполнен следующий расчет для кадмия. При комнатной температуре (300 К) вакансий мало, Nв/N = 10-18. Уже при температуре 600 К Nв/N = 10-9. Особенно быстро растет количество вакансий вблизи температуры ллавления (до 1,5 %).
Вакансии и дислоцированные атомы относятся к точечным дефектам кристаллической решетки, приводящим к ее искажению и созданию около дефектов напряженного состояния. Характер искажения решетки в плоском изображении показан на рис. 1.9.
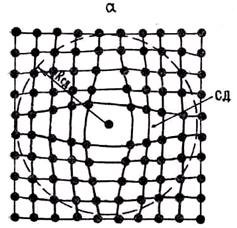
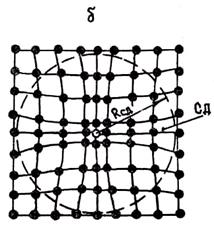
Рис. 1.9. Схема искажения кристаллической решетки около дислоцированного атома (а) и вакансии (б)
Установлено, что геометрия ионного остова и электрический потенциал решетки при этом искажаются на значительном расстоянии, равном 10 — 20 межатомным расстояниям от дефекта. Эту деформированную зону называют сферой деформации (СД). Сфера деформации около вакансии несет отрицательный заряд, так как положительный ион замещен вакансией (дыркой). Однако электрическое взаимодействие вакансий на расстояниях, превышающих радиус сферы деформации Rсд, весьма мало. Так как вакансии перемещаются по кристаллу, то перемещаются и сферы деформации. При сближении СД на расстояния l £ Rсд между ними возникают силы отталкивания.
1.1.2. СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О МЕХАНИЗМЕ ПЛАВЛЕНИЯ
В объяснении процесса плавления главную роль из рассмотренных дефектов решетки играют вакансии. На их роль впервые обратил внимание Я. И. Френкель. В литературе имеется целый ряд теорий, объясняющих плавление. На наш взгляд, очень убедительной выглядит вакансионно-кластерная теория И. В. Гаврилина и Г. С. Ершова.
При низких температурах в кристалле число вакансий невелико и расстояния между сферами деформации больше их диаметров. Поэтому СД не взаимодействуют друг с другом и подобно газовым частицам свободно, хаотически перемещаются по кристаллу (рис. 1.10, а). При некоторой температуре Т = Тк концентрация вакансий возрастает до величины, при которой расстояния между СД сравниваются с их диаметрами. При этом СД смыкаются, образуя плотную упаковку (рис. 1.10,6). Дальнейшее повышение температуры должно сопровождаться увеличением числа вакансий. Однако при T = Tк вследствие взаимного отталкивания СД места для размещения новых вакансий отсутствуют. Возникает противоречие между тенденцией сохранения дальнего порядка и тенденцией к росту числа вакансий.
Разрешение этого противоречия осуществляется путем потери дальнего порядка. Новые вакансии могут образовываться только лишь в пустотах плотной упаковки СД (рис. 1.10, б). Скопления и перемещения вакансий по границам СД приводят к тому, что решетка дробится на отдельные блоки, равные по размерам диаметру СД. Эти блоки называются кластерами. Таким образом, в пределах кластера сохраняется порядок в расположении атомов (ближний порядок), но за пределами кластера порядок нарушается (нет дальнего порядка).
Для дробления решетки на кластеры необходимо затратить энергию на разрыв связей кластеров друг с другом. Эта энергия и представляет собой теплоту плавления. Температура Гц, при которой смыкаются СД, равна температуре плавления. При плавлении происходит изменение объема, вызванное двумя следующими эффектами. Вследствие отталкивания друг от друга образовавшихся кластеров происходит увеличение объема. С другой стороны, так как при плавлении силы связи между кластерами резко уменьшаются, увеличивается их подвижность. До перехода в жидкое состояние зоны СД связаны между собой и сохраняют упаковку, характерную для кристалла. После плавления связи между кластерами разрушаются, они получают возможность смещаться относительно друг друга.
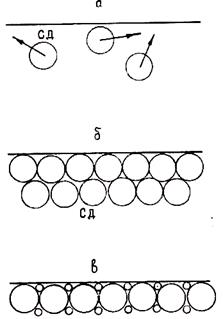
Рис. 1.10. Схема плавления по И. В. Гаврилину и Г. С. Ершову: а – Т<<Tпл; б – T» Тпл; в – Т = Тпл
Известно, что минимуму энергии отвечает более плотная упаковка (минимальная поверхность). Поэтому в жидкости кластеры принимают более плотную упаковку, чем та, которая была в кристалле. Благодаря этому эффекту объем жидкости должен быть меньше объема кристалла. Результирующее изменение объема при плавлении равно алгебраической сумме этих эффектов. Для большинства металлов превалирует первый эффект и объем при плавлении увеличивается примерно на 3%. Для таких аномальных веществ, как висмут, галлий, сурьма, кремний, превалирует эффект переупаковки кластеров и объем при плавлении уменьшается. Кластеры в жидкости находятся в сложном тепловом движении. При этом происходят процессы их воссоединения (восстановления связей) и последующего дробления, но уже по другим поверхностям разрыва.
Следует отметить, что теплота плавления значительно меньше теплоты испарения, а изменения объема невелики. Поэтому силы связи между частицами в жидкости остаются практически на том же уровне, что и в кристалле. Однако возрастает энергия теплового движения. Это позволяет считать, что при температурах, близких к температуре плавления, жидкости ближе к кристаллам, чем к газам.
В заключение необходимо отметить, что теория плавления в настоящее время еще не создана. Приведенная теория может рассматриваться как некоторое приближение.
1.1.3. МОДЕЛИ ЖИДКОГО СОСТОЯНИЯ
До сих пор не созданы такие эффективные модели жидкого состояния, какими являются модель идеального газа для газов и идеального кристалла для кристаллических тел. Все существующие модели жидкого состояния можно разделить на две большие группы: квазигазовые модели и квазикристаллические модели.
Общим для псевдогазовых моделей является игнорирование межчастичного притяжения. Взаимодействие частиц сводится только к их упругим столкновениям. Простейшей является модель «твердых шаров». Частицы жидкости уподобляются твердым взаимно непроникающим шарам. Потенциал их взаимодействия задается в следующем виде:
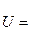 ^ f0, если г > 2R^, ~ [со, если г < 27?щ.
^ f0, если г > 2R^, ~ [со, если г < 27?щ.
Смысл формул сводится к тому, что частицы не взаимодействуют друг с другом, пока не столкнутся. При столкновении возникают упругие силы отталкивания. Радиус шаров принимают или равным радиусу первой координационной сферы кристалла, или на основании рентгенографического исследования жидкости (расстояние до первого максимума интенсивности рассеивания излучения). Так как под действием сил отталкивания при отсутствии притяжения частицы разлетятся, то вводится некоторый коэффициент их упаковки h = pd3N0/6V0, где Vo— мольный объем жидкости; No— число Авогадро. Коэффициент упаковки выбирают для конкретной жидкости.
На основании выбранных значений h и d, а также принятого для твердых сфер указанного выше потенциала можно математически определить радиальную функцию распределения частиц, т. е. число частиц, окружающих данную частицу, как функцию расстояния от нее. При этом расчетные значения функции распределения неплохо согласуются с экспериментальными данными для некоторых металлов с плотными структурами кристаллов, т.е. для гексагональной решетки и гранецентрированного куба. Вместе с тем для большинства металлов расчетные и экспериментальные данные расходятся.
С целью улучшения этой модели в 60-е гг. Дж. Бернал вместо твердых шаров предложил другие конфигурации частиц. Он провел эксперименты с пластилиновыми шарами, подвергнув конструкцию из этих шаров всестороннему сжатию. После сжатия частицы принимали форму многогранников с гранями от треугольных до 12-угольных. Однако значительная часть (больше 30%) частиц принимали вид многогранника с пятиугольными гранями. На основании этого Дж. Бернал сделал вывод, что в жидкости вокруг атома может образовываться кольцо из 5 «соседей». В кристаллах такого координационного числа нет. В остальном модель Бернала остается моделью твердых сфер, отличие состоит в том, что взаимодействуют не отдельные шары, а некоторые их конфигурации, имеющие вид рассмотренных выше фигур, в вершинах которых расположены частицы. Теория Бернала дает неплохие результаты для ряда сжиженных газов (аргон, гелий и т. д.).
Общим недостатком псевдогазовых моделей является игнорирование фактических данных о наличии в жидкости достаточно сильных сил связи. Практически эти модели никак не объясняют, почему жидкость сохраняет свой объем и ее частицы не разлетаются, занимая весь предоставленный объем, как в газах. Чем вызывается плотность упаковки?
Общим для всех квазикристаллических моделей является попытка при описании жидкого состояния учесть специфику сил межчастичного взаимодействия, установить связь структуры жидкости с предшествующим плавлению кристаллическим строением вещества.
Согласно сиботаксической модели Стюарта жидкость состоит из множества хаотически ориентированных микрокристаллических областей — сиботаксисов. Эту модель можно считать частным случаем квазиполикристаллических моделей. В современном виде идеи этих моделей сформулированы В. И. Архаровым и И. А. Новохатским. Жидкость состоит из двух структурных составляющих: кластеров и разупорядоченной зоны. В разупорядоченной зоне структура и тепловое движение соответствуют сильно сжатым реальным газам. В кластерах структура и тепловое движение соответствуют кристаллам. Между кластерами и разупорядоченной зоной нет четко выраженной границы раздела. Эта точка зрения в том или ином виде развивается в других квазикристаллических моделях. Отличия состоят в толковании кластера, характера его движения и межкластерного взаимодействия. Выше мы описали подход к понятию кластера как коллектива частиц кристалла, находящегося внутри сферы деформации около вакансии. Следует заметить, что внутри кластера исходная структура кристалла не повторяется, сохраняется только ближний порядок, т. е. конфигурации первых координационных сфер решетки кристалла.
Все квазикристаллические модели трудно поддаются количественному математическому описанию.
1.1.4. МАТЕМАТИЧЕСКИЕ И ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ЖИДКОГО СОСТОЯНИЯ
Выделим в среде частицу и проведем сферический слой толщиной dR на расстоянии R от этой частицы. Пусть в этом слое находится dN частиц. Число частиц в единице объема вещества на расстоянии R выразится формулой r(R) = dN/(4pR2dR). Эта величина в общем случае зависит от расстояния R. Она называется радиальной функцией распределения частиц и полностью характеризует структуру вещества. Для идеальных газов характерно хаотическое распределение молекул. Поэтому в среднем в каждой точке газа содержится одинаковое число молекул. В этом случае r(R) не зависит от координаты R и совпадает с объемной плотностью частиц. В идеальных кристаллах частицы расположены только на координационных сферах. Поэтому r(R) между сферами равна нулю. Графически функция радиального распределения частиц в гранецентрированной решетке показана на рис. 1.11 (R— атомный радиус).
Жидкость—динамическая система. Поэтому распределение частиц в ней носит случайный характер. Для описания r(R) следует поэтому использовать аппарат теории вероятностей.
Вероятность того, что в сферическом слое около молекулы 1 можно обнаружить частицу 2, равна dP(R) = W(R)• 4pR2dR/N. Смысл этого выражения сводится к следующему. Представим, что на бумаге начерчен круг радиуса R1, внутри которого находится круг меньшего радиуса R2. Мы с закрытыми глазами ставим внутри большого круга точку. Как оценить вероятность того,
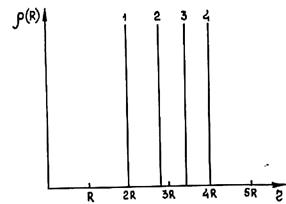
Рис. 1.11. Радиальная функция распределения для гранецентрированного кубического кристалла
что точка попадет внутрь малого круга? Если R2 = R1, то очевидно, что вероятность равна 1. Будем уменьшать радиус малого круга. Ясно, что вероятность будет уменьшаться. Если R2 = 0, то вероятность равна нулю. Поэтому вероятность (отношение числа положительных исходов к общему числу испытаний) можно вычислить как отношение площади малого круга к площади большого круга. Это будет справедливо, если положение частицы 2 не зависит от положения частицы 1.
Если между частицами есть силы взаимодействия, то очевидно, что вероятность нахождения частицы 2 на расстоянии R зависит от того, находится или нет частица / в начале координат. Этот факт учитывается множителем W(R), который называется корреляционной функцией распределения. Если частицы не взаимодействуют, ясно, что W{R} = 1. В случае взаимодействующих частиц W{R) ¹ 1. Так как вероятность нахождения частицы в бесконечной области около данной частицы равна 1, то для корреляционной функции можно написать следующее нормировочное соотношение: 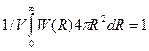 . Выразим число частиц в сферическом слое толщиной dR через радиальную функцию распределения: dN = r(R)4pR2dR. Проинтегрировав это выражение по всему объему среды, получим соотношение
. Выразим число частиц в сферическом слое толщиной dR через радиальную функцию распределения: dN = r(R)4pR2dR. Проинтегрировав это выражение по всему объему среды, получим соотношение 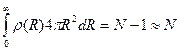 . Сравнивая его с нормировочным соотношением находим, что W(R)=V/N×r(R)=r(R)/r0, где r0 = N/V — среднее число частиц в единице объема. Значит, функция W(R) представляет собой относительную вероятность нахождения частиц на заданном расстоянии R от фиксированной молекулы. Из последней формулы находим p(R) = r0W(R), т. е. для определения радиальной функции распределения нужно знать корреляционную функцию.
. Сравнивая его с нормировочным соотношением находим, что W(R)=V/N×r(R)=r(R)/r0, где r0 = N/V — среднее число частиц в единице объема. Значит, функция W(R) представляет собой относительную вероятность нахождения частиц на заданном расстоянии R от фиксированной молекулы. Из последней формулы находим p(R) = r0W(R), т. е. для определения радиальной функции распределения нужно знать корреляционную функцию.
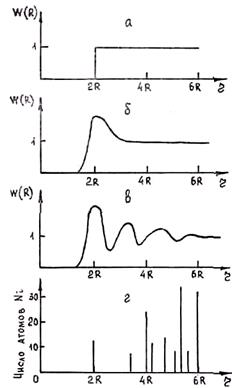
Рис. 1.12. Зависимость корреляционной функции от расстояния для идеального газа (а), реального газа (б), жидкостей (б) и кристалла ГЦК, (г)
Выясним, какой вид имеет функция W(R) для газов, кристаллов и жидкостей. Для газов, как было сказано выше, W(R) = 1, если R > 2r, где r — радиус частицы; W(R) = 0, если R £ 2r, так как r(R) = rо на всех расстояниях, превышающих диаметр частицы. Для кристаллов характер изменения корреляционной функции в зависимости от расстояния совпадает с приведенным выше графиком изменения радиальной функции распределения r(R).
Амплитуды колебаний частиц в жидкостях гораздо больше, чем в кристалле. При этом молекулы жидкости, участвуя в тепловом движении, беспрерывно обмениваются ближайшими «соседями». Если проследить за поведением какой-либо частицы, то можно убедиться, что за время наблюдения она окажется на разных расстояниях от данной частицы. Вследствие этого корреляционная функция W непрерывна. Она испытывает несколько затухающих колебаний относительно единицы. При расстоянии, превышающем некоторое значение, корреляционная функция практически равна 1, т. е. при этом исчезает порядок в размещении частиц. Это подтверждает факт, что в жидкостях нет дальнего порядка. Максимумы на кривой соответствуют более вероятным межмолекулярным расстояниям, минимумы — расстояниям, на которых частицы бывают очень редко. Последовательность максимумов соответствует последовательности равновесных межмолекулярных расстояний в жидкости и поэтому определяет характер ближней упорядоченности. Кривые W(R) для газов (идеальный и реальный), жидкостей и соответствующих кристаллов приведены на рис. 1.12.
Сопоставляя функции W(R} для жидкости и кристалла, видим, что в кристалле максимумы этой функции разделены промежутками, где W(R) = 0, тогда как в жидкости кривая непрерывна.
Для экспериментального исследования строения жидкостей применяют облучение их рентгеновскими лучами, электронами или нейтронами. При этом рентгеновские лучи рассеиваются электронами атомов, электроны — ядрами атомов и нейтроны — магнитным полем атомов. Этими методами изучают зависимость интенсивности рассеянного излучения от угла, под которым производится облучение. Теория методов, на которой мы не останавливаемся, позволяет связать интенсивность рассеивания с корреляционной функцией, т. е. по кривым интенсивности рассеивания излучения, направляемого под разными углами, можно экспериментально определить изменение корреляционной функции с увеличением расстояния.
Экспериментальные данные по изменению коррелятивных функций металлов показали, что для плотноупакованных металлов в твердом состоянии характерно сохранение ближнего порядка, имеющего место в кристалле, и уменьшение координационного числа. Первый максимум на кривой радиального распределения находится практически на том же расстоянии, что и радиус первой координационной сферы кристалла. Так, для меди в кристалле r1 = 2,55 Å; первый максимум на корреляционной кривой находится на расстоянии 2,55 Å; для алюминия расстояния равны 2,86 и 2,94; для железа — 2,52 и 2,52; для цинка — 2,9 и 2,71 Å. Второй максимум на корреляционной кривой охватывает интервал расстояний, в который попадают радиусы второй, третьей и четвертой координационных сфер кристалла золота. Уменьшение координационного числа при плавлении плотноупакованных металлов (например у алюминия с 12 до 10,8) связано с увеличением объема при плавлении и возрастанием числа вакансий.
Для рыхлых, некомпактноупакованных в твердом состоянии металлов (висмут, олово, сурьма, галлий, кремний, германий и т. п.) также характерно малое отличие расстояния первого максимума на корреляционной кривой от радиуса первых координационных сфер кристаллов (у висмута эти расстояния равны соответственно 3,25 и 3,09, у олова — 3,25 и 3,15, у сурьмы — 3,30 и 2,9 Å). Координационное число у этих металлов при плавлении увеличивается, что связано с уменьшением их объема (у висмута, например, координационное число увеличивается с 3 до 7,5 Å).
Таким образом, экспериментальные исследования подтверждают теоретические выводы о сохранении ближнего порядка кристаллов в жидких металлах и связи их строения со строением исходного кристалла.
Как следует из сказанного выше, для определения радиальной функции распределения необходимо знать корреляционную функцию. Об ее экспериментальном определении мы уже говорили. Математическое ее вычисление составляет предмет статистической физики жидкого состояния, одним из основателей которой можно признать выдающегося советского ученого академика Н. Н. Боголюбова. Рассмотрение этого вопроса выходит за пределы нашего курса.
1.1.5. ОСОБЕННОСТИ СТРОЕНИЯ ЖИДКИХ СПЛАВОВ
В отличие от чистых металлов, которые плавятся при фиксированной температуре, плавление и затвердевание сплавов осуществляется в некотором интервале температур. Температура, при которой начинается плавление или заканчивается затвердевание сплава, называется температурой солидуса Тс. Температура, при которой заканчивается плавление или начинается затвердевание,. называется температурой ликвидуса Тл. Выше температуры ликвидуса существует жидкий сплав, ниже температуры солидуса — твердый сплав. В интервале ликвидус — солидус, который может составлять более 100 °С и называется интервалом кристаллизации имеется двухфазное состояние, т. е. твердая и жидкая фазы сосуществуют. Температура ликвидуса определяется условиями равновесия жидкого сплава данного состава с выделяющейся из него твердой фазой. Аналогично температура солидуса определяется условиями равновесия твердой фазы, отвечающей составу сплава, с жидкой фазой.
В процессе плавления сплава изменяется не только его температура, но и химический состав находящихся в равновесии фаз. Как известно из курса «Металловедение», равновесие различных фаз в сплавах характеризуется диаграммами состояния, связывающими концентрации фаз с температурой и давлением. Известно много типов диаграмм состояния, зависящих от растворимости компонентов в жидком и твердом состояниях.
Вводимые в сплав компоненты могут растворяться в основном металле, образуя твердые растворы. При этом если область растворимости примыкает к чистому металлу, т. е. начинается с нулевой концентрации (на диаграмме «сигара» или ее участок начинается от чистого компонента), то при образовании раствора сохраняется тип кристаллической решетки основного металла (рис. 1.13, а). Если же область твердого раствора не примыкает к чистым металлам, то, как правило, образуется новая, более сложная, решетка (рис. 1.13, б). Если в этом случае интервал растворимости невелик, то образуются так называемые интерметаллические соединения, представляющие собой также твердые растворы со специфической решеткой.
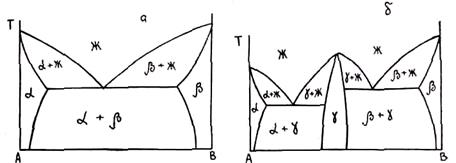
Рис. 1.13. Диаграммы состояния сплавов эвтектического типа без интерметаллидов (а) и с интерметаллидами (б)
Примеров интерметаллидов очень много, и часто именно они определяют механические и технологические свойства сплавов. Например, металлографию алюминиевых сплавов очень часто называют металлографией интерметаллидов. В качестве примера можно привести бинарные интерметаллиды CuAl2, Mg2Si, Mg2Al3 и т. д. Во многих случаях интерметаллиды могут быть многокомпонентными. Необходимо отметить, что часто и интерметаллиды могут образовывать твердые растворы с основным металлом.
Различают два типа твердых растворов: растворы замещения и растворы внедрения. В растворах замещения ионы легирующего компонента размещаются в узлах кристаллической решетки, замещая ионы основного металла-растворителя. Это имеет место тогда, когда размеры атомов компонентов близки друг к другу. Примерами растворов замещения являются растворы никеля в меди, цинка в меди и многие другие. Если размеры атомов сильно различаются и атомы имеют разные строения электронных оболочек, например у металлов и неметаллов, то образуются растворы, внедрения (растворы бора, кислорода, азота). В них атомы растворенного вещества располагаются внутри кристаллической ячейки (в междоузлиях).
Введение легирующего компонента в раствор как при замещении, так и при внедрении искажает кристаллическую решетку, изменяет ее параметр и вызывает упругое напряженное состояние. Кроме того, легирующие компоненты оказывают влияние на скорость перемещения дислокаций.
Растворимость в твердом состоянии зависит от близости атомных диаметров компонентов, однотипности их кристаллических решеток и сходства строения внешних электронных оболочек. В соответствии с правилом Юма — Розери для образования непрерывной растворимости различие в размерах атомов не должно превышать 15%. При больших различиях деформация решетки столь велика, что образование раствора становится термодинамически невыгодным.
При плавлении сплавов и металлов сохраняется ближний порядок (распределение атомов в первых координационных сферах). Исследования показывают, что в жидком и твердом состояниях число атомов каждого сорта в первых координационных сферах пропорционально их концентрации. Кривые интенсивности рассеяния излучений и радиальной функции распределения для сплавов напоминают аналогичные кривые для компонентов, отличаясь лишь координатами расположения максимумов. Максимумы располагаются между максимумами, характерными для чистых компонентов, и по мере увеличения компонента смещаются от одного компонента к другому. Если в твердом растворе атомы расположены статистически, т. е. неупорядоченно, то и в жидком сплаве сохраняется неупорядоченность, и наоборот, упорядоченность в расположении атомов в твердом растворе при плавлении сохраняется.
Статистическое распределение атомов в растворе имеет место, когда энергии парного взаимодействия атомов А и В связаны соотношением Uaa = Ubb = Uab. В этом случае конфигурации А — А, А — В, В — В энергетически равноценны. В этих сплавах расстояние первого максимума на кривой радиального распределения и координационное число линейно изменяются с увеличением концентрации от значений этих величин для компонента А к их значениям для компонента В. При плавлении интерметаллидов, если между компонентами существует сильное взаимодействие, сохраняется ближний порядок в расположении атомов, характерный для твердых интерметаллидов.
Эвтектические сплавы образуются из компонентов, различающихся кристаллической решеткой и имеющих ограниченную растворимость в твердом состоянии. Этот тип сплавов чаще всего образуют металлы и неметаллы (например алюминий — кремний) и металлы с сильно различающимися параметрами решетки (например медь с серебром). В этом случае силы взаимодействия между одноименными атомами больше, чем между разноименными, т. е. Uaa > Uab, Ubb > Uab. Как показали исследования, при плавлении эвтектики расплав состоит из конфигураций, характерных для фаз a-твердого раствора и b-твердого раствора, составляющих эвтектику. При повышении температуры происходит постепенное перемешивание атомов и образование однородного раствора. Квазиэвтектическая структура в расплаве может сохраняться при перегревах на 200—300°С.
Микронеоднородность жидких сплавов вызывается не только наличием кластеров, но и их различным составом, строением, устойчивостью. Самые устойчивые кластеры образуются наиболее сильно взаимодействующими между собой компонентами. Как показали исследования Б. А. Баума, в бинарных железоуглеродистых сплавах возможно наличие следую-
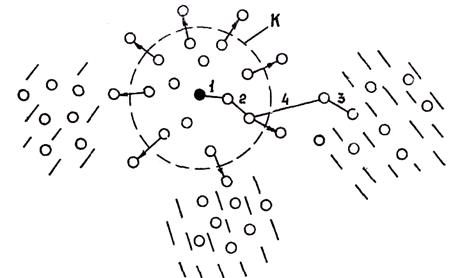
Рис. 1.14. Схема, иллюстрирующая микрунеоднородность железоуглеродистого сплава
щих кластеров. В расплаве существуют межатомные связи Fe — Fe и Fe — С, при этом наиболее сильные — в сплаве Fe — С. Расплав представляет собой неоднородную систему, в которой межатомные связи Fe — Fe в микрообластях, удаленных от атомов примеси, и в непосредственной близости от них отличаются, так как атом углерода вызывает сильные искажения электронной плотности близко расположенных атомов железной матрицы. На рис. 1.14 показана схема микронеоднородной структуры железа, легированного углеродом. Темный кружок обозначает атом углерода; светлый кружок — атом железа; сплошные линии — межатомные связи, номер и длина которых обратно пропорциональны их прочности; заштрихованные области — кластеры типа объемно центрированного куба; окружностью К. ограничен кластер, содержащий углерод.
В системе можно выделить четыре типа межатомных связей, которые в порядке убывания прочности обозначены цифрами 1 — 4. 1 — связь Fe — С внутри кластера, 2 — связь Fe — Fe вблизи атома С, 4 — связь между атомами железа в разных кластерах, 3 — связь между атомами железа в кластере, удаленном от атомов С.
Эта схема характерна для еще не расплавленного сплава. При повышении температуры прежде всего разрываются межкластерные связи 4. Происходит предсолидусное плавление, разнотипные кластеры получают повышенную подвижность. При достижении температуры солидуса начинают разрываться связи 3. Однако эти связи разрываются не все одновременно, процесс разрыва одних связей сопровождается восстановлением других. При этом образуются кластеры, характерные для расплавов чистого железа (заштрихованные области). Этот кластер имеет ближний порядок, характерный для ОЦК. Вместе с этим кластером в расплаве имеется кластер, ограниченный окружностью К. Он имеет структуру ГЦК. Этот кластер обладает повышенной устойчивостью, так как образован более сильными связями. При повышении температуры разрываются сначала связи 2, а затем связи 1.
Реальные железоуглеродистые сплавы многокомпонентны. Поэтому их микронеоднородность носит еще более сложный характер.
1.1.6. ВЗАИМОСВЯЗЬ ЖИДКОГО И ТВЕРДОГО СОСТОЯНИЙ СПЛАВА
Свойства литого сплава в твердом состоянии определяются •свойствами жидкого сплава и условиями его охлаждения в форме. Связь с жидким состоянием сложна и многопланова. Поэтому в данном курсе мы не будем рассматривать ее всесторонне, передав эту задачу технологическим курсам. Рассмотрим основные принципы, определяющие эту связь. Прежде всего, механические и другие свойства сплава в твердом состоянии в значительной мере определяются его кристаллической структурой. Процесс кристаллизации предполагает возникновение в жидком расплаве зародышей новой кристаллической фазы и ее рост. Зародышеобразование непосредственно связано с наличием в жидкости кластеров и их характеристиками. Кроме того, большое значение имеет наличие в расплаве микроскопических включений различного химического состава и строения. Определить их наличие невозможно никаким химическим анализом. Поэтому очень часто при смене поставщика шихтовых материалов при том же химсоставе выплавляемых сплавов существенно изменяются их свойства.
Зависимость свойств сплава от природы шихтовых материалов получила название «наследственность». Кроме неконтролируемого изменения содержания микропримесей наследственность можно объяснить неравновесностью жидкого состояния. Переход системы, является самопроизвольно в течение времени релаксации. При плавлении металла расплав может находиться в неравновесном состоянии, т. е. состав и конфигурация образовавшихся кластеров не обладают минимумом энергии при данных условиях. Если выдержать сплав при данной температуре достаточно долго, то в нем в конце концов установится равновесное состояние. О том, что время релаксации может быть достаточно большим, говорит хотя бы такой факт, что при вводе в расплав металлического феррохрома он не распределяется равномерно в нем даже через 20 мин.
Одним из доказательств неравновесности жидкого расплава является гистерезис свойств при нагреве и последующем охлаждении. Суть гистерезиса состоит в том, что значения свойств, полученные в измерениях в ходе нагрева сплава, не совпадают с соответствующими значениями, полученными при последующем его охлаждении. Повторные циклы измерений дают результаты, совпадающие с теми, которые получены при охлаждении сплава в первом цикле. На рис. 1.15 показан характер гистерезиса кинематической вязкости сплава. Явление гистерезиса не обнаруживается, если сплав перед измерениями подвергнуть достаточной по длительности выдержке. Гистерезис свойств можно объяснить также какими-нибудь превращениями в сплаве при нагреве, связанными с выделением из него включений или продуктов взаимодействия компонентов газовой среды или футеровки. Дискуссии по вопросу, что здесь является главным, продолжаются. Однако можно несомненно признать, что неравновесность состояния сплавов имеет место и ее надо учитывать при организации технологического процесса.
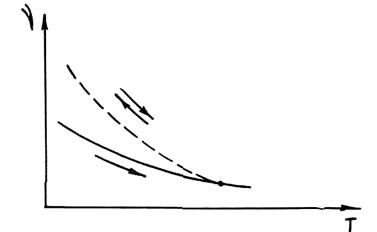
Рис. 1.15. Гистерезис кинематической вязкости
Для управления уровнем неравновесности состояния расплавов сейчас широко применяют термовременную обработку.Приэтом расплав перед разливкой подвергается длительной выдержке при температуре, несколько превышающей температуру заливки. Экспериментальные данные показывают, что при этом устраняется гистерезис свойств и существенно повышаются механические свойства литого сплава.
ГЛАВА 1.2. РЕОЛОГИЧЕСКИЕ СВОЙСТВА ЖИДКИХ И ТВЕРДЫХ СПЛАВОВ
Реология — наука, которая изучает деформации тел. Следует напомнить, что деформация— это изменение размеров и формы тела. Реология устанавливает связь между напряжениями, создаваемыми приложенными к телу силами, и вызываемыми ими деформациями. В теории литейных процессов идеи реологии начали использоваться не более 10—15 лет назад. Для реальных физических объектов связь между напряжениями и деформациями можно выразить в виде следующего уравнения: F(t, e, e, en, t, t,..., tm) = 0.
1.2.1. ПРОСТЕЙШИЕ РЕОЛОГИЧЕСКИЕ МОДЕЛИ ТЕЛ
Простейшим в реологическом отношении твердым телом является тело Гука (тело Н), для которого характерна линейная связь между напряжениями и относительными деформациями. Как известно, на законе Гука основывается такая наука, как сопротивление материалов. В соответствии с этим законом при одноосном растяжении s = Еe, а при сдвиге t = gG, где s — нормальное (приложенное перпендикулярно площадке) напряжение; t — касательное, т. е. действующее в параллельной плоскости, напряжение; e — относительная деформация растяжения (e = ∆l/l), т. е. отношение увеличения длины образца к его первоначальной длине; g — относительная деформация при сдвиге; Е — модуль упругости при растяжении (модуль Юнга) и G — модуль упругости при сдвиге.
Относительную деформацию при сдвиге можно определить в соответствии со схемой (рис. 1.16). Модуль упругости при сдвиге связан с модулем Юнга следующей зависимостью: G = E/[2(1 + m)], где m (коэффициент Пуассона) — отношение поперечной относительной деформации при сужении растягиваемого образца (поперечное сужение) к относительной деформации растяжения (для алюминия (m = 0,33, для стали m = 0,28, для бронзы m = 0,35). При растяжении s = F/S, где F — действующая сила; S — площадь сечения образца, перпендикулярного направлению силы. Поэтому напряжения, создаваемые при растяжении,
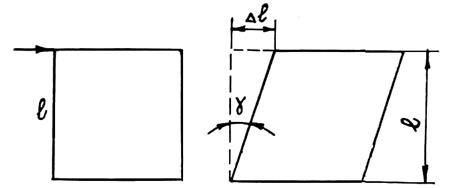
Рис. 1.16. Схема деформации при сдвиге
можно рассматривать как нормальные. При сдвиге t = f/s, где F— действующая сила, вектор которой лежит в плоскости S. Поэтому напряжение t называется касательным напряжением. В сложных случаях нагружения действующие силы создают одновременно и нормальные, и касательные напряжения.
В системе координат напряжение — деформация — время поведение тела Гука иллюстрируется схемой, приведенной на рис. 1.17. Суть состоит в том, что при приложении нагрузки в теле мгновенно возникают упругие деформации, пропорциональные напряжениям. В процессе выдержки они не меняются. При снятии нагрузки размеры тела возвращаются в исходное положение. В качестве механической аналогии тела Гука в реологии принята спиральная пружина, изображенная на рис. 1.18.
Естественно, что механическое поведение твердых тел не исчерпывается моделью Гука, и с более сложными реологическими законами твердых тел мы познакомимся в дальнейшем. Сейчасжеперейдем к рассмотрению реологических законов жидкостей.
С точки зрения механического поведения жидкости отличаются от твердых тел текучестью и малой сжимаемостью. Текучесть — свойство тела развивать сколь угодно большие деформации под действием сколь угодно малых напряжений. В твердом теле под действием приложенных усилий развивается напряженное состояние которое характеризуется наличием касательной и нормальной составляющей (рис. 1.19, а). Касательное напряжение t вызывает деформацию сдвига слоев тела вдоль плоскости тп. Напряжения носят упругий характер до тех пор, пока они непревзойдут некотором величины, называемой пределом текучести. При этом часть тела A начнет смещаться, т. е. течь относительно тела В по плоскости тп.
Жидкость в отличие от твердого тела в состоянии покоя не может развивать касательных напряжений, т.е. напряжения в ней (давления) всегда ориентированы перпендикулярно к площадке. В жидкости могут развиваться поэтому только нормальные напряжения. В силу этого касательные составляющие приложенных к жидкости сил не могут быть уравновешены напряжениями и, какова бы ни была величина этих усилий, они приведут к неограниченному смещению тела А относительно В, т. е. к течению (рис. 1.19, б). Можно сказать, жидкость — это среда, предел текучести которой равен нулю. Именно поэтому жидкость не имеет своей формы, а принимает всегда форму сосуда. Если ее предоставить самой себе в условиях поля тяжести Земли, то она растечется до слоя, толщина которого имеет порядок размеров молекулы или атома. В отличие от газов жидкость не занимает всего предоставленного ей объема сосуда. Она имеет четко выраженную поверхность раздела с воздухом.
&
 2015-06-05
2015-06-05 3365
3365
