Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химических веществ.
В основе молекулярно-кинетической теории лежат основные положения:
1. Вещество состоит из атомов (молекул).
2. Атомы (молекулы) вещества находятся в непрерывном хаотическом тепловом движении.
3. Между атомами (молекулами) вещества действуют силы притяжения и отталкивания, зависящие от расстояния между частицами.
4. Характер теплового движения молекул зависит от того, в каком агрегатном состоянии (твердом, жидком или газообразном) находится вещество.
Эти основные положения подтверждаются экспериментально и теоретически.
Количество вещества равно отношению числа атомов (молекул) этого вещества к числу Авогадро: 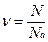 . Единица размерности ν - моль.
. Единица размерности ν - моль.
Молярная масса M равна массе вещества, взятого в количестве одного моля. Единица размерности M - кг/моль.
Количество вещества (в молях) равно 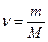 .
.
Задача молекулярно-кинетической теории состоит в том, чтобы установить связь между микроскопическими (масса, скорость, кинетическая энергия молекул) и макроскопическими параметрами (давление, газ, температура).
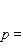

Это уравнение называют основным уравнением молекулярно-кинетической теории газов. Здесь n – концентрация молекул газа, число молекул в единице объема, Ек – средняя кинетическая энергия движения молекул газа
Для изменения кинетической энергии необходимо изменить температуру.
Единица измерения температуры Т по шкале Кельвина называется кельвином К. Температурная шкала Кельвина называется абсолютной шкалой температур.
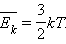
Тогда
p = nkT,
где n = N / V – концентрация молекул (то есть число молекул в единице объема сосуда), k – постоянной Больцмана.
 2015-06-05
2015-06-05 499
499







