Рассмотренный ранее процесс электрохимической коррозии с его дифференциацией на анодную стадию ионизации металла и катодную стадию электрохимического восстановления, присутствующего в растворе деполяризатора может быть представлен поляризационной диаграммой (см. рис. 2). На этой диаграмме ∆Е° = Е0к – Е0а означает начальную разность потенциалов катодных и анодных участков, а кривые, проходящие через точки Е0к и Е0а соответственно, характеризуют зависимость потенциалов катодных и анодных участков от силы тока, т. е. являются кривыми катодной и анодной поляризации. Они пересекаются в точке, абсцисса которой определяет максимальную силу тока коррозионного элемента imах, для которой ранее было выведено уравнение (7).
Поляризационная диаграмма коррозионного процесса дает возможность установить не только значение максимальной силы тока и отвечающей ему стационарный потенциал, но и позволяет оценить влияние анодной и катодной стадий на скорость коррозии. В тех случаях, когда электропроводность коррозионной среды мала, она позволяет определить роль омического фактора. Количественное влияние катодной и анодной стадий на скорость коррозионного процесса, а также роль омического фактора могут быть выражены с помощью так называемой степени катодного, анодного и омического контроля, соответственно обозначаемых через Ск, Са и СR. Все три величины определяются следующим образом:
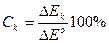 (11)
(11)
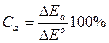 (12)
(12)
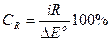 (13)
(13)
где ∆Ек и ∆Еа — соответственно смещение потенциала работающего катода и анода от их начальных значений при данной силе тока; iR — падение напряжения на омическом сопротивлении электролита между катодными и анодными участками.
Степень омического контроля (см. рис. 2) равна нулю при полной заполяризованности коррозионного элемента, когда сила тока i = imax. Скорость коррозии металла при этом определяется лишь начальной разностью потенциалов и поляризационными характеристиками катодной и анодной стадий.
В общем случае скорость коррозии зависит не только от катодной и анодной поляризаций, но и от омического сопротивления коррозионной среды. Поэтому для каждого данного коррозионного процесса характерно вполне определенное соотношение между величинами Ск, Са и СR.
Следует выделять три наиболее типичных случая:
а) катодный контроль: ∆Ек ≈ ∆Е°, Ск →100%. Коррозия металлов в нейтральных средах, как и рассмотренная в предыдущей работе кислотная коррозия чистого цинка, происходит с преобладающим катодным контролем;
б) анодный контроль: ∆Еа ≈ ∆Е°, Са → 100%. Полный или преобладающий анодный контроль имеет место при коррозии в окислительных средах алюминия, нержавеющей стали и ряда других легко пассивирующихся металлов;
в) омический контроль iR ≈ ∆Е°, С R → 100%. Коррозия при омическом контроле протекает в средах с очень низкой проводимостью.
Наряду с указанными примерами полного или преобладающего контроля скорости коррозии каким-либо одним фактором встречаются случаи смешанного контроля. Этим и определяется необходимость точной оценки степени контроля каждого фактора для характеристики работы коррозионного элемента. На практике такие определения могут быть проведены на модели коррозионного элемента с электродами макроскопических размеров. Электрическая схема установки для этой работы приведена на рис. 6. Основная часть установки — коррозионный элемент, состоящий из двух электродов, помещенных в ячейку. Электроды изготовлены из различных металлов (если преследуется цель моделирования процессов структурной коррозии гетерофазного сплава); они могут состоять также из одного и того же материала, но тогда различаться должна либо подготовка поверхности электродов, либо состав среды. Оба электрода коррозионной пары последовательно замкнуты на переменное сопротивление R и токоизмеряющий прибор (микро- или миллиамперметр). В процессе работы коррозионной пары потенциалы электродов измеряют с помощью потенциометра или же регистрируют на автоматическом электронном самописце.
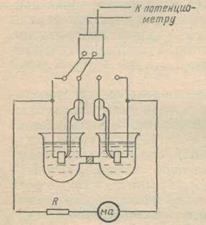
Рис.6. Установка для исследования работы коррозионного элемента
 2015-07-14
2015-07-14 798
798








