Спектроскопия ядерного магнитного резонанса (ЯМР) является наиболее мощным методом физико-химического исследования органических соединений.
С помощью ЯМР-спектроскопии можно решать те же задачи, что и с помощью ИК- и УФ-спектроскопии: определять структуру органических соединений, проводить кинетические измерения, решать задачи количественного и качественного анализа. Наибольшее применение получил протонный магнитный резонанс (ПМР) – резонанс на ядрах водорода, поскольку этот вид ЯМР применяется наиболее широко.
Ядро атома водорода (протон) обладает магнитным моментом. Если протон попадает в постоянное магнитное поле, то магнитный момент его может быть направлен или по направлению внешнего магнитного поля или против; в первом случае его спин равен минус 1/2, во втором +1/2. Расположение по направлению магнитного поля энергетически несколько более выгодно, и, чтобы расположиться против направления магнитного поля, ядро должно получить определенный квант энергии, который обозначают ∆E. Поэтому, если дополнительно воздействовать на протон излучением с такой частотой, чтобы соблюдать равенство ∆E = hν (h – постоянная Планка), то будет происходить резонансное поглощение этого излучения и изменение ориентации его магнитного спина; в спектре появится сигнал протонного резонанса данного типа атомов, т.е. пик поглощения на регистраторе резонанса. В зависимости от окружения, в котором находятся ядра водорода, сигнал протонного магнитного резонанса может находиться при различных значениях резонансной чистоты. Меняя радиочастоту в области всего спектра, мы получим своеобразную «фотографию» всех протонов, содержащихся в веществе, и изображенную пиками поглощения в спектре.
Спектрометр ПМР имеет мощный магнит, способный создать однородное магнитное поле напряженностью от 10000 и более эрстед. Между полюсами этого магнита помещается ампула с образцом. Для устранения флуктуаций в однородности поля ампула быстро вращается. Имеется генератор радиоизлучения, которое направлено перпендикулярно магнитному полю. Спектр записывается регистратором резонанса.
Принято характеризовать спектрометры ПМР по рабочей частоте генератора резонанса, которая связана с напряженностью магнитного поля прямой пропорциональной зависимостью. Выпускают спектрометры с рабочей частотой 80, 100, 200, 300 мегагерц (МГц), следовательно, с длиной волны 5,3, 1,5 и 1м. Таким образом, для облучения вещества в ЯМР-спектрометрах используются радиоволны.
Основное уравнение протонного магнитного резонанса имеет вид:
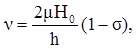
где Н0 – напряженность магнитного поля;
ν – частота излучения;
μ – магнитный момент ядра, равный для протона 2,7927;
h – постоянная Планка;
d – константа экранирования, которая характеризует величину локальных магнитных полей, экранирующих ядро.
Чем больше электронная плотность у ядра, тем более сильные локальные магнитные поля возникают, они экранируют ядро от действия приложенного магнитного поля Н0. При этом резонансный сигнал наблюдается в более сильных полях. Величина возникающих локальных магнитных полей зависит от заместителей у ближайшего углеродного атома, а также от строения более удаленных частей молекулы. Чем сильнее оттянуты электроны от протона, тем в более слабых полях (т.е. левее в спектре) наблюдается его резонансная частота в виде пика поглощения.
Положение сигнала протонного магнитного резонанса измеряется по отношению к какому-либо эталону. Международным эталоном является тетраметилсилан (ТМС) – (СН3)4Si, сигнал которого наблюдается в сильном поле, так как кремний более электроположителен, чем углерод, и поэтому электронная плотность в месте нахождения протонов у данного соединения велика. Большинство других органических соединений имеют сигналы в более слабых полях. Расстояние сигнала протонов вещества от сигнала эталона называется химическим сдвигом. Химический сдвиг – одна из основных характеристик спектров ПМР. Величина химического сдвига чаще всего обозначается d и может быть выражена в герцах. Однако эта величина зависит от прибора, на котором получен спектр ПМР. Для того чтобы иметь возможность сравнить результаты, полученные на различных приборах, величину химического сдвига измеряют в относительных единицах, получивших название «миллионные доли» (м. д.). Химический сдвиг, выраженный в миллионных долях, определяется как разность между положением сигналов образца и эталона (nобр. – nэт), выраженная в единицах частоты – герцах, – деленная на рабочую частоту прибора n0; эта величина умножается еще на 106:
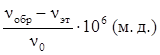
В шкале d сигнал тетраметилсилана принят за 0 (nтмс = 0) и значения химических сдвигов, выраженные в м. д., увеличиваются в сторону более слабых полей.
Химические сдвиги различного типа протонов даны в таблице 3.
Таблица 3 – Химический сдвиг сигналов протонов, м.д.
| № п/п | Тип протонов | Химический сдвиг, d, м.д. |
| Алифатические углеводороды Алифатические a-замещенные соединения, Х–СН2–Н Ацетиленовые протоны Олефиновые протоны Ароматические протоны Альдегидные протоны Кислотные протоны | 0 – 2 1,6 – 5 2 – 3 4,5 – 8 6 – 9 9 – 10 8 – 11 |
Интенсивность резонансного пика всегда пропорциональна числу эквивалентных протонов, обусловивших появление этого пика. Поэтому по химическому сдвигу и относительной интенсивности линий в спектре ПМР можно сказать, сколько и каких протонов содержится в молекуле органического соединения.
Если в соединении имеется несколько типов различных протонов, то в ПМР-спектре возникает несколько сигналов. Интегральная интенсивность сигналов (определяемая как площадь под кривой) пропорциональна числу протонов каждого вида.
Если мы наблюдаем резонансный сигнал определенных протонов, например, групп –СН3, =СН2, ºСН, а у соседних атомов углерода, находится n эквивалентных протонов, то резонансный сигнал протонов этих групп расщепляется на (n+1) линий – спин-спиновое расщепление. Расстояние между всеми соседними линиями в расщепленном сигнале одинаково, обычно оно выражается в герцах (Гц), не зависит от рабочей частоты спектрометра и называется константой спин-спинового расщепления (взаимодействия) и обозначается буквой J. Это явление вызвано взаимодействием спинов неэквивалентных протонов через валентные электроны. Величина константы J зависит от количества и характера связей между взаимодействующими ядрами и от структуры молекулы.
Хотя спин-спиновое расщепление и усложняет картину спектра, мультиплетность (сложность) сигнала дает дополнительную и весьма ценную информацию о характере расположенных рядом групп протонов.
Для съемки спектра ПМР обычно берут 5-15%-ный раствор вещества в растворителях, как правило, не имеющих своих протонов, чтобы не усложнять картину спектра (ССl4, СS2). Часто применяется дейтерированные растворители – дейтерохлороформ (CDCl3), дейтерометанол (CD3OD), дейтеробензол (C6D6), дейтероуксусная кислота (CD3COOD) и др.). В раствор прибавляют каплю тетраметилсилана в качестве внутреннего стандарта.
Дополнительную информацию об использовании спектров ПМР и анализе органических соединений можно получить в специальных руководствах /20, 21, 27/, учебниках и практикумах по органической химии /28-32/.
6 ИСПОЛЬЗОВАНИЕ КОНСТАНТ ДЛЯ ИДЕНТИФИКАЦИИ
ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Каждое органическое соединение характеризуется постоянными физическими свойствами в определенных условиях (температура и давление). Из этих физических свойств легче всего определяются и, как правило, приводятся в химической литературе при описании отдельных соединений следующие: температура плавления, температура кипения, показатель преломления, плотность, молекулярная рефракция, УФ–, ИК– и ЯМР-спектры.
Наиболее простым и удобным способом контроля наличия примесей в полученном соединении или установлении тождества неизвестного соединения с известным (идентификация) является сопоставление его физических констант с их справочными значениями. В случае отсутствия справочных данных о чистоте продукта можно судить по достижению неизменных значений физических констант в процессе многократно повторяемых циклов очистки.
Абсолютно чистое вещество можно представить себе только теоретически. В практике чистое вещество характеризуется содержанием примесей ниже определенного предела. Этот предел, как правило, составляет доли процента и менее. Получить особо чистое вещество – чрезвычайно сложная и важная технологическая задача, решенная пока для немногих веществ.
 2015-07-14
2015-07-14 4917
4917
