Бор, алюминий и их соединения
Цель работы: Изучить основные химические свойства алюминия, а также важнейших соединений алюминия и бора.
Опыт 1Л. Получение и свойства ортоборной кислоты
а) Приготовьте в пробирке на 1/3 ее объема насыщенный (при нагревании) раствор буры. Осторожно добавьте концентрированной серной кислоты. Охладите пробирку в сосуде со льдом. Отметьте цвет кристаллов.
Получение Н3ВО3: …………………………………………………………………………..
б) Поместите в пробирку немного борной кислоты и добавьте 1-2 мл воды. Отметьте растворимость. Нагрейте пробирку в пламени спиртовки. Как меняется растворимость кислоты с ростом температуры? Слегка остывший раствор испытайте лакмусовой (красной и синей) и универсальной индикаторными бумажками.
Наблюдения: …………………………………………………………………………………
…………………………………………………………………………………………………………..
Уравнение диссоциации кислоты: ………………………………………………………………..
Киониз.Н3ВО3 = 7,1.10-10
Вывод (о силе кислоты): ……………………………………………………………………………
в) Ушком очищенной нихромовой проволочки захватите несколько кристалликов кислоты и внесите в несветящееся пламя горелки.
Ортоборная кислота окрашивает пламя горелки в …………………………….цвет.
Опыт 2Л. Свойство солей борной кислоты
а) Испытайте раствор буры лакмусовой бумагой.
Уравнение гидролиза: ……………………………………………………………………...
……………………………………………………………………....; среда ……………….; рН…7.
б) Накалите ушко нихромовой проволочки в пламени спиртовки и захватите им несколько кристалликов буры (борной кислоты). Прилипшие кристаллы нагрейте в пламени до их плавления. Проволоку с образовавшимся стекловидным перлом (полиметаборатом) опустите в пробирку с крепким раствором соли кобальта и снова нагрейте до плавления. Объясните наблюдаемое. Аналогичные опыты проделайте с солями хрома(III), никеля.
Уравнения реакций:
………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
Со(ВО2)2 – синий; Сr(BO2)3 - ……………………………; Ni(BO2)2 - ………………….
Опыт 3Л. Обнаружение оксидной пленки на поверхности алюминия
В пламени горелки нагрейте алюминиевую проволоку, держа ее щипцами.
Расплавленный металл не отделяется от проволоки, т.к. …………………………..
…………………………………………………………………………………………………………..
Опыт 4Л. Взаимодействие алюминия со щелочами
[Al(OH)4]- + 3e- = Al + 4OH-; φ0 = -2,31 В
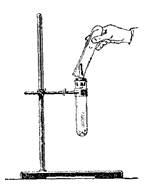 В пробирку поместите немного стружек или опилок алюминия и прилейте 30% раствор щелочи. Закройте пробирку пробкой со вставленной стеклянной трубкой с оттянутым концом. Если реакция протекает медленно, слегка подогрейте пробирку пламенем спиртовки. Проверьте выделяющийся водород на чистоту! Если газ чистый – подожгите его. Помните о ТБ при работе с водородом!
В пробирку поместите немного стружек или опилок алюминия и прилейте 30% раствор щелочи. Закройте пробирку пробкой со вставленной стеклянной трубкой с оттянутым концом. Если реакция протекает медленно, слегка подогрейте пробирку пламенем спиртовки. Проверьте выделяющийся водород на чистоту! Если газ чистый – подожгите его. Помните о ТБ при работе с водородом!
Рис.. Прибор для Уравнение реакции:
получения водорода ……………………………………………………………………….
 2015-07-21
2015-07-21 1101
1101