Вычислить реальные нулевые потенциалы реакции окисления железа (II) бихроматом при рН=3, используя полуреакции и стандартные потенциалы предыдущего примера.
Решение:
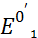 =
= 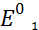 –
– 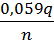 * pH = 1,36 –
* pH = 1,36 – 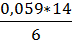 * 3 = 0,95 В
* 3 = 0,95 В
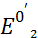 =
= 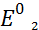 = 0,77, т.к. q = 0
= 0,77, т.к. q = 0
для вычисления реальных констант равновесия в конкретных условиях используют реальные нулевые потенциалы:
Kp = 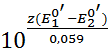 (10)
(10)
 2015-08-12
2015-08-12 630
630








