Важнейшей составной частью ионселективных электродов является полупроницаемая мембрана – тонкая пленка, отделяющая внутреннюю часть электрода (внутренний раствор) от анализируемого и обладающая способностью пропускать ионы только одного вида (катионы или анионы).
Способность мембраны быть проницаемой для ионов определенного знака заряда обусловлена наличием ионогенных групп. Если мембрана контактирует с двумя растворами иона А+ с активностями а1 (анализируемый раствор) и а2 (внутренний раствор), то и на внешней и на внутренней сторонах мембраны происходит обмен ионами. Из-за различия активностей ионов А+ в растворе и мембране на обеих сторонах мембраны возникают граничные потенциалы Е1 и Е2 соответственно. С помощью, так называемых электродов сравнения, помещенных во внешний и внутренний растворы, можно измерить разность (Е1-Е2) или так называемый мембранный потенциал (Ем):
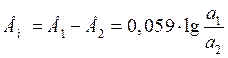
Активность ионов А+ во внутреннем растворе постоянна, поэтому
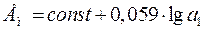
потенциал мембранного электрода линейно зависит от логарифма активности иона А+ в анализируемом растворе.
Любая мембрана в той или иной мере проницаема для всех ионов одного вида, находящихся в растворе, и поэтому необходимо учитывать влияние посторонних ионов, например, В+, на потенциал электрода. Ионы В+ проникают в фазу мембраны в результате реакции обмена:
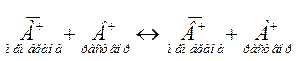
Константа равновесия этой реакции (константа обмена, КА-В) зависит от природы мембраны и природы иона В+. Подвижности ионов А+ и В+, uA и uB в фазе мембраны различны, поэтому возникает диффузионный потенциал, вносящий определенный вклад в величину Ем.
Потенциал мембранного электрода в растворе, содержащем кроме определяемого иона А посторонние ионы В, С и другие, описывается модифицированным уравнением Нернста – уравнением Никольского:
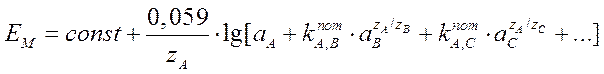 ,
,
где zA – целое число, по знаку и величине равное заряду иона А (зарядовое число); zВ и zС – то же, для ионов В и С; kпот – потенциометрический коэффициент селективности; const – включает значения потенциалов внешнего и внутреннего электродов сравнения и зависит от природы мембраны, поскольку включает величину граничного потенциала на внутренней стороне мембране.
Потенциометрический коэффициент селективности, 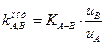 , отражает относительное влияние ионов А и В на величину мембранного потенциала и характеризует способность мембраны различать ионы А и В, А и С и т.д.
, отражает относительное влияние ионов А и В на величину мембранного потенциала и характеризует способность мембраны различать ионы А и В, А и С и т.д.
Основными характеристиками ионселективного электрода являются:
1) электродная функция;
2) селективность;
3) время отклика.
Электрод имеет нернстовскую электродную функцию в интервале активностей (концентраций), где зависимость потенциала от рА (-lg а А) линейна и имеет угловой коэффициент 59,16/zA мВ (250С). Протяженность этого интервала зависит от природы мембраны. При низких концентрациях (для хороших электродов порядка 10-6 М) электрод утрачивает электродную функцию (рис. 1); точка перегиба на графике характеризует практическую величину предела обнаружения.

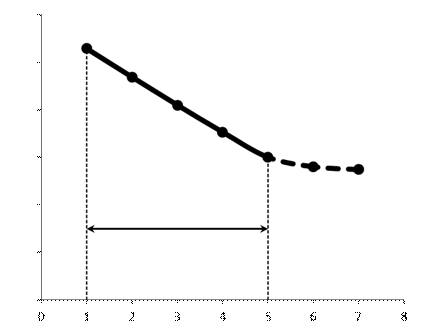
Рис. 1. Интервал выполнения электродной функции и предел обнаружения
ионселективного электрода
Селективность электрода определяется величиной 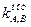 . Если
. Если 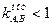 , то электрод селективен относительно ионов А. Чем меньше числовая величина
, то электрод селективен относительно ионов А. Чем меньше числовая величина 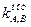 , тем выше селективность.
, тем выше селективность.
Существуют различные способы оценки величины 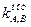 . Чаще других используют метод смешанных растворов, основанный на измерении потенциала электрода в растворах с постоянной концентрацией мешающего иона В и переменной концентрацией определяемого иона А. Точка пересечения линейных участков полученной зависимости (рис. 2) дает величину аА, по которой рассчитывают
. Чаще других используют метод смешанных растворов, основанный на измерении потенциала электрода в растворах с постоянной концентрацией мешающего иона В и переменной концентрацией определяемого иона А. Точка пересечения линейных участков полученной зависимости (рис. 2) дает величину аА, по которой рассчитывают 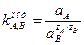 .
.

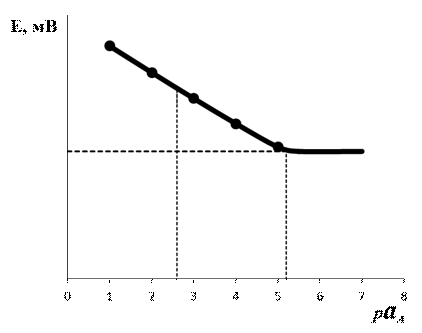
Рис. 2. Определение коэффициента селективности методом смешанных растворов (а В=const)
Иногда используют метод отдельных растворов (биионных потенциалов), который основан на измерении потенциала электрода в растворах, содержащих только ион А и только ион В. По полученным экспериментальным данным, представленным в виде графиков находят коэффициент селективности двумя способами.
Следует заметить, что метод смешанных растворов дает более надежные результаты, чем метод отдельных растворов, и его использование предпочтительно.
Время отклика (время установления стационарного потенциала) определяют по зависимости потенциала электрода от времени с момента погружения в анализируемый раствор. В зависимости от природы мембраны время отклика может колебаться от нескольких секунд до нескольких минут. Время достижения постоянного потенциала зависит от методики работы и изменяется от того, переносят ли электрод из более концентрированного раствора в более разбавленный или наоборот. У большинства электродов за 1 минуту потенциал достигает 90 % от максимальной величины. Чем меньше время отклика, тем лучше, особенно при непрерывных измерениях в потоке или при автоматизированных измерениях.
 2015-08-21
2015-08-21 4308
4308
