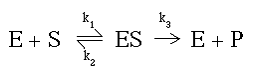 Воспользовавшись предположениями, высказанными Генри, Михаэлисом и Ментен, а также Бриггсом и Холдейном, выведем уравнение, характеризующее реакции, катализируемые ферментом
Воспользовавшись предположениями, высказанными Генри, Михаэлисом и Ментен, а также Бриггсом и Холдейном, выведем уравнение, характеризующее реакции, катализируемые ферментом
Основная гипотеза: этапом, ограничивающим скорость ферментативной реакции является (ES → E + P)
отсюда начальная скорость реакции v0 = k3 [ES];
однако[ES] трудно измерить экспериментально. Принимаем
 |
тогда, количество свободного фермента: [Et] - [ES]
так как [S] >> [Et], [S]связ << [S] свобод
[этап 1] скорость образования ES = k1 ([Et] - [ES]) [S] (1)
скорость распада ES = k2 [ES] + k3 [ES] (2)
[этап 2] гипотеза: Образование фермент-субстратного комплекса самая быстрая реакция, результатом которой является возникновение динамического равновесия между образованием и распадом комплекса, благодаря чему[ ES] = const, и следовательно (1) = (2)
k1 ([Et] - [ES]) [S] = k2 [ES] + k3 [ES]
[Этап 3] k1 [Et] [S] - k1 [ES] [S] = [ES] (k2 + k3)
k1 [Et] [S] = (k1 [S] + k2 + k3) [ES]
[ES] = k1 [Et] [S] / (k1 [S] + k2 + k3) = [Et] [S] / {[S] + (k2 + k3) / k1}
= [Et][S] / {[S] + KM } [ где Km = (k2 + k3) / k1 = константа Михаэлиса]
при условии [ES] = [Et] скорость реакции становится максимальной Vmax = k3 [ES] = k3 [Et]
отсюда v0 = k3 [ES] = k3 {[Et] [S] / { [S] + Km } = Vmax [S] / { [S] + KM }
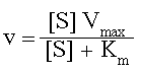 (уравнение Mихаэлиса -Ментен)
(уравнение Mихаэлиса -Ментен)
|
 2015-10-16
2015-10-16 561
561








