Стан системи, яка знаходиться у термодинамічній рівновазі, може бути визначений сукупністю властивостей. Усі величини, які характеризують будь-яку макроскопічну властивість системи, називаються термодинамічними параметрами. Розрізняють параметри зовнішні та внутрішні.
Зовнішні термодинамічні параметри задаються співвідношенням зовнішніх тіл по відношенню до системи, що розглядається (наприклад, об’єм системи, напруженість силового поля і т.ін.
Внутрішні термодинамічні параметри визначаються сукупним рухом і розподілoм у просторі системи часток, які входять до її складу (наприклад, щільність, тиск, енергія і т.ін.).
Будь-який стан системи описується мінімум двома параметрами, один з який є величиною екстенсивною, а інший – інтенсивною.
Значення екстенсивних параметрів є пропорційними масі і тому мають властивість адитивності. Це – об’єм системи, число її молей, маса.
Інтенсивні параметри описують специфічні властивості системи у даному стані і не залежать від маси. Величини їх не адитивні, вони можуть мати одне й те ж значення для усієї системи або змінюватися від точки до точки. Це – усі молярні і питомі властивості, температура, тиск.
Зазвичай, в якості незалежних термодинамічних параметрів вибирають інтенсивні властивості.
Термічний стан Q системи описується ентропією S (екстенсивний параметр) і температурою Т (інтенсивний параметр):
Q=TS (1)
Аналогічно механічний стан А системи характеризується об’ємом V (екстенсивний параметр) і тиском p (інтенсивний параметр):
A=pV (2)
Аналогічно Wi – хімічну енергію i-компоненту системи можна представити у вигляді добутку двох параметрів: кількості молей i-компоненту – nі (екстенсивний параметр) і його хімічного потенціалу 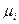 (інтенсивний параметр):
(інтенсивний параметр):
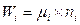 (3)
(3)
 2015-10-13
2015-10-13 3155
3155
