Кафедра общей химии
ОТЧЕТ
По лабораторной работе № 4
"Тепловые эффекты при растворении"
Студент: _________________________
Группа:___________________________
Дата выполнения:__________________
Преподаватель:____________________
Определение энтальпии гидратации безводного cульфата меди (II)
Цели опыта
· Определить значение энтальпии растворения безводного сульфата меди (II).
· Рассчитать значение энтальпии его гидратации.
· Составить термохимическое уравнение гидратации безводного сульфата меди (II).
Процесс растворения безводного сульфата меди (II),
CuSO4(к) = CuSO4(р), ΔН,
можно представить как двухстадийный: гидратация безводного сульфата меди (II)
CuSO4(к) + 5H2O(ж) = CuSO4 · 5H2O(к), ΔН1;
и растворение кристаллогидрата меди (II)
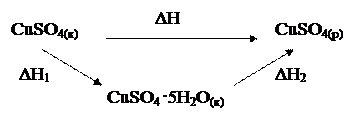 |
CuSO4 ·5H2O(к) = CuSO4(р) + 5H2O(ж), ΔН2.
Согласно закону Гесса,
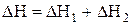 ,
,
откуда энтальпия гидратации безводного сульфата меди (II)
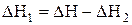
где ΔН рассчитывают по результатам эксперимента;
ΔН2 = 11,48 кДж/моль.
 2015-10-13
2015-10-13 5231
5231







